لیزین
| لیزین | |||
|---|---|---|---|
| |||
Lysine | |||
دیگر نامها 26-diaminohexanoic acid | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۷۰-۵۴-۲ DL | ||
| پابکم | ۸۶۶ | ||
| کماسپایدر | ۸۴۳ | ||
| KEGG | C16440 | ||
| ChEBI | CHEBI:25094 | ||
| ChEMBL | CHEMBL۲۸۳۲۸ | ||
| IUPHAR ligand | 724 | ||
| کد اِیتیسی | B05 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | C6H14N2O۲ | ||
| جرم مولی | ۱۴۶٫۱۹ g mol−1 | ||
| انحلالپذیری در آب | 1.5kg/L @ 25 °C[۱] | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
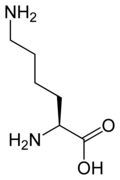
لیزین (نماد: Lys یا K) یکی از بیست آمینو اسید اصلی یاختههای زنده است. لیزین یک α-آمینو اسید است که در بیوسنتز پروتئینها استفاده میشود و حاوی یک گروه α-آمینو (که در شرایط بیولوژیکی پروتونیزه شده و به −NH3+ تبدیل میشود)، یک گروه α-کربوکسیلیک اسید (که در شرایط بیولوژیکی پروتون از دست داده و به −COO− تبدیل میشود) و یک زنجیر جانبی لیزیل (CH2)4NH2)) است و به عنوان یک آمینو اسید آلیفاتیک، باردار در پیاچ فیزیولوژیک و قلیایی طبقهبندی میشود. لیزین توسط کدونهای AAA و AAG کدگذاری میشود.
مانند تقریباً تمام اسیدهای آمینهٔ دیگر، α-کربن آن کایرال بوده و لیزین ممکن است به صورت دو انانتیومر (ایزومر نوری) L و D یا مخلوط راسمیک از هر دو انانتیومر وجود داشته باشد. تنها انانتیومر L-Lysine از نظر بیولوژیکی فعال بوده و α-کربن آن در پیکربندی S قرار دارد. بدن انسان نمیتواند لیزین را سنتز کند، بنابراین در انسان یک اسید آمینهٔ ضروری محسوب میشود و باید از غذا بهدست آید. در موجوداتی که سنتز لیزین دارند، دو مسیر اصلی بیوسنتز هست که عبارتاند از مسیر diaminopimelate و مسیر α-aminoadipate که از آنزیمها و سوبستراهای مختلف استفاده میکنند و در جانداران مختلف یافت میشوند. کاتابولیسم لیزین از طریق یکی از مسیرهای مختلف رخ میدهد، که شایعترین مسیر saccharopine است.
لیزین چندین نقش را در انسان ایفا میکند، مهمترین آنها پروتئینزایی است، اما همچنین در ارتباط متقابل پلیپپتیدهای کلاژن، جذب مواد معدنی مغذی ضروری و تولید کارنیتین، که کلیدی در متابولیسم اسیدهای چرب است نقش دارد. لیزین اغلب در تغییرات هیستون دخالت دارد و در نتیجه، اپیژنوم را متأثر میکند. گروه ε-آمین اغلب در پیوند هیدروژنی و به عنوان یک پایهٔ کلی در کاتالیز شرکت میکند.
گروه ε-آمونیوم (NH3+)به کربن چهارم از α-کربن چسبیدهاست که آن خود به گروه کربوکسیل (C=OOH) متصل است. با توجه به اهمیت آن در چندین فرایند بیولوژیکی، نبودن لیزین میتواند منجر به بیماریهای مختلفی از جمله نقص در مفاصل، اختلال در متابولیسم اسیدهای چرب، کمخونی و کمبود سیستمیک انرژی پروتئینی شود. در مقابل، تجمع بیش از حد لیزین، ناشی از کاتابولیسم ناکارآمد آن، میتواند به مشکلات شدید عصبی بینجامد. لیزین نخستین بار توسط زیستشیمیدان آلمانی به نام فردیناند هاینریش ادموند درشل در سال ۱۸۸۹ از پروتئین کازئین موجود در شیر جدا شد. او آن را «لیزین» نامید. در سال ۱۹۰۲، شیمیدان آلمانی امیل فیشر و فریتز ویگرت، ساختار شیمیایی لیزین را با سنتز آن مشخص کردند.
مسیرهای سوختوساز[ویرایش]
لیزین: سطح پایین لیزین باعث افت سنتز پروتئین شده و روی تشکیل کلاژن و ماهیچه تأثیر میگذارد.
لیزین و ویتامین ث با یکدیگر ال-کارنیتین را میسازند که سلولهای ماهیچهای را توانا به مصرف اکسیژن میکند. این خاصیت، لیزین را به یک مادهٔ منحصربهفرد برای ورزشهای استقامتی تبدیل کردهاست. لیزین یکی از ۲۰ آمینو اسیدی است که پروتئین را میسازند و بدن انسان نمیتواند این آمینو اسید را بسازد و باید از طریق مواد غذایی تأمین شود. لیزین یک باز است. در فراوردههای حیوانی، مانند گوشت، تخممرغ، پنیر و برخی از ماهیها یافت میشود و همچنین در برخی از گیاهان مانند دانههای سویا و لوبیا وجود دارد.
اهمیت لیزین[ویرایش]
لیزین به عنوان یکی از اسیدهای آمینهٔ ضروری، یکی از مهمترین اسیدهای آمینهای بوده که با هدف تحریک هورمون رشد از آن استفاده میشدهاست. میتوان گفت پس از اسید آمینهٔ آرژینین این اسید آمینهٔ لیزین است که شهرت بیشتری در میان اسیدهای آمینه در این زمینه دارد. هرچند مقادیر زیاد لیزین و آرژینین نقش رقابتی با هم دارند.
میزان نیاز روزانه[ویرایش]
میزان نیاز روزانه به اسید آمینهٔ لیزین ۳۸ میلیگرم به ازای هر کیلوگرم وزن بدن است.
کمبود لیزین در بدن[ویرایش]
کمبود دریافت لیزین در افراد ورزشکار موجب اشکال در تولید پروتئین و نبودِ سازگاری طبیعی نسبت به استرسها در تمرینات قدرتی و استقامتی میشود. محدودیت در این فرایند سازگاری باعث ایجاد اشکال در ترمیم بافت ماهیچهای، تولید پادتن و سلامت استخوانها میگردد.
گروهای در معرض خطر کمبود لیزین[ویرایش]
- کسانی که رژیم غذایی از نوع کاهش وزن دارند.
- گیاهخواران
عوامل خطرزای کمبود لیزین[ویرایش]
- کسانی که کاهش وزن ماهیچهای را تجربه کردند.
- بازیابی ضعیف پس از جلسات تمرین
- گیاهخواری
جستارهای وابسته[ویرایش]
منابع[ویرایش]
Skidmore-Roth, Y.L. , Mosby’s Handbook of Herbs & Natural Supplements. St. Louis: Mosby; 2001. 1032 p.
Nutritional ergogrnic aids / edited by Ira Wolinsky , Judy A.Driskell. CRC Press. 2004
پانویس[ویرایش]
- ↑ «Lysine - Cas 56-87-1 - Peptide Guide». بایگانیشده از اصلی در ۲۴ آوریل ۲۰۱۲. دریافتشده در ۵ مه ۲۰۱۲.