گلایسین
برای تأییدپذیری کامل این مقاله به منابع بیشتری نیاز است. (مارس ۲۰۱۸) |
| گلایسین[۱] | |||
|---|---|---|---|
| |||
| |||
گلایسین | |||
دیگر نامها آمینواتانوئیک اسید | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۵۶-۴۰-۶ | ||
| پابکم | ۷۵۰ | ||
| کماسپایدر | ۷۳۰ | ||
| UNII | TE7660XO1C | ||
| EC-number | 200-272-2 | ||
| دراگبانک | DB00145 | ||
| KEGG | D00011 | ||
| ChEBI | CHEBI:15428 | ||
| ChEMBL | CHEMBL۷۷۳ | ||
| IUPHAR ligand | 727 | ||
| کد اِیتیسی | B05 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | C2H5NO۲ | ||
| جرم مولی | ۷۵٫۰۷ g mol−1 | ||
| شکل ظاهری | جامد سفیدرنگ | ||
| چگالی | 1.607 گرم/سانتیمتر3 | ||
| دمای ذوب | ۲۳۳ °سانتیگراد (تجزیه) | ||
| انحلالپذیری در آب | 24.99 گرم/100 میلیلیتر (25 °C)[۲] | ||
| انحلالپذیری | محلول در اتانول، پیریدین نا محلول در اتر | ||
| اسیدی (pKa) | 2.34 (carboxyl) 9.6 (amino)[۳] | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
 | |
| شناسهها | |
|---|---|
| مخفف سهحرفی | Gly |
| زنجیر جانبی | هیدروژن |
| بار زنجیر جانبی | بدون بار |
| ویژگیها | |
| فرمول شیمیایی | C2H5NO2 |
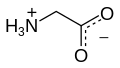
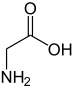
گلایسین یا گلیسین (به انگلیسی: Glycine) با نماد Gly یا G ، سادهترین اسید آمینه پایدار در تمام یاختههای زنده و در بین آمینو اسیدهاست. این اسید آمینه سبکترین و تنها اسید آمینهی غیر کایرال است. کدهای ژنتیکی این اسید آمینه عبارتند از: GGU, GGC, GGA و GGG. گلایسین یکی از ۲۰ اسید آمینه پروتئینزا است که پروتئینها را میسازند. این آمینو اسید آمفیپاتیک است و دارای هر دو سر آبگریز و آبدوست است.
تاریخچه[ویرایش]
هنری براکونات شیمیدان فرانسوی در سال ۱۸۲۰ گلایسین را با هیدرولیز کردن ژلاتین کشف کرد. وی به منظور هیدرولیز کردن ژلاتین، آن را به همراه سولفوریک اسید جوشاند.[۴]در ابتدا او نام ماده بهدست آمده را «شکر ژلاتین» نامید[۵][۶] اما ژان-بتیست بوسانگو شیمیدان فرانسوی نشان داد که این ماده شامل نیتروژن است.[۷] دانشمند آمریکایی Eben Norton Horsford و پس از آن یوستوس فون لیبیش یک دانشجوی شیمی آلمانی، واژه گلیکوکال را پیشنهاد دادند[۸][۹] اما یاکوب برسلیوس شیمیدان سوئدی نام سادهتر گلایسین را ارائه داد[۱۰][۱۱] این نام از واژه یونانی γλυκύς به معنای شیرین گرفته شدهاست.[۱۲] (به پیشوندهای glyco- و gluco- نیز ارتباط دارد، مانند گلیکوپروتئین و گلوکز). در سال ۱۸۵۸ شیمیدان فرانسوی آگوست آندره توماس کاهورس مشخص کرد که گلایسین، یک آمین از استیک اسید است.[۱۳]
ویژگیها[ویرایش]
گلایسین دارای یک اتم هیدروژن در زنجیر جانبی خود است. به همین دلیل این آمینو اسید پایدار هست و به راحتی به آمینو اسیدهای دیگر تبدیل نمیشود. گلایسین، فراوانترین آمینو اسید در کلاژن است و همچنین بهعنوان یک ناقل عصبی شناخته شدهاست.
اکثر پروتئینها مقداری خیلی کمی گلایسین دارند به استثنای گیلاتین و کولاگین که دارای ۲۵–۳۰٪ گلایسین هستند. بدن انسان مقدار زیادی گلایسین نیاز دارد برای اینکه جگر انسان بتواند کارش را بهخوبی انجام دهد.
این آمینو اسید غیر قطبی است اما در واکنشهای آب گریز شرکت نمیکند. ساختار ساده و کوچک این آمینو اسید و تبادل یک هیدروژن با زنجیره جانبی باعث شده تا در محیطهای مختلف خواص اسیدی و بازی متفاوتی از خود نشان دهد.
کاربردها[ویرایش]
مواد غذایی انسان و حیوان
اهمیت تغذیهای گلایسین دلیل استفادهٔ گستردهٔ آن در موادغذایی نیست بلکه بهعلت خاصیت نگهدارندگی، خوشبو بودن و همچنین شیرینی ملایم این ماده، از آن استفاده میشود و این ماده طعم ناخوشایند ساخارین را از بین میبرد. از ترکیب گلایسین و فلزات مانند "گلایسینات مس (II)" به عنوان مکمل خوراک دام استفاده میشود.[۱۴]
جستارهای وابسته[ویرایش]
منابع[ویرایش]
- ↑ Merck 11th-4386.
- ↑ «Solubilities and densities». بایگانیشده از اصلی در ۱۲ سپتامبر ۲۰۱۷. دریافتشده در ۲ مه ۲۰۱۲.
- ↑ Dawson, R.M.C. , et al. , Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ R.H.A. Plimmer (1912) [1908]. R.H.A. Plimmer; F.G. Hopkins (eds.). The chemical composition of the proteins. Monographs on biochemistry. Vol. Part I. Analysis (2nd ed.). London: Longmans, Green and Co. p. 82. Retrieved January 18, 2010.
- ↑ Braconnot, Henri (1820). "Sur la conversion des matières animales en nouvelles substances par le moyen de l'acide sulfurique" [On the conversion of animal materials into new substances by means of sulfuric acid]. Annales de Chimie et de Physique. 2nd series (به فرانسوی). 13: 113–125. ; see p. 114.
- ↑ MacKenzie, Colin (1822). One Thousand Experiments in Chemistry: With Illustrations of Natural Phenomena; and Practical Observations on the Manufacturing and Chemical Processes at Present Pursued in the Successful Cultivation of the Useful Arts … (به انگلیسی). Sir R. Phillips and Company.
- ↑ Boussingault (1838). "Sur la composition du sucre de gélatine et de l'acide nitro-saccharique de Braconnot" [On the composition of sugar of gelatine and of nitro-glucaric acid of Braconnot]. Comptes Rendus (به فرانسوی). 7: 493–495.
- ↑ Horsford, E.N. (1847). "Glycocoll (gelatine sugar) and some of its products of decomposition". The American Journal of Science and Arts. 2nd series. 3: 369–381.
- ↑ Ihde, Aaron J. (1970). The Development of Modern Chemistry (به انگلیسی). Courier Corporation. ISBN 978-0-486-64235-2.
- ↑ Berzelius, Jacob (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Annual Report on the Progress of Chemistry and Mineralogy). Vol. vol. 47. Tübigen, (Germany): Laupp. p. 654.
{{cite book}}:|volume=has extra text (help) From p. 654: "Er hat dem Leimzucker als Basis den Namen Glycocoll gegeben. … Glycin genannt werden, und diesen Namen werde ich anwenden." (He [i.e., the American scientist Eben Norton Horsford, then a student of the German chemist Justus von Liebig] gave the name "glycocoll" to Leimzucker [sugar of gelatine], a base. This name is not euphonious and has besides the flaw that it clashes with the names of the rest of the bases. It is compounded from γλυχυς (sweet) and χολλα (animal glue). Since this organic base is the only [one] which tastes sweet, then it can much more briefly be named "glycine", and I will use this name.) - ↑ Nye, Mary Jo (1999). Before Big Science: The Pursuit of Modern Chemistry and Physics, 1800-1940 (به انگلیسی). Harvard University Press. ISBN 978-0-674-06382-2.
- ↑ "glycine". Oxford Dictionaries. Archived from the original on 13 November 2014. Retrieved 2015-12-06.
- ↑ Cahours, A. (1858). "Recherches sur les acides amidés" [Investigations into aminated acids]. Comptes Rendus (به فرانسوی). 46: 1044–1047.
- ↑ «Ullmann's Encyclopedia of Industrial Chemistry».