پپتید
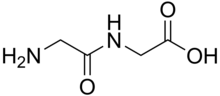


پـِپتید (Peptide از واژهٔ یونانی πεπτίδια به معنی: گواردنی کوچک، گوارَک) بسپار (پلیمر)های کوچکی هستند که از به هم پیوستن اسیدهای آمینه با ترتیب مشخصی و با پیوند پپتیدی تشکیل شدهاند.
تعریف[ویرایش]
پیوندهای پپتیدی پیوندهای شیمیایی کووالانسیای اند که هنگامی تشکیل میشوند که گروه کربوکسیل یک اسید آمینه با گروه آمینی دیگری واکنش کند. به بیانی دیگر پپتیدها آمیدهایی هستند که به واسطه اثر متقابل بین گروههای آمینو و کربوکسیل آمینواسیدها تشکیل میشوند، در چنین ترکیبهایی گروه آمینو -NHCO-، به نام اتصال یا پیوند پپتیدی نامیده میشود. وجه تمایز بین آنها بر اساس تعداد باقیماندههای اسید آمینه در هر مولکول میباشد، که بر این اساس به عنوان دیپپتید، تریپپتید و غیره و در نهایت پلیپپتید خوانده میشوند. پروتئینها، مولکولهای بسپپتیدی (پلی پپتیدی) ای هستند که از کنار هم قرار گرفتن چندین واحد پلی پپتیدی چه به صورت خطی و چه به شکلهای موضعی، سه بعدی یا حتی چند زیرواحد پلیپپتیدی که به شکل فضایی در کنار هم قرار میگیرند، موسوم به ساختار نوع چهارم، تشکیل میشوند.
تمایز بین آنها در این است که پپتیدها رشتههایی کوتاه و پلیپپتیدها و پروتئینها رشتههایی بلند از اسید آمینه هستند. به عبارتی تمایز بین آنها در تعداد پپتیدهای تشکیل دهنده زنجیره میباشد. کوتاهترین پپتیدها دی پپتیدها هستند، که شامل دو اسید آمینه پیوند شده توسط یک پیوند پپتیدی ساده میباشند، و بعد از آن تری پپتید، تترا پپتید و … یک بس پپتید (پلی پپتید) یک زنجیره طولانی، پیوسته و بدون شاخه از اسیدهای آمینه است. همچنین پپتیدها از پروتئینها بر اساس اندازه تمیز داده میشوند و به عنوان یک قرارداد شامل پنجاه اسید آمینه یا کمتر هستند.[۱] پروتئینها شامل یک یا بیشتر از پلی پپتیدهایی هستند که بر اساس کارکرد زیستشناسیشان در کنار هم قرار گرفتهاند، این دستهها اغلب با لیگاندهایی همچون کوآنزیمها، کوفاکتورها یا پروتئینهای دیگر یا درشتمولکول دیگری (همچون DNA ,RNA و …) یا مجموعههای بزرگ مولکولی پیچیده پیوند تشکیل میدهند. در نهایت هر چند آنچه که در تکنیکهای آزمایشگاهی به منظور تعیین یا تشخیص به کار برده میشوند در مورد پپتیدها متفاوت است با پلی پپتیدها و پروتئینها، (به عنوان نمونه تعیین و تشخیص با روشهای الکتروفورز، کروماتوگرافی و غیره)، با این همه مرز مشخصی بین پپتیدها و پلی پپتیدها یا پروتئینها وجود ندارد. پپتیدهای بلند زنجیره مانند بتا-آمیلویید به عنوان پروتئین مورد مطالعه قرار میگیرند و پروتئینهای کوچکتر مانند انسولین به عنوان پپتید. از این رو پپتیدها در ردیف مواد شیمیایی چندپار(اولیگومر) و بسپار(پلیمر) قرار میگیرند در حالی که همچنان جز اسیدهای نوکلییک، اولیگوساکاریدها و پلیساکاریدها طبقهبندی میشوند.
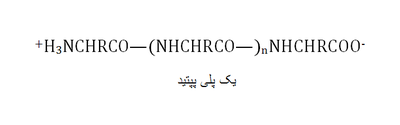
اسیدهای آمینهای که در زمره پپتیدها جای داده میشوند، باقی مانده[۲] واکنشی هستند که در طی آن یا یک یون هیدروژن از پایانه آمینی یا یک یون هیدروکسیل از پایانه کربوکسیلی یا هر دو آزاد میشوند، همچنانکه یک مولکول آب در طی تشکیل هر پیوند آمیدی آزاد میشود. همه پپتیدها به جز پپتیدهای حلقوی دارای یک پایانه نیتروژنی و یک پایانه کربنی هستند (همانطور که در شکل تتراپپتید نشان داده شدهاست).
در نمایش ساختمانهای پپتیدی، بر حسب قرارداد، باقیمانده اسید آمینه انتهایی N- (دارای گروه آمینو آزاد) در منتهیالیه سمت چپ و باقی مانده اسید آمینه انتهایی -C(دارای گروه کربوکسیل آزاد) در منتهیالیه سمت راست نوشته میشود.
مطالعه پپتیدها بهطور عمده گامی به سوی درک ترکیبهای پیچیدهتر، یعنی پروتئینها بودهاست. به هر حال پپتیدها به نوبه خود ترکیبهای بسیار مهمی هستند: به عنوان مثال: تری پپتید گلوتاتیون در بیشتر سلولهای زنده یافت میشود؛ آلفا-کورتیکوتروپین، که از ۳۹ باقیمانده آمینو اسید تشکیل میشود، بخشی از هورمون آدرنوکورتیکوتروپین ACTH است. از مدتها قبل معلوم شده بود نوناپپتید اکسی توسین که از لوب خلفی هیپوفیز ترشح میشود، دارای خاصیت تحریکی در انقباض عضله رحم است. تحقیقات نشان دادهاند که پپتیدهایی نسبتاً کوچک بر روی لذتهای تماسی و جنسی پستانداران مؤثرند. این پپتیدها بر روی همخوابگی، در آغوش گرفتن فرزند و حتی معاشرت و مراوده با مردمان تأثیر میگذارند. این ترکیبها به هورمون ارضا موسومند و راهنمای لذت خوانده میشوند.[۳]
دستهبندی پپتیدها[ویرایش]
پپتیدها بر اساس چگونگی تشکیلشان به گروههای مختلف دستهبندی میشوند.
پپتیدهای شیر[ویرایش]
پپتیدهای شیر در یک روند طبیعی طی شکست آنزیمی توسط آنزیمهای هضمکننده از پروتئین کازیین شیر به وجود میآیند. آنها همچنین میتوانند از پروتئینازِ لاکتوباسیلی در طی تخمیر شیر نیز ایجاد شوند. کازیین خانوادهای از پروتئینهای هتروژن بوده که به چهار گروه آلفا کازیین، بتا کازیین، گاما کازیین و کاپا کازیین تقسیم میشوند؛ کازیین منبع غنی پپتیدهای زیست فعال است. این پپتیدها علاوه بر ارزش تغذیهای بالا، دارای ویژگیهای بیولوژیکی و فیزیولوژیکی متعددی هستند. اثرات ضد سرطانی، ضد پوسیدگی دندان، ضد باکتریایی و ضد ویروسی، هیپوکلسترولمی،[۴] ضد پرفشاری خون و نیز تنظیم پاسخهای ایمنی تأیید شدهاند.[۵]
پپتیدهای ریبوزومی[ویرایش]
پپتیدهای ریبوزومی توسط ترجمه mRNA ساخته میشوند. آنها اغلب دستمایه پروتئین کافت[۶] به منظور ساخت شکل کامل پروتئینها قرار میگیرند. این ترکیبها نوعاً در ارگانیسمهای تکامل یافته تر، به عنوان هورمون و مولکولهای نشانهگذار[۷] عمل میکنند. بعضی از ارگانیسمها، پپتیدها را به عنوان پادزیست[۸] تولید میکنند، مانند میکروسینها.[۹] از آنجا که آنها اجزای سلولی-مولکولیِ ترجمه شدهاند، باقییماندههای آمینواسیدی محدود میشوند به استفاده توسط ریبوزومها. به هر حال، در این پپتیدها، بهطور متناوب تعدیلاتی بعد از ترجمه رخ میدهد همچون فسفریلاسیون،[۱۰] هیدروکسیلاسیون،[۱۱] سولفوناسیون،[۱۲] پالمیتولاسیون،[۱۳] گلیکوزیلاسیون[۱۴] و تشکیل دی سولفید. پپتیدهای ریبوزومی معمولاً خطی هستند، اگرچه ساختمانهای قوسی[۱۵] نیز مشاهده شدهاند. گاهی تغییرات ساختمانی نامتعارف بیشتری رخ میدهد، مانند راسمیزاسیون[۱۶] L-آمینواسیدها به D-آمینواسیدها در سم موجود در زهر نوکاردکی.
پپتیدهای غیرریبوزومی[ویرایش]
پپتیدهای غیر ریبوزومی به جای ریبوزوم توسط آنزیمهایی ساخته میشوند که مختص هر پپتید هستند. معروفترین پپتید غیر ریبوزومی گلوتاتیون[۱۷] است، که یک جز سازنده سیستمهای دفاعی ضد اکسنده[۱۸] در بیشتر ارگانیسمهای هوازی از جمله انسان میباشد. بقیه انواع پپتیدهای غیر ریبوزومی بیشتر در ارگانیسمهای تک سلولی، گیاهان و قارچها وجود دارند و توسط کمپلکسهای آنزیمی پیمانهای[۱۹] که سنتتازهای پپتیدی غیر ریبوزومی[۲۰] نامیده میشوند، ساخته میشوند. این کمپلکسها اغلب در وضعیتی مشابه پدید میآیند، و میتوانند شامل قسمتهای متفاوت زیادی جهت اجرای یک سری متنوع از دستکاریهای شیمیایی در توسعه محصولات باشند. این پپتیدها اغلب حلقوی هستند و میتوانند ساختمانهای حلقوی بسیار پیچیدهای داشته باشند، اگر چه پپتیدهای غیر ریبوزومی خطی هم معمول هستند. از هنگامیکه سیستمهای ماشینی برای ساخت اسیدهای چرب و پلیکتیدها به راه افتادند، اغلب ترکیبهای هیبرید دیده میشوند. وجود اکسازول[۲۱] یا تیازول[۲۲] اغلب نشان میدهد که ترکیب مورد نظر به روشهای ماشینی ساخته شدهاست.
پپتونها[ویرایش]
پپتون[۲۳] ترکیبی با تعداد محدودی اسید آمینه، معمولاً بین ۳ تا ۱۰ اسید آمینه است که از تجزیه(هیدرولیز) پروتئین معمولاً شیر و گوشت حیوانی بدست میآید. پپتونها در رشد باکتریها و قارچها به عنوان واسطه تغذیهای عمل میکنند. باکتریها و سلولها جهت رشد و نمو خود نیاز به منبع کربن و نیتروژن دارند که پپتونها مهمترین و اصلیترین منبع نیتروژن جهت رشد و نمو آنها هستند. پپتونها معمولاً به صورت پودر یا گرانول و به روش اسپری-درایر[۲۴] تهیه میشوند و در آب و حلالهای آبی محلولند.
پپتونها در صنایع مختلف مانند موسسات تولید واکسن و دارو، آرایشی و بهداشتی، کارخانههای تولید مخمر و مایه مخمر، تولید محیطهای کشت باکتریایی و سلولی از جمله در آزمایشگاههای تشخیص طبی، برخی صنایع غذایی تولیدکننده خوراکیهای فراوری شده و غذاهای آماده، همچنین تولید بستنی، تولید مکملها، کنسانتره، و خوراک دام و طیور[۲۵] و … و بسیاری دیگر از تولیدات فراوردههای زیستی (بیولوژیک) بهطور گسترده استفاده میشوند.
قطعههای پپتیدی[ویرایش]
قطعههای پپتیدی اشاره دارد به قطعاتی از پروتئین که جهت شناسایی کمی یا کیفی یک پروتئین معین استفاده میشوند. اغلب این قطعات پپتیدی محصول تخریب آنزیمی یا هیدرولیز جزئی یک پروتئین کامل هستند که در آزمایشگاه در شرایط کنترل شده روی نمونه انجام میشوند، اما از تخریب اجزای پروتئینی در شرایط طبیعی و تحت اثر عوامل تخریبی طبیعی نیز میتوانند ایجاد شوند.
سنتز پپتیدها[ویرایش]
از آنجا که پپتیدهای بلند زنجیره همان پروتئینها هستند، بنابراین سنتز پپتید در واقع به نوعی همان فرایند ساخت پروتئین است. اتصال آمینو اسیدهای مختلف به یکدیگر از طریق پیوندهای آمیدی یا پپتیدی منجر به سنتز پپتید یا در نهایت پروتئین خواهد شد.

پپتیدها در زیستشناسی مولکولی[ویرایش]
پپتیدها به چند دلیل در زیستشناسی مولکولی دارای اهمیت ویژهای شدهاند. اول اینکه پپتیدها اجازه تولید آنتیبادیهای پپتیدی را در حیوانات بدون نیاز به پالایش پروتئین مورد نظر میدهند. این شامل سنتز پپتیدهای آنتیژنیکِ پروتئین مورد نظر میشود. در آن صورت این پپتیدها برای ساخت آنتیبادی ضد پروتئین خرگوش یا موش میتوانند استفاده شوند.
دلیل دیگر این است که پپتیدها در اندازهگیری به روش طیفسنجی جرمی مورد استفاده قرار میگیرند؛ و به ما اجازه میدهند که پروتئینهای مورد نظر خود را بر اساس جرم یا توالی پپتیدها شناسایی کنیم. در این مورد پپتیدها اغلب توسط روش هضم درون ژلی[۲۶] بعد از جداسازی به روش الکتروفورزِ پروتئینها ایجاد میشوند.
پپتیدها اخیراً در مطالعه ساختمان و عملکرد پروتئین استفاده شدهاند. برای مثال پپتیدهای مصنوعی[۲۷] میتوانند در تعیین محل رخدادن کنش و واکنشهای بین پروتئین و پپتید به عنوان ردیاب استفاده شوند. همچنین پپتیدهای بازدارنده در تحقیقات بالینی جهت بررسی آثار پپتیدها روی جلوگیری از پیشرفت پروتئینهای سرطانی و دیگر بیماریها استفاده میشوند. برای مثال یکی از امیدوارانهترین کاربردها در این زمینه مطالعه پپتیدهایی است که به ساخت LHRH[۲۸] منتهی میشوند. این پپتیدهای ویژه به عنوان یک همکنش کننده[۲۹] عمل میکنند، به این معنی که به یک سلول به گونهای میچسبند که دریافتکنندههای LHRH را تحت کنترل درآورند. فرایند بازدارندگی سلولهای دریافتکننده هورمون، حکایت از این دارد که پپتیدها میتوانند در درمان سرطان پروستات سودمند باشند. اما پیش از نسبت دادن خواص ضد سرطانی به پپتیدها و اثبات آنچه که توسط پپتیدها به نمایش درآمدهاند، تحقیقات و آزمایشهای بیشتری لازم است تا با قطعیت بتوان آنها را پذیرفت.
خانوادههای معروف پپتید[ویرایش]
خانوادههای پپتیدهای مورد بحث در این بخش، پپتیدهای ریبوزومی هستند و معمولاً با فعالیت هورمونی. همه این پپتید بایگانیشده در ۳۰ نوامبر ۲۰۲۰ توسط Wayback Machineها توسط سلولها تا اندازه پروپپتیدها[۳۰] یا پروپروتئینها[۳۱] سنتز میشوند و پیش از خروج از سلول کوتاه میشوند و به داخل جریان خون جایی که آنها وظیفه نشانهگذاری خود را اجرا میکنند، جاری میشوند.
- پپتیدهای تاکیکینین[۳۲]
- ماده P[۳۳]
- کاسینین[۳۴]
- نوروکینین A[۳۵]
- اِلِدویسین[۳۶]
- نوروکینین B
- پپتیدهای وازو-اکتیو رودهای[۳۷]
- VIP (پپتید وازو-اکتیو رودهای؛PHM27)
- PACAP (پپتید فعالکننده آدنیلات سیکلاز مخاطی)[۳۸]
- پپتید PHI 27 (ایزولوسین هیستیدین27)[۳۹]
- GHRH 1-24 (هورمون آزادکننده هورمون رشد ۲۴–۱)[۴۰]
- گلوکاگون[۴۱]
- سکرتین[۴۲]
- پپتیدهای وابسته به پلیپپتیدهای لوزالمعدهای
- NPY (نوروپپتید Y)[۴۳]
- PYY (پپتید YY)[۴۴]
- APP (پلی پپتید لوزالمعدهای طیور)[۴۵]
- PPY (پلی پپتید لوزالمعدهای)[۴۶]
- پپتیدهای مخدره[۴۷]
- پپتیدهای پروپیوملانوکورتین (POMC)[۴۸]
- پنتا پپتیدهای انکفالین[۴۹]
- پپتیدهای پرودی نورفین[۵۰][۵۱]
- پپتیدهای کالسیتونین[۵۲]
- کالسیتونین
- آمیلین[۵۳]
- AGG01[۵۴]
- پپتیدهای دیگر
- پپتیدهای دافع نمک سدیم نوعB[۵۵] با علامت اختصاری BNP - در ماهیچه قلب تولید میشوند و در تشخیص بیماری کاربرد دارند.
- لاکتوتری پپتیدها[۵۶] - لاکتو تری پپتیدها ممکن است عامل کاهش فشار خون باشند، اگر چه شواهد هنوز روشن نیستند.
نقش پپتیدها در گرسنگی و سیری[ویرایش]
پپتیدهای موجود در معده و روده در سیری و گرسنگی نقش ایفا میکنند.
پپتیدهای سیری[ویرایش]
غذای هضم شده با گیرندههای تارهای معدی رودهای تعامل میکنند و نتیجهٔ این تعامل، آزاد شدن پپتیدها در جریان خون است. دهها پپتید (از جمله کولهسیستوکینین[۵۷] (CCK)، گلوکاگون، بومبزین،[۵۸] هورمون محرک آلفا ملانوسیت[۵۹] و سوماتوستاتین[۶۰]) مقدار غذا خوردن را کم میکنند. به ویژه دوز بسیار پایین از کولهسیستوکینین، اشتها و خوردن را کم میکند و بنابراین میتوان آن را «پپتید سیری» (یا پپتیدی که اشتها را کم میکند) در نظر گرفت.[۶۱]
پپتیدهای گرسنگی[ویرایش]
این پپتیدها اشتها را زیاد میکنند. این پپتیدها در مغز به ویژه هیپوتالاموس ساخته میشوند.[۶۲] معروفترین آنها عبارتند از:[۶۳] پپتید عصبی Y,[۶۴] گالانین،[۶۵] اورکسین A[۶۶] و گرلین[۶۷]
دکاپپتید[ویرایش]

دکاپپتید به پلی پپتیدهایی گفته میشود که از ده اسید آمینه تشکیل شدهاند. به عنوان نمونه، آنژیوتانسین I نوعی دکاپپتید است. دکا یکی از پیشوندهای SI است که برابر است با ده و علامت اختصاری آن در سیستم متریک da میباشد. پپتید (از واژهٔ یونانی πεπτίδια به معنی :هضم شدهٔ کوچک) , پلیمر کوچکی است که از به هم پیوستن اسیدهای آمینه با ترتیب مشخصی تشکیل شدهاست. آنژیوتانسین I نوعی دکاپپتید است که در سیستم رنین-آنژیوتانسین-آلدوسترون نقش بازی میکند. هورمون رهاکننده گنادوتروپین (GnRH) نیز نوعی دکاپپتید است که مسئول رهاسازی هورمون محرک فولیکول (FSH) و هورمون زردینه ساز (LH) از بخش جلویی غده هیپوفیز است.[۶۸][۶۹]
یادداشتهایی دربارهٔ واژگان[ویرایش]
طول پپتید:
- یک پلی پپتید یک زنجیره خطی منفرد از تعداد زیادی اسید آمینه است، که توسط پیوندهای آمیدی به هم متصل شدهاند.
- یک پروتیین تشکیل شده از یک یا بیشتر پلیپپتید (طول آن بیشتر از ۵۰ اسید آمینه است).[۷۰]
- یک اولیگوپپتید شامل فقط تعداد کمی اسید آمینه است (بین ۲ تا ۲۰).
تعداد اسیدهای آمینه
- مونو پپتید یک اسید آمینه در ساختار خود دارد.
- دی پپتید دو اسید آمینه در ساختار خود دارد.
- تری پپتید سه اسید آمینه در ساختار خود دارد.
- تترا پپتید چهار اسید آمینه در ساختار خود دارد.
- پنتا پپتید پنج اسید آمینه در ساختار خود دارد.
- هگزا پپتید شش اسید آمینه در ساختار خود دارد.
- هپتا پپتید هفت اسید آمینه در ساختار خود دارد.
- یک اکتا پپتید (مثل انجیو تنسین II)[۷۱] هشت اسد آمینه در ساختار خود دارد.
- یک نونا پپتید (مثل اکسی توسین[۷۲]) نُه اسید آمینه در ساختار خود دارد.
- یک دکا پپتید (مثل هورمون آزادکننده گنادوتروپین[۷۳] و نیز آنجیو تنسین I[۷۴]) ده اسید آمینه در ساختار خود دارد.
- آندکا پپتید (یا مونو دکا پپتید)[۷۵] یازده اسید آمینه در ساختار خود دارد، دو دکا پپتید (یا دی دکا پپتید) دوازده اسید آمینه، تری دکا پپتید سیزده اسید آمینه و همینطور الی آخر.
- آیکوسا پپتید[۷۶] بیست اسید آمینه در ساختار خود دارد، تریکونتا پپتید سی اسید آمینه، تتراکونتا پپتید چهل اسید آمینه[۷۷] و همینطور الی آخر.
کارکرد
- یک نوروپپتید[۷۸] پپتیدی است که در ارتباط با بافت عصبی فعالیت میکند.
- یک لیپو پپتید[۷۹] پپتیدی است که ساختار چربی در ساختمان خود دارد، و پپدوسینها[۸۰] لیپوپپتیدهایی هستند که با GPCRها[۸۱] فعل و انفعال دارند.
- یک هورمون پپتیدی، پپتیدی است که به عنوان یک هورمون عمل میکند.
- یک پروتئوز[۸۲] مخلوطی پپتیدی است که توسط هیدرولیز پروتیین تشکیل میشود. این واژه هماکنون کمتر استفاده میشود.
دوپینگ در ورزش[ویرایش]
واژه پپتید در زمینه دوپینگ در ورزش بهطور نابجا یا در یک برداشت ناروشن به معنی هورمونهای پپتیدی و سکرتاگوگهای غیرقانونی به کار میرود: پپتیدهای سکرتاگوگیِ غیرمجاز تحت عنوان جدول شماره ۲ مواد ممنوعه (جدول S۲)، در فهرست مواد ممنوعه آژانس جهانی مبارزه با دوپینگ (WADA) طبقهبندی میشوند، و بنابراین برای استفاده توسط ورزشکاران حرفهای داخل و خارج مسابقات ممنوع شدهاند. چنین سکرتاگوگهای پپتیدی دست کم از سال ۲۰۰۸ در فهرست مواد ممنوعه آژانس جهانی مبارزه با دوپینگ بودهاند. کمیسیون جرم و جنایت استرالیا (در حالی که به اشتباه از واژه پپتید استفاده میکند) به سوء مصرف سکرتاگوگهای پپتیدی غیرمجاز در ورزش استرالیا از جمله پپتیدهای آزادکننده هورمون رشد CJC1295 و نیز CHRP-6[۸۳] و GHSR[۸۴] (ژن) و هگزارلین[۸۵] اشاره میکند. در حال حاضر بحثی روی قانونی بودن یا نبودن استفاده از سکرتاگوگهای پپتیدی در ورزش وجود دارد.
پانویس[ویرایش]
- ↑ در برخی منابع پپتیدهای با وزن مولکولی تا ۱۰۰۰۰ واحد را پلی پپتید و بیشتر از آن را پروتئین میخوانند. منبع ۱۶ جلد۲
- ↑ residue در مفهوم شیمیایی آن بایستی با واژههایی رساتر از پسمانده، باقیمانده، پساب، تفاله، بازمانده و … ترجمه شود. اما متأسفانه رساترین ترجمههای فعلی را باید از میان همین عبارتها برگزینیم.
- ↑ منبع ۱۷، ص ۱۳۹۶
- ↑ Hypocholestrolemia
- ↑ برای مطالعه بیشتر نگاه کنید به منبع ۱۸
- ↑ Proteolysis
- ↑ Signaling molecules
- ↑ Antibiotic
- ↑ microcins
- ↑ phosphorylation
- ↑ Hydroxylation
- ↑ Sulfonation
- ↑ Palmitoylation
- ↑ Glycosylation
- ↑ lariat structures
- ↑ راسمیک شدن Racemization
- ↑ glutathione
- ↑ antioxidant defenses
- ↑ modular enzyme complexes
- ↑ nonribosomal peptide synthetases
- ↑ oxazole
- ↑ thiazole
- ↑ Peptone
- ↑ Spray-drayer خشک کنهای افشان یا پاشنده
- ↑ مکمل و کنسانتره، ترکیبات واسطه پیش از تهیه خوراک نهایی مورد استفاده جهت پرورش دام یا طیور به شکل صنعتی هستند. غلیظترین شکل آن مکمل و رقیقتر از آن کنسانتره است. در صنعت دام کنسانتره معمولاً مستقیماً مورد مصرف دام قرار میگیرد، ولی در صنعت پرورش طیور کنسانتره پیش از مصرف بایستی در فرایندی جداگانه به خوراک آماده تبدیل (رقیق) شود.
- ↑ In-gel digestion هضم درون ژلی، بخشی از آمادهسازی نمونه در شناسایی پروتئین به روش تجزیه Proteomics میباشد. این روش اولین بار در سال ۱۹۹۲ توسط روزنفلد (نگا منبع ۲۰) معرفی شد.
- ↑ Synthetic
- ↑ Luteinizing Hormone-Releasing Hormone
- ↑ agonist آگونیست، همکنش کننده
- ↑ propeptides
- ↑ proproteins
- ↑ Tachykinin peptides
- ↑ Substance P
- ↑ Kassinin
- ↑ Neurokinin A
- ↑ Eledoisin
- ↑ Vasoactive intestinal peptides
- ↑ Pituitary Adenylate Cyclase Activating Peptide
- ↑ Peptide Histidine Isoleucine
- ↑ Growth Hormone Releasing Hormone
- ↑ Glucagon
- ↑ Secretin
- ↑ NeuroPeptide Y
- ↑ Peptide YY
- ↑ Avian Pancreatic Polypeptide
- ↑ Pancreatic Polypeptide
- ↑ Opioid Peptide
- ↑ Proopiomelanocortin (POMC) peptides
- ↑ Enkephalin pentapeptides
- ↑ همچنین به نام پرو انکفالین B نیز شناخته میشود.
- ↑ Prodynorphin peptides
- ↑ Calcitonin peptides
- ↑ Amylin
- ↑ نام آزمایشی یک پادزیست پپتیدی جدیدی است که در شیر کیسه داری به نام والابی تامار کشف شدهاست. قدرت آن صد بار بیشتر از پنیسیلین گزارش شدهاست.
- ↑ B-type Natriuretic Peptide(BNP)
- ↑ Lactotripeptides
- ↑ Cholecystokinin
- ↑ Bombesin
- ↑ Alpha-Melanocyte-stimulating hormone
- ↑ Somatostatin
- ↑ Ritter, 2004
- ↑ نگاه کنید به منبع ۱۹
- ↑ نگاه کنید به پانویس قبلی
- ↑ Neuropeptide Y
- ↑ Galanin
- ↑ Orexin-A, also known as hypocretin-1
- ↑ Ghrelin
- ↑ Campbell RE, Gaidamaka G, Han SK, Herbison AE (June 2009). "Dendro-dendritic bundling and shared synapses between gonadotropin-releasing hormone neurons". Proc. Natl. Acad. Sci. U.S.A. 106 (26): 10835–40. doi:10.1073/pnas.0903463106. PMC 2705602. PMID 19541658
- ↑ Basso N, Terragno NA (December 2001). "History about the discovery of the renin-angiotensin system". Hypertension 38 (6): 1246–9. doi:10.1161/hy1201.101214. PMID 11751697
- ↑ نگاه کنید به پانویس ۱
- ↑ Angiotensin II
- ↑ Oxytocin
- ↑ gonadotropin-releasing hormone
- ↑ Angiotensin I
- ↑ undecapeptide/monodecapeptide
- ↑ icosapeptide
- ↑ tricontapeptide/tetracontapeptide
- ↑ Neuropeptide
- ↑ Lipopeptide
- ↑ Pepducin
- ↑ G Protein-Coupled Receptor گیرندههای جفت شونده با پروتیین جی
- ↑ Proteose
- ↑ Growth Hormone-Releasing Peptide
- ↑ Growth Hormone Secretagogue Receptor
- ↑ Hexarelin
منابع[ویرایش]
- ۱.مشارکتکنندگان ویکیپدیا. «Peptide». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۶ آگوست ۲۰۱۵.
- ۲. Duquesne S, Destoumieux-Garzón D, Peduzzi J, Rebuffat S (2007). "Microcins, gene-encoded antibacterial peptides from enterobacteria". Natural Product Reports. 24 (4): 708–34. doi:10.1039/b516237h. PMID 17653356.
{{cite journal}}: Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ۳. Pons M, Feliz M, Antònia Molins M, Giralt E (1991). "Conformational analysis of bacitracin A, a naturally occurring lariat". Biopolymers. 31 (6): 605–12. doi:10.1002/bip.360310604. PMID 1932561.
{{cite journal}}: Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ۴. Torres AM, Menz I, Alewood PF; et al. (2002). "D-Amino acid residue in the C-type natriuretic peptide from the venom of the mammal, Ornithorhynchus anatinus, the Australian platypus". FEBS Letters. 524 (1–3): 172–6. doi:10.1016/S0014-5793(02)03050-8. PMID 12135762.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ۵. Meister A, Anderson ME (1983). "Glutathione". Annual Review of Biochemistry. 52 (1): 711–60. doi:10.1146/annurev.bi.52.070183.003431. PMID 6137189.
- ۶. Hahn M, Stachelhaus T (2004). "Selective interaction between nonribosomal peptide synthetases is facilitated by short communication-mediating domains". Proceedings of the National Academy of Sciences of the United States of America. 101 (44): 15585–90. doi:10.1073/pnas.0404932101. PMC 524835. PMID 15498872.
{{cite journal}}: Unknown parameter|month=ignored (help) - ۷. Finking R, Marahiel MA (2004). "Biosynthesis of nonribosomal peptides1". Annual Review of Microbiology. 58 (1): 453–88. doi:10.1146/annurev.micro.58.030603.123615. PMID 15487945.
- ۸. Payne JW (1976). "Peptides and micro-organisms". Advances in Microbial Physiology. 13: 55–113. doi:10.1016/S0065-2911(08)60038-7. PMID 775944.>
- ۹. Hummel J, Niemann M, Wienkoop S; et al. (2007). "ProMEX: a mass spectral reference database for proteins and protein phosphorylation sites". BMC Bioinformatics. 8: 216. doi:10.1186/1471-2105-8-216. PMC 1920535. PMID 17587460.
{{cite journal}}: Explicit use of et al. in:|author=(help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ۱۰. Webster J, Oxley D (2005). "Peptide mass fingerprinting: protein identification using MALDI-TOF mass spectrometry". Methods in Molecular Biology. 310: 227–40. doi:10.1007/978-1-59259-948-6_16. PMID 16350956.
- ۱۱. Marquet P, Lachâtre G (1999). "Liquid chromatography-mass spectrometry: potential in forensic and clinical toxicology". Journal of Chromatography. B, Biomedical Sciences and Applications. 733 (1–2): 93–118. doi:10.1016/S0378-4347(99)00147-4. PMID 10572976.
{{cite journal}}: Unknown parameter|month=ignored (help) - ۱۲. Bulinski JC (1986). "Peptide antibodies: new tools for cell biology". International Review of Cytology. 103: 281–302. doi:10.1016/S0074-7696(08)60838-4. PMID 2427468.
- ۱۳. C.Michael Hogan. 2011. sulfur. Encyclopedia of Earth, eds. Andy Jorgensen and C.J.Cleveland, National Council for Science and the environment, Washington DC
- ۱۴. Obesity: Pathology and Therapy J. C. G. Halford, J. E. Blundell Springer-Verlag Berlin Heidelberg ۲۰۰۰
- ۱۵. The temporal organization of ingestive behaviour and its interaction with regulation of energy balance Strubbe JH, van Dijk G. 2002 [۱]
- ۱۶. Robert Thornton Morrison,Robert Neilson Boyd, Organic Chemistry,sixth edition,Chapter 36(Amino Acids and peptides) 1992
- ۱۷. شیمی آلی III(جلد سوم)، موریسون و بوید، ویرایش ششم، ترجمه بکاولی، هروی، رحیمیزاده، نشر مشهد، ۱۳۸۳، فصل ۳۶
- ۱۸. مجله علوم تغذیه و صنایع غذایی ایران، سال هفتم، شماره ۵، ویژهنامه زمستان ۱۳۹۱، صفحات ۸۱۱ تا ۸۲۰، مقاله بررسی اثرات بیولوژیک کازیین و پپتیدهای زیست فعال شده مشتق از کازیین، رقیه شهبازی، سید حسین داوودی، سید امیر محمد مرتضویان، سعیده اسمعیلی
- ۱۹. روانشناسی فیزیولوژیک- جان پینل -ویراست چهارم۲۰۰۷- مهرداد فیروزبخت- نشر ویرایش- چاپ اول ۱۳۸۷-ص ۴۰۶.
- ۲۰. Rosenfeld J, Capdevielle J, Guillemot JC, Ferrara P (1992) In-gel digestion of proteins for internal sequence analysis after one- or two-dimensional gel electrophoresis. Anal Biochem 203:173–179

