کربن: تفاوت میان نسخهها
| [نسخهٔ بررسینشده] | [نسخهٔ بررسینشده] |
جزبدون خلاصۀ ویرایش |
←چرخه کربن: بازنویسی کامل |
||
| خط ۱۵۸: | خط ۱۵۸: | ||
=== چرخه کربن === |
=== چرخه کربن === |
||
{{اصلی|چرخه کربن}} |
{{اصلی|چرخه کربن}} |
||
در شرایط متداول بر روی زمین، تبدیل یک عنصر به دیگری، رخدادی بسیار نادر است. بنابراین مقدار کربن موجود بر روی زمین به میزان تقریبا کاملی، ثابت است. از همینرو، فرایندهایی که طی آنها کربن مصرف میشود، بایستی کربن مورد نیاز خود را از یک محل تهیه و کربن پسماند را در محلی دیگر دفع کنند. مسیرهای کربنی موجود در محیط زیست، تشکیل دهنده [[چرخه کربن]] هستند. برای مثال گیاهانی که [[فتوسنتز]] میکنند، کربن دیاکسید مورد نیاز خود را از هوا (یا آب دریا) دریافت میکنند و سپس آن را به زیستتوده تبدیل میکنند، همانند [[چرخه کالوین]] که طی آن کربن تثبیت میشود. برخی از این زیستتوده تولید شده، توسط حیوانات خورده میشود و مقداری دیگر از آن بهصورت کربن دیاکسید توسط حیوانات تنفس میکند. چرخه کربن در عمل، فرایندی پیچیدهتر از توصیفی است که در اینجا به آن اشاره شد. بهعنوان مثال، مقداری از کربن دیاکسیدی که در آب اقیانوسها حل میشود و گیاهان مرده یا مواد جانوری چنانچه توسط باکتریها مصرف نشوند، ممکن است به نفت یا زغالسنگ تبدیل شوند که میتوانند در زمان سوزانده شدن، موجبآزادسازی کربن دیاکسید شوند.<ref>{{cite journal|journal=Science|date=2000|volume=290|issue=5490|pages=291–296|doi=10.1126/science.290.5490.291|title=The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System|pmid=11030643|last1=Falkowski|first1=P.|last2=Scholes|first2=R. J.|last3=Boyle|first3=E. |last4=Canadell|first4=J.|last5=Canfield|first5=D.|last6=Elser|first6=J.|last7=Gruber|first7=N. |last8=Hibbard|first8=K.|last9=Högberg|first9=P.|s2cid=1779934|bibcode=2000Sci...290..291F|display-authors=8 }}</ref><ref>{{cite journal|doi=10.1007/BF01104986|title=The global terrestrial carbon cycle|date=1993|last1=Smith|first1=T. M.|last2=Cramer|first2=W. P.|last3=Dixon|first3=R. K.|last4=Leemans|first4=R.|last5=Neilson|first5=R. P.|last6=Solomon|first6=A. M.|journal=Water, Air, & Soil Pollution|volume=70|issue=1–4|pages=19–37|bibcode=1993WASP...70...19S}}</ref> |
|||
== مدل اتمی == |
== مدل اتمی == |
||
نسخهٔ ۲۵ ژوئن ۲۰۲۰، ساعت ۲۰:۰۲
گرافیت (راست) و الماس (چپ) ، دو دگرشکل کربن | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کربن | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| دگرشکلی | گرافیت، الماس، دگرشکلهای کربن | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| جرم اتمی استاندارد (Ar، استاندارد) | (۱۲٫۰۰۹۶، ۱۲٫۰۱۱۶) conventional: ۱۲٫۰۱۱ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کربن در جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اتمی (Z) | 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| گروه | ۱۴ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دوره | دوره ۲ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| بلوک | بلوک-p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دسته | نافلز, به عنوان یک شبهفلز در نظر گرفته میشود. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آرایش الکترونی | [He] 2s2 2p2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ۲٬۴ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای فیزیکی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| فاز در STP | جامد | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه تصعید | ۳۹۱۵ K (۳۶۴۲ °C, ۶۵۸۸ °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| چگالی (near r.t.) | آمورف: ۱٫۸–۲٫۱ g/cm3[۱] گرافیت: ۲٫۲۶۷ g/cm3 الماس: ۳٫۵۱۵ g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه سهگانه | ۴۶۰۰ K, ۱۰٬۸۰۰ kPa[۲][۳] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارت همجوشی | گرافیت: ۱۱۷ kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظرفیت حرارتی مولی | گرافیت: ۸٫۵۱۷ J/(mol·K) الماس: ۶٫۱۵۵ J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای اتمی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اکسایش | −4, −3, −2, −1, 0, +1,[۴] +2, +3,[۵] +4[۶] (یک اکسید اسیدی ملایم) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الکترونگاتیوی | مقیاس پائولینگ: ۲٫۵۵ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انرژی یونش |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع کووالانسی | pm sp3: ۷۷ pm sp2: ۷۳ pm sp: ۶۹ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع واندروالسی | ۱۷۰ pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دیگر ویژگی ها | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ساختار بلوری | گرافیت: دستگاه بلوری ششگوشه (سیاه) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ساختار بلوری | الماس: (شفاف) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعت صوت thin rod | الماس: ۱۸٬۳۵۰ m/s (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انبساط حرارتی | الماس: ۰٫۸ µm/(m·K) (at 25 °C)[۷] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانندگی گرمایی | گرافیت: ۱۱۹–۱۶۵ W/(m·K) الماس: ۹۰۰–۲۳۰۰ W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش الکتریکی | گرافیت: ۷٫۸۳۷ µΩ·m[۸] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش مغناطیسی | دیامغناطیس[۹] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| پذیرفتاری مغناطیسی | ۱۰-۶×۵.۹- (graph.) cm3/mol[۱۰] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول یانگ | الماس: ۱۰۵۰ GPa[۷] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول برشی | الماس: ۴۷۸ GPa[۷] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول حجمی | الماس: ۴۴۲ GPa[۷] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نسبت پواسون | الماس: ۰٫۱[۷] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی موس | گرافیت: ۱–۲ الماس: ۱۰ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شماره ثبت سیایاس |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| تاریخچه | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کشف | مصر باستان و سومر[۱۱] (۳۷۵۰ پیش از میلاد) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نام بردن به عنوان یک عنصر | آنتوان لاووازیه[۱۲] (۱۷۸۹) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایزوتوپهای کربن | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
کربن واژهای برگرفته از یک واژه لاتین بهنام کربو[a] بهمعنای زغالسنگ است. کربن عنصری شیمیایی با نماد C و عدد اتمی ۶ است. این عنصر، که در طبقه عناصر غیرفلزی جای میگیرد، چهارظرفیتی است، بهاین معنی که دارای چهار الکترون در دسترس برای تشکیل یک پیوند شیمیایی کووالانسی است. کربن متعلق به گروه چهاردهم در جدول تناوبی و دارای سه ایزوتوپ طبیعی است. این ایزوتوپها عبارتاند از کربن-۱۲ و کربن-۱۳ که ایزوتوپهای پایداری هستند و کربن-۱۴ که یک ایزوتوپ پرتوزا محسوب میشود و زمان نیمهعمر واپاشی آن حدود ۵۷۳۰ سال است. از دوران باستان تا سال ۱۶۹۹ میلادی تنها سیزده عنصر توسط بشر شناسایی شده بودند که کربن یکی از آنها است. از لحاظ فراوانی، کربن پانزدهمین عنصر در پوسته زمین و پس از هیدروژن، هلیم و اکسیژن، چهارمین عنصر در تمام کیهان است. فراوانی کربن، تنوع منحصر به فرد ترکیبات ساخته شده از آن و توانایی تشکیل بسپار در دماهای متداول قابل دسترسی بر روی زمین، موجب میشود که این عنصر به عنوان عنصر مشترک در تمامی انواع شکلهای شناخته شده از زندگی وجود داشته باشد. این عنصر به لحاظ جرم، پس از اکسیژن، دومین عنصر موجود در بدن انسان است (تشکیل دهنده حدود ۱۸٫۵ درصد از جرم بدن).
اتمهای کربن میتوانند به صورتهای مختلفی با یکدیگر پیوند برقرار نمایند که این موجب میشود دگرشکلهای متنوعی از کربن تشکیل شود. شناخته شدهترین نوع از دگرشکلهای کربنی، عبارتاند از گرافیت، الماس و فولرن. خواص فیزیکی کربن در هر کدام از دگرشکلهای کربنی متفاوت است. بهعنوان مثال گرافیت دارای ظاهری کدر و سیاهرنگ است، در حالیکه الماس کاملا شفاف است. گرافیت به قدری نرم است که میتواند برروی کاغذ اثری از خود برجا بگذارد و خود واژه گرافیت نیز از کلمهای یونانی بهمعنای نوشتن[b] برگرفته شدهاست. درحالیکه الماس، سختترین ترکیب طبیعی یافت شده بر روی زمین است. گرافیت یک هدایت کننده خوب جریان الکتریکی است، اما الماس یک هادی ضعیف جریان الکتریسیته است. در فشار معمولی، الماس، نانولولههای کربنی و گرافن، دارای بالاترین هدایت گرمایی در بین تمام ترکیبات شناخته شده هستند. آنها در مقابل تغییرات شیمیایی مقاوم هستند و برای این که با اکسیژن وارد واکنش شوند یا به عبارت دیگر برای این که سوزانده شوند، به دمای بالا نیاز دارند.
متداولترین حالت اکسایشی کربن در ترکیبات معدنی برابر با ۴+ است، در حالیکه عدد اکسایش ۲+ در موردی مانند کربن مونوکسید و کمپلکسهای کربونیلی فلزات واسطه قابل مشاهده است. بزرگترین منابع کربن معدنی عبارتاند از سنگ آهک، دولومیت و کربن مونوکسید. این در حالی است که مقادیر قابل توجهی از کربن بهصورت ذخیره شده در منابع آلی مانند زغالسنگ، تورب، نفت خام و آذریخ وجود دارد. کربن طیف گستردهای از ترکیبات را شامل میشود، بهطوری که دامنه آن گسترهتر از هر عنصر دیگری است. تا بهامروز بیش از ده میلیون ترکیب آلی ثبت شدهاست و مسیر شناسایی ترکیبات جدیدتر همچنان باز است، چرا که این تعداد ترکیب کشف شده تنها بخشی از ترکیبات مجموعه ترکیبات کربنی فرضی ممکن و پایدار در شرایط استاندارد هستند. این همان علتی است که باعث میشود از کربن بهعنوان پادشاه عناصر یاد شود.
تاریخ و نامگذاری

ریشه نام کربن از واژه لاتین carbo به معنای زغالسنگ یا زغال چوب گرفته شدهاست. همچنین در زبان فرانسوی به صورت charbon و به معنی زغال چوب است. در آلمانی، هلندی و دانمارکی نام کربن به ترتیب Kohlenstoff , koolstof و kulstof است که به معنای واقعی کلمه به معنی ماده زغالسنگ هستند.[۱۳]
کشف کربن به دوران پیشاتاریخ بر میگردد و استفاده از آن به صورت دوده و زغال چوب در زندگی اولین تمدنهای بشری مشهور بود. الماس شکل دیگری از کربن احتمالاً در اوایل سال ۲۵۰۰ پیش از میلاد در چین شناخته شده بود و به صورت شیمایی امروزی، در دوران روم باستان از زغال چوب ساخته میشد. همچنین از مخلوط آن با خاک رس در اهرام به منظور پوششی در برابر ورود هوا استفاده میشدهاست.[۱۴][۱۵]

در سال ۱۷۲۲، رنه آنتوان فرشاکو دی رامور نشان داد که آهن با جذب برخی از مواد به فولاد تبدیل میشود، که امروزه به عنوان کربن شناخته شدهاست.[۱۶] در سال ۱۷۷۲، آنتوان لاووازیه، پدر علم شیمی نوین نشان داد که الماسها نوعی کربن هستند. او با سوزاندن ذغال سنگ و الماس دریافت که پس از سوختن هیچکدام آبی تولید نمیکنند و هر دو به مقدار یکسان کربن دیاکسید در هر گرمآزاد میکنند.[۱۷] زمانی که تصور میشد گرافیت شکل دیگری از سرب است، کارل ویلهلم شیله نشان داد که در واقع گرافیت و زغال چوب شکلهای مشابه یکدیگر دارند با مخلوط کوچی از آهن و هنگامی که با نیتریک اسید اکسیده شد آن را "aerial acid" نامید که که نامی برای کربن دیاکسید بود.[۱۸] در سال ۱۷۸۶، دانشمندان فرانسوی، کلود لویی برتوله، گاسپار مونژ و سیای واندرموند با اکسید کردن گرافیت به همان روشی که لاووازیه برای الماس انجام داده بود تأیید کردند که گرافیت بیشتر کربن است.[۱۹] با باقی ماندن مقداری آهن در انتها آنها بر این باور شدند که آهن در ساختار گرافیت لازم است. آنها در نگارشهای خود برای گازی که از سوختن گرافیت خارج میشد نام کاربون (carbone) را پیشنهاد دادند که از واژه لاتین carbonum گرفته شده بود. در سال ۱۷۸۹ لاووازیه در کتابهای درسی از کربن به عنوان یک عنصر نام برد.[۲۰]
در سال ۱۹۸۵ شیمیدانهای آمریکایی رابرت کرل و ریچارد اسمالی و شیمیدان بریتانیایی هارولد کروتو موفق به کشف فولرن، یکی از دگرشکلیهای مصنوعی عنصر کربن شدند[۲۱] که خود انواع گوناگون و متعددی شامل اشکال نانوساختار مانند باکیبالها و نانولولهها است.[۲۲] کاشفان این شکل جدید از کربن در سال ۱۹۹۶ جایزه نوبل شیمی را دریافت کردند.[۲۳] از طرف دیگر علاقه جدید به اشکال جدید منجر به کشف دگرشکلیهای بیشتر از جمله کربن شیشهای، و کربن آمورف شد.[۲۴]
ویژگی

گرافیت که یکی از دگرشکلهای محسوب میشود، یکی از نرمترین مواد شناخته شده و الماس دگرشکل دیگر کربنی، سختترین ترکیب طبیعی شناخته شده بر روی زمین است. کربن میتواند به آسانی با اتمهای کوچک دیگر مانند اتم کربن پیوند برقرار کند و قادر است شکلهای متنوعی از پیوندهای کووالانسی پایدار با اتمهای دارای ظرفیتهای پیوندی مناسب شکل دهد. کربن با داشتن بیش از ده میلیون ترکیب شناخته شده، بیشترین سهم در داشتن ترکیبات مربوط به خود را در بین تمام اتمهای جدول تناوبی دارا است.[۲۵] کربن دارای بالاترین دمای تصعید در میان مام عناصر موجود است. در فشار معمولی اتمسفر، فاقد نقطه ذوب است، چراکه نقطه سهگانه آن در فشار ۰٫۲±۱۰٫۸ مگاپاسکال و دمای ۳۰۰±۴۶۰۰ درجه کلوین (۳۰۰±۴۳۳۰ درجه سانتیگراد؛ ۵۴۰±۷۸۲۰ درجه فارنهایت) بهوقوع میپیوندد[۲][۳] و درنتیجه آن، کربن در دمایی در حدود ۳۹۰۰ درجه کلوین (۳۶۳۰ درجه سانتیگراد؛ ۶۵۶۰ درجه فارنهایت) تصعید میشود.[۲۶][۲۷]
در شرایط استاندارد، گرافیت با اینکه دارای پایداری ترمودینامیکی بالاتری در مقایسه با الماس است، اما نسبت به آن دارای واکنشپذیری بالاتری دارد، چراکه دارای پیوندهای پای نامستقر است و این موجب میشود راحتتر وارد واکنش شیمیایی شود. بهعنوان مثال، در شرایط استاندارد، گرافیت میتواند توسط نیتریک اسید غلیظ و داغ اکسید شود و منجر به تولید ملیتیک اسید شود. در طی چنین تغییری اگرچه واحدهای ششگوشه موجود در ساختار گرافیت حفظ میشود، با اینحال، ساختار و نظم کلی گرافیت شکسته میشود.[۲۸]
کربن در حضور یک قوس کربنی تصعید میشود، جایی که دمای آن به حدود ۵۸۰۰ درجه کلوین (۵۵۳۰ درجه سانتیگراد؛ ۹۹۸۰ درجه فارنهایت) میرسد. صرف نظر از نوع، تمامی دگرشکلهای کربنی در دماهایی حتی بالاتر از دمای ذوب فلزاتی مانند تنگستن و رنیوم، جامد باقی میماند. اگرچه کربن از لحاظ ترمودینامیکی تمایل به اکسید شدن دارد، با این حال در مقابل اکسایش مقاومت میکند و مقاومت آن در برابر اکسایش بسیار موثرتر از مقاومت فلزاتی مانند آهن و مس است. کربن با داشتن عدد اتمی ۶ بهعنوان عنصر ششم محسوب میشود و دارای آرایش الکترونی 1s22s22p2 است که چهار الکترون موجود در اوربیتالهای 2s و 2p بهعنوان الکترونهای ظرفیت آن بهحساب میآیند، الکترونهایی که میتوانند موجب تشکیل پیوند و ساخته شدن پیوندهای بین اتمی و درنتیجه ترکیبات مولکولی جدید شوند. چهار انرژی یونیزاسیون ابتدایی کربن عبارتاند از: ۱۰۸۰٫۵، ۲۳۵۲٫۶، ۴۶۲۰٫۵ و ۶۲۲۲٫۷ کیلوژول برمول که این مقادیر انرژی یونیزاسیون بسیار بیشتر از سایر عناصر موجود در گروه چهاردهم جدول تناوبی (عناصر زیرین در گروه شامل کربن) هستند. میزان الکترونگاتیویته کربن (توضیح: در مقیاس پائولینگ) برابر با ۲٫۵ است که بهطور قابل توجهی از مقدار الکترونگاتیویته سایر عناصر همگروه با کربن (۱٫۸-۱٫۹) در گروه چهاردهم جدول تناوبی بیشتر و تقریبا مشابه با عناصر غیرفلزی مجاور با کربن و فلزات واسطه ردیف دوم و سوم است. شعاع پیوند کووالانسی کربنی معمولا برابر با ۷۷٫۲ پیکومتر برای پیوند کربن-کربن یگانه، ۶۶٫۷ پیکومتر برای پیوند کربن-کربن دوگانه، ۶۰٫۳ پیکومتر برای پیوند کربن-کربن سهگانه است، با اینحال این مقادیر مطلق نیستند و بسته به نوع عدد کوئوردیناسیون و نوع اتصالات دو اتم کربن درگیر در پیوند مورد نظر، متفاوت هستند. بهطور عمومی، شعاع کووالانسی، با کاهش عدد کوئوردیناسیون و افزایش مرتبه پیوند، کاهش مییابد.[۲۹]
ترکیبات کربنی تشکیل دهنده پایه تمامی شکلهای شناخته شده حیات بر روی زمین هستند و چرخه کربن-نیتروژن، با کمک گرفتن از پرتوهای خورشیدی و سایر ستارگان، تامین کننده انرژی لازم برای مصرف موجودات است. اگرچه کربن دارای تعداد بسیار زیاد و متنوع از ترکیبات است، اغلب این ترکیبات در دمای معمولی واکنش ناپذیر هستند. در دما و فشار استاندارد، کربن در مقابل تمامی تغییرات شیمیایی مقاومت میکند با اینحال اکسیدکنندههای قوی میتوانند موجب واکنش پذیری ان شوند. کربن در مقابل سولفوریک اسید، هیدروکلریک اسید، کلر، و تمامی قلیاها، واکنش ناپذیر است. در دماهای بالاتر از دمای استاندارد، کربن با اکسیژن وارد واکنش میشود و منجر به تولید اکسوکربنها میشود و در این شرایط چنانچه در مجاورت اکسیدهای فلزی قرار بگرید، با گرفتن اکسیژن آنها، موجب تبدیل آنها به اکسید فلز به شکل عنصر فلزی میشود. واکنش انجام شده طی واکنش کربن با اکسید فلزی مانند اکسید آهن، یک واکنش گرمازا است و از آن در تولید آهن در صنعت فولاد بهمنظور ذوب کردن آهن و کنترل میزان کربن موجود در فولاد استفاده میشود.
Fe3O4 + 4C(s) → 3Fe(s) + 4CO(g)
کربن مونوکسید میتواند با استفاده از مقدار بیشتری آهن، مورد استفاده قرار بگیرد.
Fe3O4 + 4CO(g) → 3Fe(s) + 4CO2(g)
استفاده از گوگرد، موجب تولید کربن دیسولفید و استفاده از بخار آب، موجب تولید کربن مونوکسید میشود:
C(s) + H2O(g) → CO(g) + H2(g)
کربن در دماهای بالا قابلیت واکنش با برخی از فلزات و تولید کاربید فلزی را دارد. بهعنوان مثال تولید آهن کاربید در فرآیند تولید فولاد و تنگستن کاربید که از آن بهعنوان یک ساینده در ساخت نوک سخت ابزارهای برش استفاده میشود.
دگرشکلهای کربنی طیف وسیعی از خواص فیزیکی و شیمیایی را منجر میشوند که در جدول زیر به برخی از آنها اشاره شده است:
| گرافیت یکی از نرمترین ترکیبات شناخته شده است. | نانوبلور سنتزی الماس، سختترین ترکیب طبیعی شناخته شده است.[۳۰] |
| گرافیت با داشتن خاصیت "ابرروانکنندگی"[c] یک روانکننده خوب است.[۳۱] | الماس بهترین ترکیب موجود برای ساییدن دیگر مواد است. |
| گرافیت هادی جریان الکتریسیته است.[۳۲] | الماس یک عایق عالی برای جریان الکتریسیته است.[۳۳] و دارای بالاترین میزان شکست میدان الکتریکی در میان تمامی مواد شناخته شده است. |
| برخی از انواع گرافیت مناسب برای استفاده بهعنوان عایق حرارتی (عایق آتش و محافظ) هستند در حالیکه برخی دیگر، هدایت کننده بسیار خوب حرارت محسوب میشوند. | الماس بهترین ترکیب طبیعی هادی حرارت است. |
| گرافیت کِدر است. | الماس فوقالعاده شفاف است. |
| گرافیت در شبکه بلوری ششگوشه متبلور میشود..[۳۴] | الماس در شبکه بلوری مکعبی متبلور میشود. |
| کربن بیشکل[d]، کاملا همسانگرد است. | نانولولههای کربنی در میان ناهمسانترین مواد شناخته شده قرار میگیرند. |
دگر شکلها

کربن اتمی دارای عمری کوتاه است که این موضوع موجب میشود شکلهای متنوع مولکولی یا همان دگرشکلهای کربنی شکل بگیرند. سه دگرشکل شناخته شده کربن عبارتاند از کربن بیشکل، گرافیت و الماس. فولرن، دگرشکل بهعنوان دیگر کربن، زمانی گونهای خاص و عجیب بهشمار میآمد، اما امروزه بهصورت متداول تهیه و در تحقیقات علمی مورد استفاده قرار میگیرد. خانواده دگرشکلهای فولرنی خود شامل فولرن باکمینستر[۲۲][۳۵]، نانولوله کربنی[۳۶]، نانوجوانه کربنی[۳۷] و نانوالیاف کربنی[۳۸][۳۹] است. علاوهبر دگرشکلهای مرسوم، چندین نوع دگرشکل غیرمعمول نیز از کربن شناخته شده است که عبارتاند از لونسدالیت[۴۰]، کربن شیشهای[۲۴]، نانوفوم کربنی[۴۱] و کربن استیلنی خطی یا همان کاربین[۴۲].

گرافن یکی دیگر از دگرشکلهای کربنی است که متشکل از ورقهای دوبعدی و ساخته شده از ساختارهای ششگوشه کربنی است. تا سال ۲۰۰۹، گرافن بهعنوان محکمترین ماده بررسی شده بود.[۴۳] فرایند جداسازی گرافن از گرافیت، نیازمند توسعه فناوری به منظور تجاری سازی تولید آن است.[۴۴] چنانچه تولید تجاری گرافن قابل دسترس شود، گرافن میتواند در تولید اهداف متنوعی مورد استفاده قرار بگیرید که آسانسور فضایی و ذخیره ایمن هیدروژن در ماشینهای مبتنی بر موتور هیدروژنی از جمله آنها هستند.[۴۵]
کربن بیشکل، بهعنوان دگرشکلی از کربن، فرمی است که در آن اتمهای کربن در ساختاری غیربلوری، نامنظم و شیشهای مانند قرار گرفتهاند. این نوع کربن بهصورت پودری است و جزء اصلی تشکیل دهنده زغال، کربن سیاه، دوده و کربن فعال است.
در فشار متداول، کربن ساختاری مانند گرافیت را اتخاذ میکند، بهطوری که هر اتم به صورت مثلثی با سهاتم دیگر پیوند برقرار میکند و منجر به تولید یک صفحه مسطح متشکل از واحدهای حلقوی ششگوشه درست همانند هیدروکربنهای آروماتیک میشود.[۴۶] ساختار بهوجود آمده یک شبکه دوبعدی از اتمهای کربن است و این صفحات مسطح کربنی میتوانند با کمک نیروی ضعیف واندروالسی بر روی یکدیگر قرار بگیرند. استحکام پایین پیوند میان این صفحات قرار گرفته بر روی یکدیگر، موجب لغزش آسان صفحات بر روی یکدیگر و نرمی گرافیت میشود. نیروی واندروالسی میان لایهها براثر همپوشانی الکترونهای خارجی اتمهای تشکیل دهنده لایهها است و این همپوشانی منجر به تشکیل یک ابر پای و عدم استقرار الکترونی میشود. وجود ابر ناشی از عدم استقرار الکترونی، باعث میشود که گرافیت بتواند تنها در محل تشکیل پیوندهای نامستقر و در راستای صفحات خود، هادی جریان الکتریکی باشد. این محدودیت سبب میشود که خصلت هدایت الکتریکی توده کربن در مقایسه با اغلب فلزات کمتر باشد. عدم استقرار الکترونی همچنین موجب میشود که گرافیت در مقایسه با الماس، پایداری بیشتری در دمای اتاق داشته باشد.
در فشارهای بالا، کربن دگرشکلهای فشردهتری مانند الماس را تشکیل میدهد که تقریبا دارای چگالی دوبرابر گرافیت است. برخلاف گرافیت، در ساختار الماس، هر اتم به صورت چهاروجهی با چهار اتم دیگر پیوند برقرار میکند و منجر به تشکیل یک شبکه سه بعدی از حلقههای شش عضوی منقبض شده میشود. الماس همانند سیلیسیم و ژرمانیم، دارای ساختار مکعبی است و بهعلت قدرت پیوندهای کربن-کربن، سختترین ماده طبیعی شناخته شده در مقابل خراشیده شدن است. برخلاف باور عمومی که بیان میکند «الماسها تا ابد باقی میمانند»، الماس در شرایط استاندارد (دما: ۲۹۸ کلوین، فشار: ۱۰٬۰۰۰۰ پاسکال[۴۷]) از نظر ترمودینامیکی ناپایدار است (انرژی استاندارد تشکیل گیبس (ΔfG°) برای الماس در دمای ۲۹۸ کلوین = ۲٫۹ کیلوژول بر مول[۴۸]) و در نهایت به گرافیت تبدیل میشود. باتوجه به سد انرژی بالای فعالسازی، تبدیل الماس به گرافیت در دمای اتاق بهقدری آهسته است که قابل تشخیص نیست. باقیمانده کربنی که دچار تغییر فاز شده است بهصورت تجربی مورد بررسی قرار نگرفته است اما مطالعات نظری اخیر با استفاده از روش نظریه تابعی چگالی به این نتیجه رسیده است که در شرایط رسیدن دما و فشار بهترتیب به صفر کلوین و صفر پاسکال، الماس به ساختری با استحکامی در حدود ۱/۱ کیلوژول بر مول بیشتر از گرافیت تبدیل میشود. تحت برخی شرایط، کربن به لونسدالیت متبلور میشود، ساختاری که یک شبکه بلوری ششگوشه است و در آن، همه اتها، همانند آنچه در الماس رخ میدهد، بهصورت کووالانسی با یکدیگر پیوند برقرار میکنند.[۴۰] فولرنها، بلورهایی سنتزی با ساختای مشابه گرافیت هستند با این تفاوت که تمام از واحدهای تشکیل دهنده ششگوشه مسطح ساخته نشدهاند و تعدادی واحد ششگوشه نامسطح، پنچگوشه و حتی هفتگوشه نیز در ساختار آنها وجود دارد. صفحات سازنده فولرنها به صورت کره، بیضی یا استوانهای شکل میگیرند. خواص خانواده ترکیبات فولرنی هنوز بهصورت کامل ارزیابی نشده است و این موضوع خود زمینه وسیعی در تحقیقات نانومواد را به خود اختصاص داده است. فولرن یا نام متداول دیگر آن یعنی باکیبال، برگرفته از نام باکمینستر فولر و مخترع گنبد ژئودزیک است، گنبدی که دارای ساختاری مشابه با فولرنها است. باکیبالها دارای ساختارهای مولکولی بزرگی از کربن هستند که که اتمهای کربن در آنها بهصورت مثلثی با یکدیگر پیوند دادهاند و موجب شکلگیری یک ساختاری کرهگون شدهاند (شناخته شدهترین و سادهترین نوع فولرن، فولرن باکمینستر با ۶۰ اتم کربن است که دارای ساختاری شبیه توپ فوتبال است.)[۲۲]. نانولولههای کربنی (موسوم به باکیتیوب) همانند باکیبالها هستند با این تفاوت که هر اتم کربن در صفحه کربنی ساخته شده بهصورت مثلثی با سه اتم دیگر در پیوند است و موجب ایجاد ساختاری استوانهای شکل و توخالی میشود.[۳۵][۳۶] نانوجوانهها برای اولینبار در سال ۲۰۰۷ گزارش شدند و ترکیبی از باکیبالها و نانولولهها هستند، به این صورت که باکیبالها به صورت کووالانسی به سطح خارجی یک نانولوله متصل شدهاند که این موجب تجمیع خواص این دو گونه در غالب یک ساختار واحد میشود.[۳۷]
از دیگر دگرشکلهای شناخته شده، کربن نانوفوم است که در سال ۱۹۹۷ کشف شد. این دگرشکل متشکل از مجموعه خوشههای دارای چگالی کم از اتمهای کربن است که این اتمهای کربنی به صورت رشته مانند در شبکه سهبعدی ضعیفی نگه داشته شدهاند. در ساختار این کربن نانوفوم، اتمها به صورت مثلثی با یکدیگر در پیوند هستند و منجر به تشکیل حلقههایی شش یا هفت عضوی میشوند. این دگرشکل یکی از سبکترین مواد جامد شناخته شده است بهطوری که تنها دارای یک چگالی ۲ کیلوگرم برای هر متر مکعب است.[۴۹] بهصورت مشابهی با کربن نانوفوم، کربن شیشهای نیز شامل نسبت زیادی فضاهای متخلخل بسته است[۲۴] با این تفاوت که برخلاف ساختار گرافیتی، فاقد ساختاری منظم از صفحات چیده شده بر روی یکدیگر همانند صفحات یک کتاب است و صفحات بهصورت نامنظم و تصادفی بر روی یکدیگر قرار گرفتهاند.

کربن استیلنی خطی که با نام کاربین نیز شناخته میشود، دارای ساختار شیمیایی −n(C:::C)− است[۴۲]. کربن در این نوع دگرشکل، دارای هیبریداسیون از نوع sp است و شکل کلی دگر شکل مانند یک پلیمر است که دارای پیوندهای یگانه و سهگانه بهصورت یکدرمیان است. کاربین توجه زیادی را در نانوفناوری به خود جلب کرده است چراکه دارای مدول یانگ برابر با ۴۰ برابر الماس است.[۵۰] در سال ۲۰۱۵، یک تیم از دانشگاه ایالتی کارولینای شمالی، اعلام کرد که دگرشکل دیگری از از کربن را توسعه دادهاند که نام آن کربن کیو[e] گذاشته شدهاست. این دگرشکل، خواص فرومغناطیس، فلوئورسانس نشان میدهد و سختی آن بیشتر از الماس است.[۵۱]
در فاز بخار، برخی از اتمهای کربن، تشکیل کربن دواتمی میدهند. این گونه در زمان برانگیخته شدن، نور سبز رنگ از خود منتشر میکند.
فراوانی


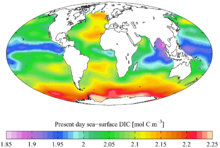
از لحاظ فراوانی جرمی، پس از هیدروژن، هلیم و اکسیژن، کربن چهارمین عنصر در سراسر کیهان است. کربن در خورشید، سایر ستارگان، دنبالهدارها و جو اغلب سیارات، بهوفور یافت میشود.[۵۲] برخی از شهاب سنگها حاوی الماسهای میکروسکوپی هستند که در دوران اولیه تشیکل منظومه شمسی، زمانی که منظومه شمسی تنها یک قرص پیشسیارهای بودهاست، تشکیل شدهاند.[۵۳] الماسهای میکروسکوپی همچنین ممکن است در فشار و دمای بالا در بخشهایی از شهابسنگها که در محل برخورد شهابسنگها قرار دارند، تشکیل شوند.[۵۴]
در سال ۲۰۱۴، ناسا از یک بانک اطلاعاتی بهروز شده گسترده برای دنبال کردن هیدروکربنهای آروماتیک چندحلقهای در کیهان رونمایی کرد. بیش از ۲ درصد کربن موجود در کیهان، ممکن است با هیدروکربنهای آروماتیک چندحلقهای در ارتباط باشد، ترکیبات پیچیدهای متشکل از کربن و هیدروژن، بدون اکسیژن.[۵۵] این ترکیبات اساس "فرضیه دنیای ناشی از هیدروکربنهای آروماتیک چندحلقهای"[f] و پیدایش حیات را بهعهده دارند. این ترکیبات که در حدود چند میلیارد سال پس از مهبانگ تشکیل شدهاند، در سرتاسر کیهان پراکنده شدهاند و با ستارههای جدیدی و سیارات خارج از منظومه شمسی در ارتباط هستند.[۵۲]
تخمین زده میشود که بخش جامد زمین، متشکل از ۷۳۰ قسمت در میلیون[g] کربن است و این مقدار در هسته به ۲۰۰۰ و در بخشهای گوشته و پوسته روی هم به ۱۲۰ قسمت در میلیون میرسد.[۵۶] باتوجه به اینکه جرم زمین برابر ۱۰۲۴×۵٫۹۷۲ کیلوگرم است، بنابراین مقدار کربن را میتوان برابر با ۴۳۶۰ گیگاتن دانست. این مقدار بسیار بیشتر از کربن موجود در اقیانوسها و جو زمین است.
فرم ترکیب شده کربن با اکسیژن، بهشکل کربن دیاکسید، کربن در جو زمین یافت میشود (تقریبا ۹۰۰ گیگاتن کربن، هر قسمت در میلیون معادل ۲/۱۳ گیگاتن است) و بهصورت حل شده در تمامی آب موجود در بدن موجودات (تقریبا ۳۶۰۰۰ گیگاتن کربن). تخمین زده میشود، کربن موجود در زیست کره حدود ۵۵۰ گیگاتن است که البته بهعلت عدم دقت در تعیین میزان باکتریهای موجود در اعماق زمین، میزان عدم قطعیت این تخمین زیاد است.[۵۷] هیدروکربنها (مانند زغالسنگ، نفت خام و گاز طبیعی) نیز بهعنوان منابع حاوی کربن محسوب میشوند. مقدار کربن موجود در ذخایر زغالسنگ برابر با ۹۰۰ گیگاتن است، درحالیکه این مقدار برای منابع زغالسنگ شاید به ۱۸۰۰۰ گیگاتن هم برسد.[۵۸] میزان کربن ذخایر نفت خام نیز به حدود ۱۵۰ گیگاتن میرسد. منابع اثبات شده گاز طبیعی تقریبا برابر با ۱۰۱۲×۱۷۵ متر مکعب است (که میزان کربن آن را حدودا برابر با ۱۰۵ گیگاتن است)، با اینحال مطالعات تخمین میزند که ۱۰۱۲×۹۰۰ متر مکعب گاز دیگر در منابعی مانند گاز شیل وجود دارد که میزان کربن آن را میتوان تا ۵۴۰ گیگاتن محاسبه کرد.[۵۹]
کربن همچنین به صورت آذریخ در مناطق قطبی و در زیر اقیانوس یافت میشود. تخمینهای متفاوتی از میزان کربن مربوط ارائه شدهاست که مقدار آن را ۵۰۰، ۲۵۰۰ یا ۳۰۰۰ گیگاتن اعلام میکنند.[۶۰][۶۱]
در گذشته، مقدار هیدروکربنها بسیار بیشتر بودهاست. برمبنای یک منبع، بین سالهای ۱۷۵۱ تا ۲۰۰۱، حدود ۳۴۷ گیگاتن از کربن موجود، بر اثر سوزاندن سوختهای فسیلی، بهصورت کربن دیاکسید به درون جو زمین رها شدهاست.[۶۲] منبع دیگری بیان میکند که از سال ۱۷۵۰ به بعد، میزان کربن رها شده بهدرون جود زمین برابر با ۸۷۹ گیگاتن و مجموع کربن رها شده بهدرون جو، اقیانوسها و خشکی (مانند خاک باتلاقی) برابر با ۲۰۰۰ گیگاتن بودهاست.[۶۳]
کربن یکی از اجزای اصلی سنگهای کربناتی (مانند سنگ اهک، دولومیت، مرمر) است بهطوری که بهلحاظ جرمی، در مجموع سهمی ۱۲ درصدی دارد. زغالسنگ دارای مقدار بسیار بالایی کربن است (بهعنوان مثال آنتراسیت دارای ۹۲ تا ۹۸ درصد کربن است)[۶۴] و زغالسنگ، با داشتن ۴۰۰۰ گیگاتن کربن و سهمی ۸۰ درصدی از سوختهای فسیلی، بزرگترین منبع تجاری کربن معدنی است.[۶۵]
بهعنوان یکی از دگرشکلهای کربن، گرافیت به مقدار زیادی در مناطقی مانند ایالات متحده آمریکا (غالبا نیویورک و تگزاس)، روسیه، مکزیک، گرینلند و هند یافت میشود. الماس طبیعی در منابعی مانند سنگهای کیمبرلیت موجود در مجرای آتش فشانها یافت میشود. اغلب الماس موجود بر روی زمین در قاره آفریقا و بهویژه در آفریقای جنوبی، نامیبیا، بوتسوانا، جمهوری کنگو و سیرالئون قرار دارد. علاوهبراین منابع الماس در آرکانزاس، کانادا، شمالگان در قسمت روسیه، برزیل و شمال و غرب استرالیا یافت میشود. امروزه همچنین الماس از کف اقیانوس در دماغه امید نیک نیز استخراج میشود. اگرچه الماس بهطور طبیعی نیز یافت میشود، با اینحال حدود ۳۰ درصد تمام الماسهای مورد استفاده در صنعت در ایالات متحده امریکا، بهصورت مصنوعی ساخته میشوند.
کربن-۱۴ در لایه بالای تروپوسفر و استراتوسفر در ارتفاعی بین ۹ تا ۱۵ کیلومتر تولید میشود، جایی که کربن براثر واکنش با پرتوهای کیهانی تهنشین میشود.[۶۶] نوترونهای حرارتی با برخورد با نیتروژن-۱۴ موجب تبدیل آنها به کربن-۱۴ و یک پرتون بهازای هر کربن-۱۴ تولید شده، میشوند. برهمین اساس، ۱۰-۱۰×۱٫۵ درصد از کربن دیاکسید موجود در جو زمین، حای کربن-۱۴ است.[۶۷]
سیارکهای غنی از کربن، نسبت قابل توجهی را در مناطق خارج از کمربند سیارکی در منظومه شمسی به خود اختصاص میدهند. دانشمندان هنوز موق به نمونه برداری مستقیم از این سیارکها نشدهاند. با اینحال این سیارکها میتوانند بهعنوان منابع کربن در فرضیه معادن فضایی استخراج کربن مورد استفاده قرار بگیرند، طرحی که با فناوری امروزی غیرممکن است، اما ممکن است در آینده عملی شود.[۶۸]
ایزوتوپ
ایزوتوپهای کربن در واقع همگی اتمهای کربن دارای شش پرتون هستند و تفاوت آنها در داشتن تعداد متفاوتی از نوترونها است، نوترونهایی که تعدادشان میتواند از ۲ تا ۱۶ متغیر باشد. از میان تمامی ایزوتوپهای کربن، تنها دو مورد، ایزومر طبیعی و پایدار محسوب میشوند که دارای بیشترین میزان فراوانی نیز هستند.[۶۹] از این میان این دو ایزوتوپ، ایزوتوپ کربن-۱۲ حدود ۹۸٫۹۳ درصد از کربن موجود بر روی زمین را تشکیل میدهد و ایزوتوپ کربن-۱۳، سهمی برابر ۱٫۰۷ درصد را دارا است.[۶۹] میزان کربن-۱۲ در ترکیبات زیستی حتی از مقدار ذکر شده نیز بیشتر میشود چراکه در واکنشهای زیستشیمیایی، تمایل زیادی برای کربن-۱۲ نسبت به کربن-۱۳ وجود دارد.[۷۰] در سال ۱۹۶۱، اتحادیهٔ بینالمللی شیمی محض و کاربردی، ایزوتوپ کربن-۱۲ را بهعنوان مبنای تعیین جرم اتمی نسبی عناصر انتخاب کرد.[۷۱] در طیفسنجی رزونانس مغناطیسی هستهای از کربن-۱۳ برای شناسایی ساختمان شیمیایی ترکیبات کربنی استفاده میشود.
کربن-۱۴ دیگر ایزوتوپ کربن است که بهصورت طبیعی یک ایزوتوپ پرتوزا است که توسط واکنش پرتوهای کیهانی با نیتروژن در لایه بالایی جو (در بخشهای پایینی استراتوسفر و بالایی تروپوسفر) ایجاد میشود.[۷۲] این ایزوتوپ در مقادیر بسیار ناچیزی برابر ۱ قسمت در تریلیون[h] (۰٫۰۰۰۰۰۰۰۰۰۱ درصد) بهویژه در جو و انباشتهها سطحی مانند تورب و دیگر مواد آلی یافت میشود.[۷۳] کربن-۱۴ با انتشار پرتوی بتایی با بار منفی و انرژی ۰٫۱۵۸ مگاالکترون ولت فروپاشیده میشود. بهعلت زمان فروپاشی نسبتا آهسته این ایزوتوپ که حدود ۵۷۳۰ سال است، کربن-۱۴ عملا در میان سنگهای قدیمی یافت نمیشود. مقدار این ایزوتوپ در جو زمین و همچنین در بدن موجودات زنده تقریبا ثابت است، اما بهصورت مشخصی بعد از مرگ موجودات زنده، مقدار ان در بدن آنها کاهش مییابد. این کاهش، عملا بهعنوان یک اصل در روش عمرسنجی رادیوکربنی مورد استفاده قرار میگیرد. این روش که در سال ۱۹۴۹ ابداع شده است، بهصورت گستردهای برای تعیین سن مواد کربنی تا عمری در حدود ۴۰۰۰۰ سال، استفاده میشود.[۷۴][۷۵]
بیش از ۱۵ نوع ایزوتوپ کربن شناخته شده وجود دارد که از میان آنها کمترین نیمهعمر به کربن-۸ تعلق دارد، ایزوتوپی که با نشر پروتون و واپاشی آلفا دارای نیمهعمری معادل ۲۱-۱۰×۱٫۹۸۷۳۹ ثانیه دارد.[۷۶] کربن-۱۹ یکی دیگر از ایزوتوپهای غیرعادی کربن است که دارای هاله هستهای[i][توضیح ۱] است. به این معنی که اگر هسته را معادل یک کره دارای چگالی واحد در نظر بگیریم، هسته این ایزوتوپ بزرگتر از حد مورد انتظار است.[۷۷]
شکلگیری در ستارهها
کربن اتمی درون یک ستاره غول یا ابرغول از طریق انجام فرایند آلفا سهگانه رخ میدهد. این مسیر نیازمند برخورد تقریبا همزمان سه ذره آلفا (هسته اتم هلیم) است، چراکه محصول واکنش همجوشی هستهای یک هلیم با هیدروژن و یا اتم هلیم دیگر، بهترتیب لیتیم-۵ و هلیم-۸ خواهند بود که هردو فوق العاده ناپایدار هستند و فورا به گونههای سبکتر فروپاشیده میشوند.[۷۸] فرایند آلفا سهگانه در دمایی بیش از ۱۰۰ مگاکلوین انجام میشود. در نتیجه در دورانهای اولیه تشکیل کیهان که سرعت بالای انبساط و افت دما رخ دادهاست، مقدار قابل توجهی کربن تولید نشدهاست.
بر طبق نظریات فعلی اخترفیزیک، کربن در بخشهای درونی ستارگان در زمانی که آنها در مرحله شاخه افقی قرار دارند، تشکیل میشود.[۷۹] زمانی که ستارگان کلان جرم، با تولید سوپرنوا شروع به نابود شدن میکنند، کربنهای تولید شده مانند غبار به درون فضا پرتاب میشوند. این غبار پراکنده شده، بهعنوان مواد سازنده نسل بعدی ستارگان که اصطلاحا ستارگان فلزینه نامیده میشوند[توضیح ۲] و دارای سیاراتی به دور خود هستند، مورد استفاده قرار میگیرد.[۵۲][۸۰] خورشید واقع در منظومه شمسی یکی از ستارگان این چنینی است که با داشتن مقدار زیاد کربن، وجود حیاتی که امروزه بر روی زمین وجود دارد را ممکن ساختهاست.
چرخه سیاناو، که یک سازوکار همجوشی هیدروژن اضافی است با کمک کربن در نقش کاتالیزور، موجب نیرو بخشیدن به ستارگان میشود.
انتقالات چرخشی گونههای مختلف ایزوتوپی مولکول کربن مونوکسید (برای مثال کربن-۱۲، ۱۳ و ۱۸) توسط اخترشناسی زیرمیلیمتری[j][توضیح ۳] قابل تشخیص هستند و از آنها در مطالعه ستارگان تازه متولد شده و ابرهای مولکولی استفاده میشود.[۸۱]
چرخه کربن
در شرایط متداول بر روی زمین، تبدیل یک عنصر به دیگری، رخدادی بسیار نادر است. بنابراین مقدار کربن موجود بر روی زمین به میزان تقریبا کاملی، ثابت است. از همینرو، فرایندهایی که طی آنها کربن مصرف میشود، بایستی کربن مورد نیاز خود را از یک محل تهیه و کربن پسماند را در محلی دیگر دفع کنند. مسیرهای کربنی موجود در محیط زیست، تشکیل دهنده چرخه کربن هستند. برای مثال گیاهانی که فتوسنتز میکنند، کربن دیاکسید مورد نیاز خود را از هوا (یا آب دریا) دریافت میکنند و سپس آن را به زیستتوده تبدیل میکنند، همانند چرخه کالوین که طی آن کربن تثبیت میشود. برخی از این زیستتوده تولید شده، توسط حیوانات خورده میشود و مقداری دیگر از آن بهصورت کربن دیاکسید توسط حیوانات تنفس میکند. چرخه کربن در عمل، فرایندی پیچیدهتر از توصیفی است که در اینجا به آن اشاره شد. بهعنوان مثال، مقداری از کربن دیاکسیدی که در آب اقیانوسها حل میشود و گیاهان مرده یا مواد جانوری چنانچه توسط باکتریها مصرف نشوند، ممکن است به نفت یا زغالسنگ تبدیل شوند که میتوانند در زمان سوزانده شدن، موجبآزادسازی کربن دیاکسید شوند.[۸۲][۸۳]
مدل اتمی
ساختار الماس (sp3)
ساختار گرافیت (sp2)
پیوند سهگانه (sp1)
ترکیبات
ترکیبات آلی
ترکیبات معدنی
ترکیبات آلی فلزی
محصولات
گرافیت
الماس
الیاف کربن
گرافین
نانولوله کربنی
فولرن
کاربردها
الماس
ایمنی و احتیاط
خواص الکتریکی کربن (رسانا)
کربن به عنوان یک ماده الکتریکی شناخته میشود. کربن میتواند به شکلهای مختلفی باشد: یک رسانای خوب به شکل گرافیت، یکنیمهرسانای خیلی سخت با فاصله زیاد به شکل الماس، یک ابر رسانا هنگامی که با یک جزء مناسب مخلوط شود. به علاوه؛ مواد الکتریکی بر پایه کربن نمونههایی از مواد را عرضه میکنند که مجموعهٔ به هم پیوستهای از ابعاد را نشان میدهند از فلورنها که نقاط ذرهای صفر بعدی هستند، تا نانولولههای کربنی که لولههای کوانتومی ۱ بعدی هستند، تا گرافیت که ماده غیر همسان لایهای ۲ بعدی است و سرانجام تا الماس، یکنیمهرسانا با فاصلهٔ عریض ۳ بعدی.[۸۴]
تولید کربن
کربن در اثر مهبانگ (انفجار بزرگ آغازین) حاصل نشده، چون این عنصر برای تولید نیاز به یک برخورد سه مرحلهای ذرات آلفا (هسته اتم هلیم) دارد. جهان در ابتدا گسترش یافت و چنان به سرعت سرد شد که امکان تولید آن غیرممکن بود. به هر حال، کربن درون ستارگانی که در رده افقی نمودار H-R قرار دارند، یعنی جایی که ستارگان هسته هلیم را با فرایند سهگانه آلفا به کربن تبدیل میکنند، تولید شد.
کاربردها
کربن بخش بسیار مهمی در تمامی موجودات زندهاست و تا آنجا که میدانیم بدون این عنصر زندگی وجود نخواهد داشت (به برتر پنداری کربن مراجعه کنید). عمدهترین کاربرد اقتصادی کربن، فرم هیدروکربنها میباشد که قابل توجهترین آنها سوختهای فسیلی، گاز متان و نفت خام است. نفت خام در صنعت پتروشیمی برای تولید محصولات زیادی از جمله مهمترین آنها بنزین، گازوئیل و نفت سفید بکار میرود که از طریق فرایند تقطیر در پالایشگاهها بدست میآیند. از نفت خام مواد اولیه بسیاری از مواد مصنوعی، که بسیاری از آنها در مجموع پلاستیک نامیده میشوند، شکل میگیرد.
دیگر کاربردها
- ایزوتوپ C-۱۴ که در ۲۷ فوریه ۱۹۳۰ کشف شد در سن یابی کربن پرتوزا مورد استفادهاست.
- گرافیت در ترکیب با خاک رس بهعنوان مغز مداد بکار میرود.
- الماس جهت تزئین ونیز در متهها و سایر کاربردهایی که سختی آن مورد استفادهاست کاربرد د ارد.
- برای تولید آلیاژ فولاد، به آهن کربن اضافه میکنند.
کربن در میله کنترل در واکنشگاههای اتمی بکار میرود.
- گرافیت به شکل پودر و سفت شده بهعنوان زغال چوب برای پخت غذا، در آثار هنری و موارد دیگر مورد استفاده قرار میگیرد.
- قرصهای زغال چوب در پزشکی که به صورت قرص یا پودر وجود دارند برای جذب سم از دستگاه گوارشی مورد استفادهاند.
خصوصیات ساختمانی و شیمیایی فولرن به شکل ریزتیوب کربن، کاربردهای بالقوه امیدوارکنندهای در رشته در حال شکلگیری نانوتکنولوژی دارد.
پیدایش
تقریباً ده میلیون ترکیبات کربنی که برای دانش شناخته شدهاند وجود دارد که هزاران نوع آنها در فرایندهای حیاتی و واکنشهای آلی بسیار مهم اقتصادی، ضروری هستند. این عنصر به مقدار فراوان در خورشید، ستارگان، دنباله دارها و نیز در جو بیشتر سیارات یافت میشود. بعضی از شهابسنگها حاوی الماسهای میکروسکپی هستند که در زمانیکه منظومه شمسی هنوز یک دیسک گازی شکل بود شکل گرفتهاند. کربن به صورت ترکیب با سایر عناصر در جو زمین وجود دارد و در همه گونه آب حل میشود. کربن به همراه مقادیر کمتر کلسیم، منیزیم و آهن، عنصر اصلی سازنده جرم زیادی از سنگ کربنات (سنگ آهک، دولمیت، سنگ مرمر و…) است. این عنصر در صورت ترکیب با هیدروژن تولید زغال سنگ، نفت خام و گاز طبیعی میکند که آنها را هیدرو کربن مینامند. گرافیت به مقدار فراوان در نیویورک و تکزاس، آمریکا، روسیه، مکزیک، گرینلند و هند یافت میشود. الماس طبیعی در کیمبرلیت معدنی موجود درچینهها یا ستونهای سنگهای آذرین یافت میشوند. بیشترین الماس در آفریقا به ویژه آفریقای جنوبی، نامیبیا، بوتسوانا، جمهوری کنگو و سیرالئون وجود دارد. همچنین کانادا، قسمتهای قطبی روسیه، برزیل و بخشهای غربی و شرقی استرالیا دارای الماس میباشد.
ترکیبات غیر آلی
(به شیمی آلی هم مراجعه کنید)
معروفترین اکسید کربن، دیاکسید کربن (CO2) است که به مقدار کمتری در اتمسفر زمین وجود دارد. این اکسید توسط موجودات زنده، و برخی موارد دیگر تولید شده و مورد استفاده قرار میگیرد. آب مقدار کمی اسید کربنیک تولید میکند اما دیاکسید کربن مانند بیشتر ترکیباتی که دارای پیوندهای ساده چندگانه با اکسیژنهای روی یک کربن هستند، ناپایدار است. به هر حال، از طریق این واسطه، یونهای کربنات با تشدید تثبیت شده، بهوجود میآیند. تعدادی از مواد معدنی مهم، کربناتها هستند که معروفترین آنها کلسیت است. دی سولفید کربن، (۲ CS)، هم مانند آن است.
اکسیدهای دیگر آن، مونوکسید کربن (CO) و زیراکسید (suboxide) نادر C3O۲ هستند. مونوکسید کربن که گازی بیرنگ و بیبو است بهوسیله اکسیده شدن ناقص بهوجود میآید. هر یک از این مولکولها دارای یک پیوند سهگانه و نسبتاً قطبی هستند که ناشی از تمایل به یک پیوند دائمی با مولکولهای هموگلوبین میباشد بهطوریکه این گاز بسیار سمی است. سیانید (CN-) دارای ساختار و رفتاری بسیار شبیه به یون هالید بوده و نیترید سیانوژن (CN2) نیز به آن مربوط است.
کربن با فلزات قوی، کاربید C-، یا استیلید C22-؛ بهوجود میآورد که با متان و استیلن همراه بوده و هر دوی آنها اسیدهای بهطور باور نکردنی پائتیک اسید هستند. در کل، کربن با الکترو نگاتیوی ۵/۲ به تشکیل پیوندهای کووالانسی تمایل دارد. تعداد کمی از کاربیدها مثل کربوراندوم و Sic، که شبیه الماس میباشند، به صورت شبکههای کووالانسی هستند.
زنجیرهٔ کربن
در ساختار اتمی هیدروکربنها، گروهی از اتمهای کربن (اشباع شده با اتمهای هیدروژن) تشکیل یک زنجیره میدهند. روغنهای فرار زنجیرههای کوچکتری دارند. چربیها دارای زنجیرههای بلندتر و پارافینها زنجیرههایی بیاندازه بلند دارند.
چرخهٔ کربن
فرایند مداوم ترکیب و آزادسازی کربن و اکسیژن که در آن انرژی و حرارت ذخیره و دفع میشود را چرخه کربن میگویند. فروگشت (کاتابولیسم) + فراگشت (آنابولیسم) = دگرگشت (متابولیسم). (واژهها از فرهنگستان زبان و ادب فارسی). به چرخه کربن مراجعه کنید
هشدارها
ترکیبات کربن گستره وسیعی از آثار سمی دارند. مونوکسید کربن (C O) موجود در اگزوز موتورهای درونسوز و سیانید (CN) که گاهی اوقات در آلودگیهای معدنی وجود دارد برای پستانداران بسیار سمی هستند. بسیاری از ترکیبات دیگر کربن نه تنها سمی نیستند بلکه در واقع برای زیست ضروری میباشند. گازهای آلی مثل اتیلن (H2C=CH2) و اتان و (HCCH)، و متان (CH4) در صورت مخلوط شدن با هوا قابلیت انفجار و اشتعال خطرناکی پیدا میکنند.
برخی از شکل های کربن
توضیحات
- ↑ هسته دارای هاله، به هستهای گفته میشود که توسط ابری هاله مانند از پروتون و یا نوترون احاطه شدهاست و درنتیجه بزرگتر از یک هسته معمولی و فاقد هاله دیده میشود
- ↑ ستارگانی که تناه شامل هیدروژن و هلیم نیستند و شامل عناصر سنگینتر مانند کربن، نیتروژن، اکسیژن و نئون هستند.
- ↑ روش اخترشناسی زیرمیلیمتری که به بررسی میلیمتری و ظریف طیفهای نشری بهدست آمده از مولکولها مینماید موجود در فضای خارجی مینماید.
واژه نامه
جستارهای وابسته
منابع
- ↑ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ↑ ۲٫۰ ۲٫۱ Haaland, D (1976). "Graphite-liquid-vapor triple point pressure and the density of liquid carbon". Carbon. 14 (6): 357–361. doi:10.1016/0008-6223(76)90010-5.
- ↑ ۳٫۰ ۳٫۱ Savvatimskiy, A (2005). "Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)". Carbon. 43 (6): 1115–1142. doi:10.1016/j.carbon.2004.12.027.
- ↑ "Fourier Transform Spectroscopy of the Electronic Transition of the Jet-Cooled CCI Free Radical" (PDF). Retrieved 2007-12-06.
- ↑ "Fourier Transform Spectroscopy of the System of CP" (PDF). Retrieved 2007-12-06.
- ↑ "Carbon: Binary compounds". Retrieved 2007-12-06.
- ↑ ۷٫۰ ۷٫۱ ۷٫۲ ۷٫۳ ۷٫۴ Properties of diamond, Ioffe Institute Database
- ↑ "Material Properties- Misc Materials". www.nde-ed.org. Retrieved 12 November 2016.
- ↑ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ↑ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. pp. E110. ISBN 978-0-8493-0464-4.
- ↑ "History of Carbon and Carbon Materials - Center for Applied Energy Research - University of Kentucky". Caer.uky.edu. Retrieved 2008-09-12.
- ↑ Senese, Fred (2000-09-09). "Who discovered carbon?". Frostburg State University. Retrieved 2007-11-24.
- ↑ Shorter Oxford English Dictionary, Oxford University Press
- ↑ "Chinese made first use of diamond". BBC News. 17 May 2005. Archived from the original on 20 March 2007. Retrieved 2007-03-21.
- ↑ van der Krogt, Peter. "Carbonium/Carbon at Elementymology & Elements Multidict". Archived from the original on 2010-01-23. Retrieved 2010-01-06.
- ↑ Ferchault de Réaumur, R. -A. (1722). L'art de convertir le fer forgé en acier, et l'art d'adoucir le fer fondu, ou de faire des ouvrages de fer fondu aussi finis que le fer forgé (English translation from 1956). Paris, Chicago.
- ↑ "Carbon". Canada Connects. Archived from the original on 2010-10-27. Retrieved 2010-12-07.
- ↑ Senese, Fred. "Who discovered carbon?". Frostburg State University. Archived from the original on 2007-12-07. Retrieved 2007-11-24.
- ↑ Giolitti, Federico (1914). The Cementation of Iron and Steel. McGraw-Hill Book Company, inc.
- ↑ Senese, Fred (2000-09-09). "Who discovered carbon". Frostburg State University. Archived from the original on 2007-12-07. Retrieved 2007-11-24.
- ↑ Kroto, H. W.; Heath, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (1985). "C60: Buckminsterfullerene". Nature. 318 (6042): 162–163. Bibcode:1985Natur.318..162K. doi:10.1038/318162a0.
- ↑ ۲۲٫۰ ۲۲٫۱ ۲۲٫۲ Unwin, Peter. "Fullerenes(An Overview)". Archived from the original on 2007-12-01. Retrieved 2007-12-08.
- ↑ "The Nobel Prize in Chemistry 1996 "for their discovery of fullerenes"". Archived from the original on 2007-10-11. Retrieved 2007-12-21.
- ↑ ۲۴٫۰ ۲۴٫۱ ۲۴٫۲ Harris, PJF (2004). "Fullerene-related structure of commercial glassy carbons" (PDF). Philosophical Magazine. 84 (29): 3159–3167. Bibcode:2004PMag...84.3159H. CiteSeerX 10.1.1.359.5715. doi:10.1080/14786430410001720363. Archived from the original (PDF) on 2012-03-19. Retrieved 2011-07-06.
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامlanlوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Greenville Whittaker, A. (1978). "The controversial carbon solid−liquid−vapour triple point". Nature. 276 (5689): 695–696. Bibcode:1978Natur.276..695W. doi:10.1038/276695a0.
- ↑ Zazula, J. M. (1997). "On Graphite Transformations at High Temperature and Pressure Induced by Absorption of the LHC Beam" (PDF). CERN. Archived (PDF) from the original on 2009-03-25. Retrieved 2009-06-06.
- ↑ Greenwood and Earnshaw, pp. 289–292.
- ↑ Greenwood and Earnshaw, pp. 276–8.
- ↑ Irifune, Tetsuo; Kurio, Ayako; Sakamoto, Shizue; Inoue, Toru; Sumiya, Hitoshi (2003). "Materials: Ultrahard polycrystalline diamond from graphite". Nature. 421 (6923): 599–600. Bibcode:2003Natur.421..599I. doi:10.1038/421599b. PMID 12571587.
- ↑ Dienwiebel, Martin; Verhoeven, Gertjan; Pradeep, Namboodiri; Frenken, Joost; Heimberg, Jennifer; Zandbergen, Henny (2004). "Superlubricity of Graphite" (PDF). Physical Review Letters. 92 (12): 126101. Bibcode:2004PhRvL..92l6101D. doi:10.1103/PhysRevLett.92.126101. PMID 15089689. Archived (PDF) from the original on 2011-09-17.
- ↑ Deprez, N.; McLachan, D. S. (1988). "The analysis of the electrical conductivity of graphite conductivity of graphite powders during compaction". Journal of Physics D: Applied Physics. 21 (1): 101–107. Bibcode:1988JPhD...21..101D. doi:10.1088/0022-3727/21/1/015.
- ↑ Collins, A. T. (1993). "The Optical and Electronic Properties of Semiconducting Diamond". Philosophical Transactions of the Royal Society A. 342 (1664): 233–244. Bibcode:1993RSPTA.342..233C. doi:10.1098/rsta.1993.0017.
- ↑ Delhaes, P. (2001). Graphite and Precursors. CRC Press. ISBN 978-90-5699-228-6.
- ↑ ۳۵٫۰ ۳۵٫۱ Ebbesen, T. W., ed. (1997). Carbon nanotubes—preparation and properties. Boca Raton, Florida: CRC Press. ISBN 978-0-8493-9602-1.
- ↑ ۳۶٫۰ ۳۶٫۱ Dresselhaus, M. S.; Dresselhaus, G.; Avouris, Ph., eds. (2001). Carbon nanotubes: synthesis, structures, properties and applications. Topics in Applied Physics. Vol. 80. Berlin. ISBN 978-3-540-41086-7.
- ↑ ۳۷٫۰ ۳۷٫۱ Nasibulin, Albert G.; Pikhitsa, P. V.; Jiang, H.; Brown, D. P.; Krasheninnikov, A. V.; Anisimov, A. S.; Queipo, P.; Moisala, A.; et al. (2007). "A novel hybrid carbon material". Nature Nanotechnology. 2 (3): 156–161. Bibcode:2007NatNa...2..156N. doi:10.1038/nnano.2007.37. PMID 18654245. S2CID 6447122.
- ↑ Nasibulin, A.; Anisimov, Anton S.; Pikhitsa, Peter V.; Jiang, Hua; Brown, David P.; Choi, Mansoo; Kauppinen, Esko I. (2007). "Investigations of NanoBud formation". Chemical Physics Letters. 446 (1): 109–114. Bibcode:2007CPL...446..109N. doi:10.1016/j.cplett.2007.08.050.
- ↑ Vieira, R; Ledoux, Marc-Jacques; Pham-Huu, Cuong (2004). "Synthesis and characterisation of carbon nanofibers with macroscopic shaping formed by catalytic decomposition of C2H6/H2 over nickel catalyst". Applied Catalysis A: General. 274 (1–2): 1–8. doi:10.1016/j.apcata.2004.04.008.
- ↑ ۴۰٫۰ ۴۰٫۱ Clifford, Frondel; Marvin, Ursula B. (1967). "Lonsdaleite, a new hexagonal polymorph of diamond". Nature. 214 (5088): 587–589. Bibcode:1967Natur.214..587F. doi:10.1038/214587a0.
- ↑ Rode, A. V.; Hyde, S. T.; Gamaly, E. G.; Elliman, R. G.; McKenzie, D. R.; Bulcock, S. (1999). "Structural analysis of a carbon foam formed by high pulse-rate laser ablation". Applied Physics A: Materials Science & Processing. 69 (7): S755–S758. Bibcode:1999ApPhA..69S.755R. doi:10.1007/s003390051522.
- ↑ ۴۲٫۰ ۴۲٫۱ Heimann, Robert Bertram; Evsyukov, Sergey E.; Kavan, Ladislav (28 February 1999). Carbyne and carbynoid structures. Springer. pp. 1–. ISBN 978-0-7923-5323-2. Archived from the original on 23 November 2012. Retrieved 2011-06-06.
{{cite book}}: Unknown parameter|last-author-amp=ignored (|name-list-style=suggested) (help) - ↑ Lee, C.; Wei, X.; Kysar, J. W.; Hone, J. (2008). "Measurement of the Elastic Properties and Intrinsic Strength of Monolayer Graphene". Science. 321 (5887): 385–8. Bibcode:2008Sci...321..385L. doi:10.1126/science.1157996. PMID 18635798. S2CID 206512830. Lay summary.
{{cite journal}}: Cite uses deprecated parameter|lay-url=(help) - ↑ Sanderson, Bill (2008-08-25). "Toughest Stuff Known to Man : Discovery Opens Door to Space Elevator". nypost.com. Archived from the original on 2008-09-06. Retrieved 2008-10-09.
- ↑ Jin, Zhong; Lu, Wei; O’Neill, Kevin J.; Parilla, Philip A.; Simpson, Lin J.; Kittrell, Carter; Tour, James M. (2011-02-22). "Nano-Engineered Spacing in Graphene Sheets for Hydrogen Storage". Chemistry of Materials. 23 (4): 923–925. doi:10.1021/cm1025188. ISSN 0897-4756.
- ↑ Jenkins, Edgar (1973). The polymorphism of elements and compounds. Taylor & Francis. p. 30. ISBN 978-0-423-87500-3. Archived from the original on 2012-11-23. Retrieved 2011-05-01.
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامtherm propوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Rossini, F. D.; Jessup, R. S. (1938). "Heat and Free Energy of Formation of Carbon Dioxide and of the Transition Between Graphite and Diamond". Journal of Research of the National Bureau of Standards. 21 (4): 491. doi:10.6028/jres.021.028.
- ↑ Schewe, Phil; Stein, Ben (March 26, 2004). "Carbon Nanofoam is the World's First Pure Carbon Magnet". Physics News Update. 678 (1). Archived from the original on March 7, 2012.
{{cite journal}}: Unknown parameter|last-author-amp=ignored (|name-list-style=suggested) (help) - ↑ Itzhaki, Lior; Altus, Eli; Basch, Harold; Hoz, Shmaryahu (2005). "Harder than Diamond: Determining the Cross-Sectional Area and Young's Modulus of Molecular Rods". Angew. Chem. Int. Ed. 44 (45): 7432–5. doi:10.1002/anie.200502448. PMID 16240306.
- ↑ "Researchers Find New Phase of Carbon, Make Diamond at Room Temperature". news.ncsu.edu. 2015-11-30. Archived from the original on 2016-04-06. Retrieved 2016-04-06.
- ↑ ۵۲٫۰ ۵۲٫۱ ۵۲٫۲ Hoover, Rachel (21 February 2014). "Need to Track Organic Nano-Particles Across the Universe? NASA's Got an App for That". NASA. Archived from the original on 6 September 2015. Retrieved 2014-02-22.
- ↑ Lauretta, D.S.; McSween, H.Y. (2006). Meteorites and the Early Solar System II. Space science series. University of Arizona Press. p. 199. ISBN 978-0-8165-2562-1. Archived from the original on 2017-11-22. Retrieved 2017-05-07.
- ↑ Mark, Kathleen (1987). Meteorite Craters. University of Arizona Press. ISBN 978-0-8165-0902-7.
- ↑ "Online Database Tracks Organic Nano-Particles Across the Universe". Sci Tech Daily. February 24, 2014. Archived from the original on March 18, 2015. Retrieved 2015-03-10.
- ↑ William F McDonough The composition of the Earth بایگانیشده در ۲۰۱۱-۰۹-۲۸ توسط Wayback Machine in Majewski, Eugeniusz (2000). Earthquake Thermodynamics and Phase Transformation in the Earth's Interior. ISBN 978-0126851854.
- ↑ Yinon Bar-On; et al. (Jun 19, 2018). "The biomass distribution on Earth". PNAS. 115 (25): 6506–6511. doi:10.1073/pnas.1711842115. PMC 6016768. PMID 29784790.
- ↑ Fred Pearce (2014-02-15). "Fire in the hole: After fracking comes coal". New Scientist. 221 (2956): 36–41. Bibcode:2014NewSc.221...36P. doi:10.1016/S0262-4079(14)60331-6. Archived from the original on 2015-03-16.
- ↑ "Wonderfuel: Welcome to the age of unconventional gas" بایگانیشده در ۲۰۱۴-۱۲-۰۹ توسط Wayback Machine by Helen Knight, New Scientist, 12 June 2010, pp. 44–7.
- ↑ Ocean methane stocks 'overstated' بایگانیشده در ۲۰۱۳-۰۴-۲۵ توسط Wayback Machine, BBC, 17 Feb. 2004.
- ↑ "Ice on fire: The next fossil fuel" بایگانیشده در ۲۰۱۵-۰۲-۲۲ توسط Wayback Machine by Fred Pearce, New Scientist, 27 June 2009, pp. 30–33.
- ↑ Calculated from file global.1751_2008.csv in "Index of /ftp/ndp030/CSV-FILES". Archived from the original on 2011-10-22. Retrieved 2011-11-06. from the Carbon Dioxide Information Analysis Center.
- ↑ Rachel Gross (Sep 21, 2013). "Deep, and dank mysterious". New Scientist: 40–43. Archived from the original on 2013-09-21.
- ↑ Stefanenko, R. (1983). Coal Mining Technology: Theory and Practice. Society for Mining Metallurgy. ISBN 978-0-89520-404-2.
- ↑ Kasting, James (1998). "The Carbon Cycle, Climate, and the Long-Term Effects of Fossil Fuel Burning". Consequences: The Nature and Implication of Environmental Change. 4 (1). Archived from the original on 2008-10-24.
- ↑ "Carbon-14 formation". Archived from the original on 1 August 2015. Retrieved 13 October 2014.
- ↑ Aitken, M.J. (1990). Science-based Dating in Archaeology. pp. 56–58. ISBN 978-0-582-49309-4.
- ↑ Nichols, Charles R. "Voltatile Products from Carbonaceous Asteroids" (PDF). UAPress.Arizona.edu. Archived from the original (PDF) on 2 July 2016. Retrieved 12 November 2016.
- ↑ ۶۹٫۰ ۶۹٫۱ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامisotopesوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Gannes, Leonard Z.; Del Rio, Carlos Martı́nez; Koch, Paul (1998). "Natural Abundance Variations in Stable Isotopes and their Potential Uses in Animal Physiological Ecology". Comparative Biochemistry and Physiology – Part A: Molecular & Integrative Physiology. 119 (3): 725–737. doi:10.1016/S1095-6433(98)01016-2. PMID 9683412.
- ↑ "Official SI Unit definitions". Archived from the original on 2007-10-14. Retrieved 2007-12-21.
- ↑ Bowman, S. (1990). Interpreting the past: Radiocarbon dating. British Museum Press. ISBN 978-0-7141-2047-8.
- ↑ Brown, Tom (March 1, 2006). "Carbon Goes Full Circle in the Amazon". Lawrence Livermore National Laboratory. Archived from the original on September 22, 2008. Retrieved 2007-11-25.
- ↑ Libby, W. F. (1952). Radiocarbon dating. Chicago University Press and references therein.
- ↑ Westgren, A. (1960). "The Nobel Prize in Chemistry 1960". Nobel Foundation. Archived from the original on 2007-10-25. Retrieved 2007-11-25.
- ↑ "Use query for carbon-8". barwinski.net. Archived from the original on 2005-02-07. Retrieved 2007-12-21.
- ↑ Watson, A. (1999). "Beaming Into the Dark Corners of the Nuclear Kitchen". Science. 286 (5437): 28–31. doi:10.1126/science.286.5437.28.
- ↑ Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (1997). "The NUBASE evaluation of nuclear and decay properties" (PDF). Nuclear Physics A. 624 (1): 1–124. Bibcode:1997NuPhA.624....1A. doi:10.1016/S0375-9474(97)00482-X. Archived from the original (PDF) on 2008-09-23.
- ↑ Ostlie, Dale A.; Carroll, Bradley W. (2007). An Introduction to Modern Stellar Astrophysics. San Francisco (CA): Addison Wesley. ISBN 978-0-8053-0348-3.
{{cite book}}: Unknown parameter|last-author-amp=ignored (|name-list-style=suggested) (help) - ↑ Whittet, Douglas C. B. (2003). Dust in the Galactic Environment. CRC Press. pp. 45–46. ISBN 978-0-7503-0624-9.
- ↑ Pikelʹner, Solomon Borisovich (1977). Star Formation. Springer. p. 38. ISBN 978-90-277-0796-3. Archived from the original on 2012-11-23. Retrieved 2011-06-06.
- ↑ Falkowski, P.; Scholes, R. J.; Boyle, E.; Canadell, J.; Canfield, D.; Elser, J.; Gruber, N.; Hibbard, K.; et al. (2000). "The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System". Science. 290 (5490): 291–296. Bibcode:2000Sci...290..291F. doi:10.1126/science.290.5490.291. PMID 11030643. S2CID 1779934.
- ↑ Smith, T. M.; Cramer, W. P.; Dixon, R. K.; Leemans, R.; Neilson, R. P.; Solomon, A. M. (1993). "The global terrestrial carbon cycle". Water, Air, & Soil Pollution. 70 (1–4): 19–37. Bibcode:1993WASP...70...19S. doi:10.1007/BF01104986.
- ↑ Ramirez, Arthur P. (2005-11-17). "Carbon nanotubes for science and technology". Bell Labs Technical Journal (به انگلیسی). 10 (3): 171–185. doi:10.1002/bltj.20112. ISSN 1089-7089.
کتابشناسی
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Oxford: Butterworth-Heinemann. ISBN 0080379419.
{{cite book}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link)
پیوند به بیرون
- Carbon on In Our Time at the BBC. (listen now)
- Carbon at The Periodic Table of Videos (University of Nottingham)
- Carbon on Britannica
- Extensive Carbon page at asu.edu
- Electrochemical uses of carbon
- Carbon—Super Stuff. Animation with sound and interactive 3D-models.
| جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||||||||||||||||||||||||||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





