متابولیسم
| بخشی از مجموعه مباحث دربارهٔ |
| بیوشیمی |
|---|
 |
سوختوساز، دِگَرگشت یا مِتابولیسم (به انگلیسی: Metabolism)، مجموعهٔ تغییرهای ترکیبی و تخریبی در موجودات زنده است. دگرگشت مجموعهای از تحولات شیمیایی زندگی پایدار در سلولهای سازوارههای زنده است. آنزیمهایی که واکنشها را کاتالیز میکنند، به سازوارهها (ارگانیسمها) اجازه رشد و تولیدمثل، حفظ ساختار، و پاسخ به محیط خود را میدهند. کلمه دگرگشت به تمام واکنشهای شیمیایی که در ارگانیسم زنده اتفاق میافتد نیز اشاره دارد، از جمله گوارش و انتقال مواد به داخل و بین سلولهای مختلف، که در این صورت مجموعه واکنشهای درون سلولها، دگرگشت واسطهای یا دگرگشت متوسط نامیده میشود.
متابولیسم معمولاً به دو دسته تقسیم میشود. فروگشت (کاتابولیسم) که باعث شکسته شدن مواد و تولید انرژی به وسیله تنفس سلولی میشود، و فراگشت (آنابولیسم) که برای ساخت اجزای سلول از جمله پروتئینها و اسید نوکلئیک از انرژی استفاده میکند.
واکنشهای شیمیایی متابولیسم در چند مسیر سوختوساز سازماندهی میشوند و طی آنها یک ماده شیمیایی توسط دنبالهای از آنزیمها در طول مجموعهای از مرحلهها به ماده شیمیایی دیگر تبدیل میشود. آنزیمها برای متابولیسم ضروری هستند زیرا با اتصال به فرایندهایی که انرژی آزاد میکنند به ارگانیسم اجازه میدهند تا انرژی لازم برای واکنشهای مطلوب را فراهم کنند. آنزیمها بهعنوان کاتالیز باعث میشوند تا واکنشها با سرعت بیشتری عمل کنند. آنزیمها به نظریه کنترل مسیرهای متابولیکی در پاسخ به تغییرات در محیط سلول، یا پیامرسانی سلولی از سلولهای دیگر نیز اجازه میدهند.
سیستم متابولیسم یک ارگانیسم تعیین میکند که کدام ماده سم و کدام ماده برای تغذیه (ماده مغذی) است. به عنوان نمونه، بعضی پروکاریوتها از سولفید هیدروژن به عنوان ماده مغذی استفاده میکنند، در حالی که این گاز برای جانوران سمی است.[۱] سرعت متابولیسم، میزان سوختوساز پایه (BMR)، بر مقدار مواد غذایی لازم برای ارگانیسم و همچنین توانایی آن در بهدستآوردن غذا تأثیر دارد.
یکی از ویژگیهای قابل توجه متابولیسم، شباهت آن به مسیرهای سوختوساز پایه و اجزای بین گونههای بسیار متفاوت است.[۲] به عنوان مثال، مجموعهای از کربوکسیلیک اسیدها که به عنوان حدواسط در چرخه اسید سیتریک شناخته میشوند در تمام موجودات زنده شناختهشده وجود دارند، در گونههایی از باکتری تک سلولی اشریشیا کلی (E. coli) و پرسلولیهای عظیم مثل فیلها یافت میشوند.[۳] این شباهت قابل توجه در مسیرهای سوخت و ساز احتمالاً به دلیل شباهت اولیه آنها در تاریخ فرگشتی حیات و حفظ اثربخشی آن است.[۴][۵]
بهطور خلاصه میتوان گفت: متابولیسم، روندهای شیمیایی هستند که ادامهٔ زندگی را برای سلولها امکانپذیر میسازد.[۶]
واژه شناسی
[ویرایش]متابولیسم فراواژگان آنابولیسم و کاتابولیسم است. در زبان یونانی باستان، άνω به معنای بالا، κάτω به معنای پایین و βολή به معنای رسیدن است. [۷]
زیستشیمی کلیدی
[ویرایش]بیشتر ساختارهایی که جانوران، گیاهان و میکروبها را تشکیل میدهند از سه دسته اساسی مولکولها تشکیل شدهاند: آمینواسیدها، کربوهیدراتها و لیپیدها (اغلب چربیها نامیده میشوند). همانطور که این مولکولها برای زندگی اساسی هستند، واکنشهای متابولیکی روی ساخت این مولکولها در ساخت و ساز یاختهها و بافتها، یا شکستن آنها و استفاده از آنها به عنوان منبع انرژی به وسیله هضم آنها تمرکز دارند. این واکنشها میتوانند برای ساخت چند پلیمر از جمله دیانای و پروتئینها، درشتمولکولهایی که برای زندگی اساسی هستند، به یکدیگر متصل میشوند.
| نوع مولکول | نام شکل تکپار | نام شکل بسپار | نمونههایی از اشکال بسپار |
|---|---|---|---|
| آمینو اسیدها | آمینو اسیدها | پروتئینها (همچنین پلی پپتید نیز نامیده میشوند) | پروتئینهای فیبری و پروتئینهای کروی |
| کربوهیدراتها | تکقندی | چندقندی | نشاسته، گلیکوژن و سلولز |
| اسید نوکلئیک | نوکلئوتید | چند نوکلئوتیدها | دیانای و آرانای |
آمینو اسیدها و پروتئینها
[ویرایش]پروتئینها از اتصال زنجیرهای خطی آمینواسیدها که با پیوند پپتیدی به هم متصل هستند تشکیل شدهاند. بسیاری از پروتئینها آنزیمهایی هستند که کاتالیزگر واکنشهای شیمیایی در متابولیسم میباشند. دیگر پروتئینها عملکرد ساختاری یا مکانیکی دارند، از جمله آنهایی که به شکل اسکلت سلولی، سامانه داربست هستند که شکل سلول را حفظ میکنند.[۸] پروتئینها همچنین در پیامرسانی سلولی، پادتنها، چسبندگی سلولی، انتقال فعال سلولی در سراسر غشا و چرخه سلولی نقش دارند.[۹] آمینو اسیدها نیز با ارائه یک منبع کربن برای چرخه اسید سیتریک (چرخه تریکربوکسیلیک اسید)[۱۰] در متابولیسم انرژی سلولی دخالت دارند، بهویژه زمانی که منبع اولیه انرژی مثل گلوکز کمیاب بوده یا زمانی که سلول تحت تأثیر فشار سوختوساز است.[۱۱]
لیپیدها
[ویرایش]لیپیدها گروهی با بیشترین تنوع زیستشیمیایی هستند. استفاده اساسی آنها در ساختار غشاهای زیستی داخلی و خارجی میباشد، مانند پوسته سلول یا به عنوان منبع انرژی استفاده میشوند.[۹] لیپیدها معمولاً به عنوان ماده آبگریز یا آمفیپاتیک مولکولهای بیولوژیکی تعریف میشوند اما در حلالهای آلی از جمله بنزن و کلروفرم حل میشوند.[۱۲] چربیها گروه بزرگی از ترکیبات هستند که از اسید چرب و گلیسیرول تشکیل شدهاند؛ یک مولکول گلیسرول به سه استر اسید چرب متصل شده و تریگلیسرید نامیده میشود.[۱۳]
کربوهیدراتها
[ویرایش]کربوهیدراتها آلدهیدها یا کتونهایی با اتصال گروه هیدروکسیل هستند که به صورت زنجیرههای مستقیم یا حلقهای وجود دارند. کربوهیدراتها فراوانترین مولکولهای زیستی هستند و نقشهای متعددی از جمله ذخیره و انتقال انرژی (نشاسته، گلیکوژن) و ترکیبات ساختاری (سلولوز در گیاهان، کیتین در جانوران) دارند.[۹] واحد اصلی کربوهیدراتها تکقندیها هستند و شامل گالاکتوز، فروکتوز و از همه مهمتر گلوکز میباشند. تکقندیها با روشهای نامحدودی میتوانند با هم پیوند یافته و چندقندیها را تشکیل دهند.[۱۴]
نوکلئوتیدها
[ویرایش]دو اسیدنوکلوئیک دیانای و آرانای پلیمرهای نوکلئوتیدها هستند، هر نوکلئوتید از یک گروه فسفات متشکل از یک گروه قند ریبوز با یک پایه نیتروژنی تشکیل شدهاست. اسیدهای نوکلئیک برای ذخیرهسازی و استفاده از اطلاعات ژنتیکی مهم هستند و در طول فرایندهای رونویسی و زیستساخت پروتئین بیان میشوند.[۹] این اطلاعات توسط مکانیسمهای بازسازی دیانای محافظت و توسط همانندسازی گسترش مییابند. بیشتر ویروسها ژنوم آرانای دارند، به عنوان مثال اچآیوی، از روش رونویسی معکوس برای تشکیل الگو دیانای از ژنوم آرانای ویروسی استفاده میکند.[۱۵] آرانای در ریبوزیمها به عنوان پیرایشگر بوده و در ریبوزومها مشابه آنزیمهایی هستند که میتوانند واکنشهای شیمیایی را کاتالیز کنند. نوکلئوزیدهای منحصر به فرد توسط اتصال باز نوکلئوتیدی با یک قند ریبوز تشکیل میشوند. این بازهای حلقه هتروسیکلی حاوی نیتروژن، به نام پورینها یا پریمیدینها دستهبندی میشوند. نوکلئوتیدها به عنوان کوآنزیم در واکنشهای انتقال گروه دگرگشتی نیز عمل میکنند.[۱۶]
کوآنزیمها
[ویرایش]سوخت و ساز شامل آرایه وسیعی از واکنشهای شیمیایی است، اما اغلب در چند نوع اساسی از واکنشها که شامل انتقال گروههای عاملی از اتمها و پیوندهای بین آنها در درون مولکولها قرار میگیرند.[۱۷] این شیمی مشترک به سلولها اجازه میدهد تا از مجموعه کوچکی از واسطههای شیمیایی برای حمل گروههای شیمیایی بین واکنشهای مختلف استفاده کنند.[۱۶] این واسطههای انتقال گروهی را کوآنزیم مینامند. هر دسته از واکنشهای انتقال گروهی توسط کوآنزیم مخصوص انجام میشوند، که برای مجموعهای از آنزیمهایی که آنها را تولید کردهاند، و مجموعهای از آنزیمهایی که آنها را مصرف میکنند پیش ماده هستند. این کوآنزیمها بهطور مداوم تولید، مصرف و بازیافت میشوند.[۱۸]
یکی از کوآنزیمهای مرکزی آدنوزین تریفسفات (ATP) میباشد، که انرژی همگانی را در سلولها انتشار میدهد. این نوکلئوتید از انرژی شیمیایی انتقال بین واکنشهای شیمیایی مختلف استفاده میکند. تنها مقدار کمی از ATP در سلولها وجود دارد، اما بهطور مداوم بازسازی میشود، بدن انسان میتواند در حدود وزن خود ATP در روز مصرف کند.[۱۸] ATP به عنوان پلی بین کاتابولیسم و آنابولیسم عمل میکند. کاتابولیسم مولکولها را شکسته و آنابولیسم آنها را به هم متصل میکند. واکنشهای کاتابولیسم ATP را تولید و واکنشهای آنابولیسم آن را مصرف میکنند. این ماده همچنین به عنوان یک حامل از گروههای فسفاتی در واکنشهای فسفرگیری عمل میکند.
مواد معدنی و کوفاکتورها
[ویرایش]عناصر معدنی نقش مهمی را در سوختوساز بازی میکنند؛ بعضیها فراوان هستند (مثل سدیم و پتاسیم) در حالی که بعضی دیگر به صورت غلظت در دقیقه عمل میکنند. حدود ۹۹٪ از جرم پستانداران از عناصر کربن، نیتروژن، کلسیم، سدیم، کلر، پتاسیم، هیدروژن، فسفر، اکسیژن و گوگرد تشکیل شدهاست.[۱۹] ترکیبات آلی (پروتئینها، لیپیدها و کربوهیدراتها) اکثراً از کربن و نیتروژن تشکیل یافتهاند، اکسیژن و هیدروژن در حال حاضر به عنوان آب وجود دارند.[۱۹]
عناصر معدنی به عنوان الکترولیتهای یونی عمل میکنند. مهمترین یونها سدیم، پتاسیم، کلسیم، منیزیم، کلر، فسفات و یون آلی بیکربنات هستند. ابقا دقیق شیب یونی در طول پوسته یاخته، فشار اسمزی و پیاچ را حفظ میکند.[۲۰] همچنین یونها برای عملکرد اعصاب و ماهیچهها مهم هستند. الکترولیتها از طریق پروتئینهای غشا سلولی به نام کانالهای یونی به سلول وارد یا از آن خارج میشوند. به عنوان مثال، انقباض عضله به حرکت کلسیم، سدیم و پتاسیم از طریق کانالهای یونی و لوله تی بستگی دارد.[۲۱]
فلزهای واسطه با روی و آهن که فراوانترین آنها هستند، در حال حاضر به عنوان عنصر ردیابی در ارگانیسمها وجود دارند.[۲۲][۲۳] این فلزات در بعضی از پروتئینها به عنوان کوفاکتور استفاده میشوند و برای فعالیتهای آنزیمها از جمله کاتالاز و پروتئینهای حملکننده اکسیژن مثل هموگلوبین اساسی هستند.[۲۲][۲۳] کوفاکتورهای فلزی با اتصال سختی به بخشهای خاصی از پروتئینها متصل هستند؛ اگرچه کوفاکتورهای آنزیمی میتوانند در طول تجزیه اصلاح شوند، آنها همیشه در پایان واکنش کاتالیز به حالت اولیه خود بازمیگردند.
فروگشت
[ویرایش]در مرحله کاتابولیسم، مولکولهای ترکیب آلی مواد غذایی (کربوهیدراتها، چربیها و پروتئینها) درون یاخته خورد میشوند. مسیرهای فروگشت انرژی آزاد میکنند؛ برخی به صورت ذخیره شده در آدنوزین تریفسفات و برخی به صورت ناقلین الکترون کاهش یافته مانند NADH، NADPH و FADH2 و انرژی باقی مانده به صورت گرما آزاد میشود.
هدف واکنشهای کاتابولیک ارائه انرژی و اجزا مورد نیاز برای واکنشهای آنابولیک است. ماهیت دقیق این واکنشهای کاتابولیک از ارگانیسم به ارگانیسم دیگر متفاوت است و ارگانیسمها میتوانند بر اساس منبع انرژی و کربن دستهبندی شوند (گروههای مواد مغذی اولیه)، همانطور که در جدول زیر نشان داده شدهاست. مولکولهای آلی به عنوان منبع انرژی توسط ارگانوتروفها استفاده میشوند، درحالیکه لیتوتروفها از مواد معدنی استفاده کرده و فتوتروفها نور خورشید را به عنوان انرژی شیمیایی به دام میاندازند. هر چند، تمام روشهای مختلف دگرگشتی به واکنشهای اکسایش-کاهش بستگی دارند که شامل انتقال الکترون از مولکولهای کاهشدهنده مثل ترکیبهای آلی، آب، آمونیاک، سولفید هیدروژن یا یونهای آهنی به مولکولهای پذیرنده مثل اکسیژن، نیترات یا سولفات هستند.[۲۴] در جانوران این واکنشها شامل ترکیبات آلی پیچیده هستند که به مولکولهای سادهتر میشکنند، مثل کربن دیاکسید و آب. در ارگانیسمهای فتوسنتز کننده مثل گیاهان و سیانوباکتریها، این واکنشهای انتقال دهنده الکترون انرژی را آزاد نمیکنند، اما به عنوان یک روش ذخیرهسازی انرژی جذب شده از نور خورشید استفاده میشوند.[۹]
| منبع انرژی | نور خورشید | فوتو- | -تروف | ||
| مولکولهای تشکیل شده از قبل | کمو- | ||||
| دهنده الکترون | ترکیب آلی | ارگانو- | |||
| ترکیب معدنی | لیتو- | ||||
| منبع کربن | ترکیب آلی | هترو- | |||
| ترکیب معدنی | اتو- | ||||
مجموعهای از شایعترین واکنشهای کاتابولیک در جانوران را میتوان به سه مرحله اصلی تقسیم کرد. ابتدا، مولکولهای آلی مثل پروتئینها، پلی ساکاریدها یا لیپیدها در خارج از سلول به قطعات کوچکتر خود تبدیل میشوند. سپس، این قطعات کوچکتر توسط سلول برداشته شده و به قطعات کوچکتر تبدیل میشوند، معمولاً، استیل-کوآ (acetyl-CoA)، و مقداری انرژی آزاد میکنند. در نهایت، گروه استیل موجود در کوآ در چرخه اسید سیتریک و زنجیره انتقال الکترون به آب و کربن دیاکسید، اکسید شده و انرژی ذخیره شده توسط کاهش نیکوتینآمیدآدنیندی نوکلئوتید (NAD+) به NADH.
هضم
[ویرایش]درشت مولکولهایی مثل نشاسته، سلولز یا پروتئینها نمیتوانند به سرعت توسط سلولها گرفته شوند و قبل از اینکه در متابولیسم سلولی مصرف شوند باید به واحدهای کوچکتر شکسته شوند. چندین دسته مشترک از آنزیمها به این پلیمرها هضم میشوند. این آنزیمهای گوارشی از جمله پروتئازها پروتئینها را به آمینواسیدها تجزیه میکنند، همچنین گلیکوزید هیدرولازها که چندقندیها را به قندهای ساده به نام تک قندیها تجزیه میکنند. میکروبها به راحتی آنزیمهای گوارشی را در اطراف خود ترشح میکنند،[۲۵][۲۶] در حالیکه جانوران آنزیمها را از سلولهای مخصوصی در روده خود ترشح میکنند.[۲۷] تک قندیها یا قندهای آزاد شده توسط این آنزیمهای خارج سلولی توسط پروتئینهای انتقال فعال، درون سلولها پمپ میشوند.[۲۸][۲۹]
انرژی به دست آمده از ترکیبات آلی
[ویرایش]کاتابولیسم کربوهیدراتها، کربوهیدراتها را به واحدهای کوچکتر میشکند. کربوهیدراتها معمولاً یک بار توسط سلولها گرفته شده و به تکقندیها هضم میشوند.[۳۰] در داخل، مسیر اصلی شکستن قندکافت است، جایی که قندهایی مثل گلوکز و فروکتوز به پیرووات تبدیل شده و مقداری ATP تولید میشود.[۳۱] پیرووات یک ماده واسطهای در چندین مسیر متابولیکی میباشد، اما اکثر آن به استیل-کوآ تبدیل شده و در چرخه اسید سیتریک تغذیه میشود. اگرچه بیشتر ATP در چرخه اسید سیتریک تولید میشود، مهمترین ماده تولید شده NADH است، که هنگام اکسید شدن استیل-کوآ از NAD+ ساخته میشود. این اکسیداسیون دیاکسید کربن را به عنوان یک ماده زائد تولید میکند. در شرایط بی هوازی، قندکافت اسید لاکتیک|لاکتات تولید میکند. مسیر جایگزین برای شکستن گلوکز، مسیر پنتوز فسفات میباشد، که کوآنزیم NADPH را کاهش میدهد و قندهای پنتوزی مثل ریبوز را تولید میکند، که جزو قندهای اسید نوکلئیک است.
تبدیل انرژی
[ویرایش]فسفرگیری اکسایشی
[ویرایش]در فسفرگیری اکسایشی، الکترونها از مولکولهای آلی موجود در زمینههایی از جمله چرخه پروتوگون اسید برداشته شده و به اکسیژن انتقال یافته و انرژی آزاد شده از آن برای ساختن ATP استفاده میشود. این واکنش در یوکاریوتها توسط مجموعهای از پروتئینهای غشای میتوکندری انجام شده و زنجیره انتقال الکترون نامیده میشود. در پروکاریوتها، این پروتئینها در غشای داخلی سلول وجود دارند.[۳۲] این پروتئینها از انرژی آزاد شده از عبور الکترون از کاهش مولکولهایی نظیر NADH بر روی اکسیژن در پمپ پروتون در سرتاسر غشا استفاده میکنند.[۳۳] پمپهای پروتون خارج میتوکندری واپخش پروتون را در طول غشا ایجاد کرده و یک شیب الکتروشیمیایی را تولید میکنند.[۳۴] این نیرو پروتونها را از طریق آنزیمهایی به نام ایتیپی سنتاز به داخل میتوکندری بازمیگرداند. جریان پروتونها چرخش زیرواحد پایه را ایجاد میکند و باعث فعال شدن دامنه سنتاز به تغییر شکل و فسفرگیری آدنوزین دیفسفات و تبدیل آن به ATP میشود.
انرژی به دست آمده از ترکیبات معدنی
[ویرایش]کمولیتوتروف یک نوع واکنش دگرگشتی است که در پروکاریوتهایی که برای ایجاد انرژی از اکسایش ترکیبات معدنی استفاده میکنند یافت میشود. این ارگانیسمها میتوانند از هیدروژن،[۳۵] کاهش ترکیبات گوگردی (از جمله، سولفید، سولفید هیدروژن و تیوسولفات)، اکسید آهن (II) یا آمونیاک[۳۶] به عنوان منبع کاهش نیرو استفاده کرده و انرژی را از اکسیداسیون این ترکیبات با پذیرندههای الکترون از جمله اکسیژن یا نیترات به دست آورند.[۳۷] این فرایندهای میکروبی در چرخههای بیوژئوشیمی جهانی از جمله آستوژنسیس، نیتریفیکاسیون و دنیتریفیکاسیون مهم بوده و برای حاصلخیزی خاک خطرناک هستند.[۳۸][۳۹]
انرژی به دست آمده از نور خورشید
[ویرایش]انرژی نور خورشید توسط گیاهان، سیانو باکتریها، باکتریهای بنفش، باکتریهای گوگردی سبز و بعضی از آغازیان به دام میافتد. این فرایند اغلب همراه با تبدیل دیاکسید کربن به ترکیبات آلی، به عنوان بخشی از فرایند فتوسنتز میباشد که در ادامه بحث شدهاست. انرژی به دام افتاده و سیستمهای تثبیت کربن میتوانند به صورت جداگانه در پروکاریوتها عمل کنند، به عنوان مثال باکتریهای بنفش و باکتریهای گوگردی سبز میتوانند از انرژی خورشید در هنگام جابهجایی بین تثبیت کربن و تخمیر ترکیبات آلی به عنوان منبع انرژی استفاده کنند.[۴۰][۴۱] در گیاهان، جلبکها و سیانوباکتریها، فتوسیستم II از انرژی نورانی برای جدا کردن الکترون از آب استفاده کرده و اکسیژن را به عنوان یک محصول زائد آزاد میکند. سپس الکترونها به سمت مجموعه سیتوکروم ب۶اف جریان مییابند، که از انرژی آنها برای پمپ پروتونها در سراسر غشای تیلاکوئیدها در کلروپلاستها استفاده میکنند.[۹] این پروتونها با تحریک ATPسنتاز دوباره از غشا به عقب برمیگردند. سپس الکترونها به سمت فتوسیستم I جریان مییابند و میتوانند برای کاهش کوآنزیم NADP+ برای استفاده در چرخه کالوین استفاده شوند که در ادامه بحث خواهد شد یا برای تولید بیشتر ATP بازیافت شوند.[۴۲]
فراگشت
[ویرایش]فراگشت یا آنابولیسم فرایندی سازنده در روند سوختوساز بدن (دگرگشت) است که در آن انرژی صرف میشود تا مواد سادهتر مانند اسید آمینو ترکیب گردد و ترکیبات آلی پیچیدهتر مانند زیمایهها (آنزیمها) و اسیدهای هستهای ساخته شود. فراگشت مجموعهای از فرایندهای سازنده در جایی است که انرژی آزاد شده به وسیله فروگشت برای ساختن مولکولهای پیچیده استفاده میشود. بهطور کلی، مولکولهای پیچیدهای که ساختار سلولی را تشکیل میدهند مرحله به مرحله از پیشسازهای کوچک و ساده ساخته شدهاند. فراگشت شامل سه مرحله اصلی میباشد. اولین مرحله، تولید پیشسازهایی از جمله آمینواسیدها، تکقندیها، ایزوپرنوئیدها و نوکلئوتیدها، دومین مرحله، فعالسازی خود به وسیله واکنشهایی با استفاده از انرژی ATP، و سومین مرحله، گردآوری این پیشسازها و تشکیل مولکولهای پیچیده از جمله، پروتئینها، چندقندیها، لیپیدها و نوکلئیک اسیدها میباشد.
تثبیت کربن
[ویرایش]فتوسنتز، سنتز کربوهیدراتها از نور خورشید و کربن دیاکسید (CO2) میباشد. واکنش تثبیت کربن توسط آنزیم روبیسکو به عنوان بخشی از چرخه کالوین انجام میشود.[۴۳] یک نوع فتوسنتز در گیاهان اتفاق میافتد، تثبیت کربن C3، تثبیت کربن C4 و فتوسنتز CAM. کربن دیاکسید مسیرهای متفاوتی را در چرخه کالوین طی میکند، در مسیر C3 گیاهان CO2 را بهطور مستقیم تثبیت میکنند، درحالیکه در مسیر فتوسنتز C4 و CAM برای سازگاری با نور شدید خورشید و شرایط خشک، ابتدا CO2 را با دیگر مواد ترکیب میکنند.[۴۴] در پروکاریوتهای فتوسنتزی سازوکارهای تثبیت کربن متنوعتر هستند. در اینجا، کربن دیاکسید میتواند توسط چرخه کالوین، چرخه کربس[۴۵] یا کربوکسیلاسیون استیل کوآ تثبیت شود.[۴۶][۴۷]
کربوهیدراتها و گلیکانها
[ویرایش]در فراگشت کربوهیدرات، اسیدهای آلی ساده به تک قندیهایی مثل گلوکز تبدیل شده و سپس به چندقندیهایی مثل نشاسته تبدیل میشوند. تولید گلوکز از ترکیباتی مثل پیرووات، لاکتات، گلیسرول، گلیسرات ۳ فسفات و آمینواسیدها را نوگلوکززایی میگویند. چندقندیها و گلیکانها با اضافه شدن متوالی تکقندیها توسط گلیکوزیل ترنسفراز ساخته میشوند، از واکنش، یک دهنده قند-فسفات مانند اوریدین دیفسفاتگلوکز (UDP-گلوکز) به یک پذیرنده گروه هیدروکسیل چندقندیها گسترش مییابند.
اسیدهای چرب، ایزوپرنوئیدها و استروئیدها
[ویرایش]اسیدهای چرب توسط سنتز اسیدهای چرب ساخته میشوند، با هم ترکیب شده و سپس واحدهای استیل کوآ را کاهش میدهند.
ترپن و ترپنوئیدها گروه بزرگی از لیپیدها شامل کاروتنوئیدها و فرمی از بزرگترین گروه تولیدات طبیعی گیاهان هستند.[۴۸] این ترکیبات با تجمع و اصلاح واحدهای ایزوپرن داده شده از پیشسازهای واکنشهای ایزوپنتنیل پیروفسفات و دیمتیلآلیل پیروفسفات ساخته میشوند.[۴۹] یک واکنش مهم که در دهندههای ایزوپرن فعال استفاده میشود بیوسنتز استروئید میباشد. در اینجا، واحدهای ایزوپرن به یکدیگر متصل شده و اسکوآلن را میسازند و سپس تا خورده و مجموعهای از حلقهها را برای ساختن لانواسترول تشکیل میدهند.[۵۰] لانواسترول میتواند به دیگر استروئیدها از جمله کلسترول و ارگوسترول تبدیل شود.[۵۰][۵۱]
پروتئینها
[ویرایش]اسیدهای آمینه برای ساختن پروتئینها در یک زنجیرهای از پیوندهای پپتیدی به یکدیگر متصل میشوند. هر پروتئین دارای یک توالی خاص از اسید آمینه است. آمینو اسیدها میتوانند در توالیهای مختلفی با هم اتصال پیدا کرده و گروه عظیمی از پروتئینهای مختلف را بسازند. اسیدهای آمینه با پیوند استری توسط مولکول آرانای حامل به هم متصل شده و پروتئینها را تشکیل میدهند.
سنتز نوکلئوتیدها و روش ساخت
[ویرایش]نوکلئوتیدها از آمینواسیدها، دیاکسید کربن و اسید فرمیک در مسیری که نیاز به مقدار زیادی از انرژی دگرگشتی دارد تشکیل میشوند.[۵۲] در نتیجه، بیشتر ارگانیسمها سیستمهای کارآمدی برای مازاد نوکلئوتیدهای تشکیل شده دارند.[۵۲][۵۳] پورینها به عنوان نوکلئوزیدها ساخته میشوند (بازهای متصل شده به ریبوز). آدنین و گوانین از پیشمادههای نوکلئوزیدی اینوزین مونوفسفات تشکیل شدهاند، که آنها نیز از اتمهای آمینواسیدهای گلیسین، گلوتامین و آسپارتیک اسید، همچنین فرمات منتقل شده از کوآنزیم تتراهیدروفولات سنتز شدهاند. از طرف دیگر، پریمیدینها، از باز اوروتات که از گلوتامین و آسپارتات تشکیل شده، ساخته میشوند.[۵۴]
ترمودینامیک موجودات زنده
[ویرایش]سازوارههای زنده باید از قوانین ترمودینامیک پیروی کنند، این قوانین انتقال گرما و کار را توصیف میکند. قانون دوم ترمودینامیک بیان میکند که در هر سامانه بسته، مقدار آنتروپی تمایل به افزایش دارد. اگرچه پیچیدگی شگفتانگیز موجودات زنده متضاد این قانون را نشان میدهد، زندگی زمانی ممکن است که تمام موجودات در یک سامانه باز، ماده و انرژی را با محیط اطراف خود تبادل کنند. از لحاظ ترمودینامیکی، حفظ سوختوساز بدن با ایجاد بی نظمی، تنظیم میشود.
تعریف کالری
[ویرایش]کالری صرفاً روشی برای اندازهگیری انرژی است – انرژی موجود در مواد غذایی و همچنین انرژی آزاد شده در بدن. از لحاظ فنی، ۱ کالری مقدار انرژی لازم برای افزایش حرارت ۱ گرم آب به مقدار ۱ درجهٔ سانتیگراد است. زمانی که آرام مینشینید در هر دقیقه ۱ کالری مصرف میکنید، یعنی مقدار حرارت یکسانی که یک شمع یا لامپ ۷۵ واتی آزاد میکند.[۵۵]
تنظیم و کنترل
[ویرایش]بیشتر سازوارهها در محیطهای زندگی، همواره در حال تغییر هستند، واکنشهای دگرگشتی باید برای مجموعهای از حالتهای درون سلولها به نام هومئوستاز، تنظیم نهایی شوند.[۵۶][۵۷] همچنین تنظیمات متابولیکی به ارگانیسمها اجازه میدهند تا به سیگنالها پاسخ داده و تعامل فعالی با محیط خود داشته باشند.[۵۸] سطوح متعددی از تنظیمات متابولیکی وجود دارند. در تنظیم ذاتی، خودتنظیمی مسیر متابولیکی مسئول تغییرات در سطح لایهها یا تولیدات میباشد. این نوع از تنظیمات اغلب شامل دگرریختاری فعالیتهای آنزیمهای متعدد در مسیر میباشد.[۵۹] کنترل بیرونی شامل یک سلول در سازواره پرسلولی میباشد که دگرگشت خود را در پاسخ به سیگنالهای دیگر سلولها تغییر میدهد. سپس این سیگنالها توسط دومین سیستمهای پیامرسان که اغلب شامل فسفرگیری پروتئینها میباشد به داخل سلول منتقل میشوند.[۶۰]
یک مثال بسیار خوب در کنترل بیرونی تنظیم دگرگشت گلوکز توسط هورمون انسولین میباشد.[۶۱]
تکامل
[ویرایش]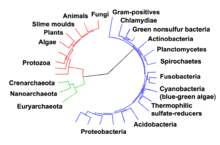
مسیرهای اصلی دگرگشت که در بالا توضیح داده شدند، از جمله گلیکولیز و چرخه اسیدسیتریک، در حال حاضر در تمام سه دامنه موجودات زنده وجود دارند و در آخرین جد جهانی نیز حاضر بودند.[۳][۶۲] این سلولهای اجدادی جهانی، پروکاریوت و احتمالاً متانوژن بودند که متابولیسم گستردهای از آمینواسید، نوکلئوتید، کربوهیدرات و لیپیدها دارند.[۶۳][۶۴] اولین مسیرهای متابولیسم آنزیم-باز ممکن است بخشی از متابولیسم نوکلئوتید پورین باشد، درحالیکه مسیرهای متابولیکی قبلی بخشی از دنیای آرانای اجدادی بودند.[۶۵]
علاوه بر تکامل مسیرهای متابولیکی جدید، تکامل میتواند باعث از دست رفتن عملکردهای متابولیک شود. به عنوان مثال، بعضی انگلها فرایندهای متابولیکی را که برای زنده ماندن اساسی نیستند، از دست داده و آمینواسیدها، نوکلئوتیدها و کربوهیدراتها را به جای بازماندههای میزبان دوباره تشکیل میدهند.[۶۶] کاهش تواناییهای متابولیکی مشابه را میتوان در ارگانیسمهای اندوسیمبیوزیس دید.
تحقیق و دستکاری
[ویرایش]
بهطور کلاسیک، متابولیسم با یک رویکرد تقلیلگرایانه مورد مطالعه قرار میگیرد که تنها بر روی یک روش متابولیکی متمرکز است. ارزشمندترین روش استفاده از ردیاب در تمام ارگانیسم، بافت و لایههای سلولی است که مسیرهای پیشسازها را در تبدیل به محصول نهایی، با واسطه مواد رادیواکتیو نشاندار کرده و محصولات را تعریف میکند.[۶۷] آنزیمهایی که واکنشهای شیمیایی را کاتالیز میکنند سپس میتوانند خالص شده و سینتیک آنها و پاسخ به بازدارندگی آنها مورد بررسی قرار میگیرد. ایده پیچیدگی شبکههای دگرگشتی در سلولها که با هزاران آنزیم مختلف شمرده میشود، در شکل نشان داده شده، تعامل بین فقط ۴۳ پروتئین و ۴۰ متابولیت را نمایش میدهد. این مدلها زمانی که مسیر و اطلاعات متابولیت به دست آمده از روشهای کلاسیک را با اطلاعات بیان ژن از مطالعات پروتئومیک و ریزآرایه دیانای ادغام میکنند، بسیار قدرتمند هستند.[۶۸] استفاده از این تکنیکها، یک مدل از متابولیسم انسانی در حال حاضر تولید شدهاست که کشف داروها و تحقیقات بیوشیمیایی را در آینده هدایت خواهد کرد.[۶۹]
تاریخچه
[ویرایش]اصطلاح متابولیسم از کلمه یونانی Μεταβολισμός مشتق شدهاست – «متابولیسموس» برای «تغییرات»، یا «سرنگونی».[۷۰] در سده سیزدهم یک پزشک مسلمان به نام ابن نفیس دریافت بدن و اجزای آن بهطور مستمر در حال انحلال و تغذیه هستند و به ناچار، دائماً تغییر میکنند.[۷۱] اولین مرجع مستند در مورد دگرگشت توسط ابن نفیس در سال ۱۲۶۰ بعد از میلاد مسیح در مطالعهای با عنوان «الرساله الکاملیه فی السیرة النبویه» نوشته شدهاست. تاریخچه مطالعه دگرگشت در محدوده چندین قرن میباشد و در مطالعات اخیر از آزمایش جانوران به آزمایشهای فردی واکنشهای دگرگشتی در زیستشیمی مدرن حرکت کردهاست. اولین آزمایشهای کنترل شده در دگرگشت انسانی توسط سانتوریو سانتوریو در سال ۱۶۱۴ در کتاب Ars de statica medicina منتشر شدهاست.[۷۲]
در بررسیهای اخیر، سازوکارهای این فرایندهای دگرگشتی مشخص نشدهاست و اعتقاد به اصالت حیات به زندگی بخشیدن به بافتهای زنده معتقد است.[۷۳]
کشف آنزیمها در آغاز سده بیستم توسط ادوارد بوخنر انجام شد که مطالعه واکنشهای شیمیایی دگرگشت را از مطالعه زیستشناختی یاختهها جدا کرده و آغاز زیستشیمی را مشخص کردهاست.[۷۴] یکی از برجستهترین زیستشیمیدانهای نوین هانس آدولف کربس میباشد که کمک بسیار بزرگی در مطالعه دگرگشت انجام دادهاست. او چرخه اوره را کشف کرده و بعدها، با همکاری هانس کورنبرگ، چرخه سیتریک اسید و چرخه گلیاکسیلات را کشف کردهاست.[۷۵][۷۶] تحقیقات مدرن زیستشیمی تا حد زیادی با گسترش روشهایی از جمله کروماتوگرافی (سَوانِگاری)، بلورشناسی پرتو ایکس، طیفسنجی تشدید مغناطیسی هستهای، برچسب ایزوتوپی، میکروسکوپ الکترونی و شبیهسازی دینامیک ملکولی پیشرفت زیادی کردهاست. این روشها کشف و تجزیه و تحلیل دقیق بسیاری از مولکولها و مسیرهای متابولیکی را در سلول امکانپذیر کردهاند.
جستارهای وابسته
[ویرایش]- آنابولیسم (فراگشت)
- کاتابولیسم (فروگشت)
منابع
[ویرایش]این مقاله یک ترجمه از ویکیپدیای انگلیسی است. یادکردها و منابع توسط مترجم بررسی نشدهاست و از مقالهٔ ویکیپدیای انگلیسی کپی شدهاند. شیوهٔ ارجاع این مقاله ارجاع دست دوم است. |
- ↑ Friedrich C (1998). "Physiology and genetics of sulfur-oxidizing bacteria". Adv Microb Physiol. Advances in Microbial Physiology. 39: 235–89. doi:10.1016/S0065-2911(08)60018-1. ISBN 978-0-12-027739-1. PMID 9328649.
- ↑ Pace NR (January 2001). "The universal nature of biochemistry". Proc. Natl. Acad. Sci. U.S.A. 98 (3): 805–8. Bibcode:2001PNAS...98..805P. doi:10.1073/pnas.98.3.805. PMC 33372. PMID 11158550.
- ↑ ۳٫۰ ۳٫۱ Smith E, Morowitz H (2004). "Universality in intermediary metabolism". Proc Natl Acad Sci USA. 101 (36): 13168–73. Bibcode:2004PNAS..10113168S. doi:10.1073/pnas.0404922101. PMC 516543. PMID 15340153.
- ↑ Ebenhöh O, Heinrich R (2001). "Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems". Bull Math Biol. 63 (1): 21–55. doi:10.1006/bulm.2000.0197. PMID 11146883.
- ↑ Meléndez-Hevia E, Waddell T, Cascante M (1996). "The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution". J Mol Evol. 43 (3): 293–303. doi:10.1007/BF02338838. PMID 8703096.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ گایتون، آرتور (۱۳۶۶). فیزیولوژی پزشکی.
- ↑ https://www.etymonline.com/word/metabolism
- ↑ Michie K, Löwe J (2006). "Dynamic filaments of the bacterial cytoskeleton". Annu Rev Biochem. 75: 467–92. doi:10.1146/annurev.biochem.75.103004.142452. PMID 16756499.
- ↑ ۹٫۰ ۹٫۱ ۹٫۲ ۹٫۳ ۹٫۴ ۹٫۵ Nelson, David L.; Michael M. Cox (2005). Lehninger Principles of Biochemistry. New York: W. H. Freeman and company. pp. 841. ISBN 0-7167-4339-6.
- ↑ Kelleher, J,Bryan 3rd, B, Mallet,R, Holleran, A, Murphy, A, and Fiskum, G (1987). "Analysis of tricarboxylic acid-cycle metabolism of hepatoma cells by comparison of 14CO2 ratios". Biochem J. 246 (3): 633–639. PMC 346906. PMID 6752947.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Hothersall, J and Ahmed, A (2013). "Metabolic fate of the increased yeast amino acid uptake subsequent to catabolite derepression". J Amino Acids. 2013: e461901. doi:10.1155/2013/461901. PMC 3575661. PMID 23431419.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E (2005). "A comprehensive classification system for lipids". J Lipid Res. 46 (5): 839–61. doi:10.1194/jlr.E400004-JLR200. PMID 15722563. Archived from the original on 24 August 2010. Retrieved 11 November 2014.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ "Nomenclature of Lipids". IUPAC-IUB Commission on Biochemical Nomenclature (CBN). Retrieved 2007-03-08.
- ↑ Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R (2005). "Glycomics: an integrated systems approach to structure-function relationships of glycans". Nat Methods. 2 (11): 817–24. doi:10.1038/nmeth807. PMID 16278650.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Sierra S, Kupfer B, Kaiser R (2005). "Basics of the virology of HIV-1 and its replication". J Clin Virol. 34 (4): 233–44. doi:10.1016/j.jcv.2005.09.004. PMID 16198625.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ ۱۶٫۰ ۱۶٫۱ Wimmer M, Rose I (1978). "Mechanisms of enzyme-catalyzed group transfer reactions". Annu Rev Biochem. 47: 1031–78. doi:10.1146/annurev.bi.47.070178.005123. PMID 354490.
- ↑ Mitchell P (1979). "The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems". Eur J Biochem. 95 (1): 1–20. doi:10.1111/j.1432-1033.1979.tb12934.x. PMID 378655.
- ↑ ۱۸٫۰ ۱۸٫۱ Dimroth P, von Ballmoos C, Meier T (March 2006). "Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series". EMBO Rep. 7 (3): 276–82. doi:10.1038/sj.embor.7400646. PMC 1456893. PMID 16607397.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ ۱۹٫۰ ۱۹٫۱ Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R (1991). "Chemical and elemental analysis of humans in vivo using improved body composition models". Am J Physiol. 261 (2 Pt 1): E190–8. PMID 1872381.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Sychrová H (2004). "Yeast as a model organism to study transport and homeostasis of alkali metal cations" (PDF). Physiol Res. 53 Suppl 1: S91–8. PMID 15119939.
- ↑ Dulhunty A (2006). "Excitation-contraction coupling from the 1950s into the new millennium". Clin Exp Pharmacol Physiol. 33 (9): 763–72. doi:10.1111/j.1440-1681.2006.04441.x. PMID 16922804.
- ↑ ۲۲٫۰ ۲۲٫۱ Husted S, Mikkelsen B, Jensen J, Nielsen N (2004). "Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics". Anal Bioanal Chem. 378 (1): 171–82. doi:10.1007/s00216-003-2219-0. PMID 14551660.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ ۲۳٫۰ ۲۳٫۱ Mahan D, Shields R (1998). "Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight". J Anim Sci. 76 (2): 506–12. PMID 9498359. Archived from the original on 30 April 2011. Retrieved 11 November 2014.
- ↑ Nealson K, Conrad P (1999). "Life: past, present and future". Philos Trans R Soc Lond B Biol Sci. 354 (1392): 1923–39. doi:10.1098/rstb.1999.0532. PMC 1692713. PMID 10670014.
- ↑ Häse C, Finkelstein R (December 1993). "Bacterial extracellular zinc-containing metalloproteases". Microbiol Rev. 57 (4): 823–37. PMC 372940. PMID 8302217.
- ↑ Gupta R, Gupta N, Rathi P (2004). "Bacterial lipases: an overview of production, purification and biochemical properties". Appl Microbiol Biotechnol. 64 (6): 763–81. doi:10.1007/s00253-004-1568-8. PMID 14966663.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Hoyle T (1997). "The digestive system: linking theory and practice". Br J Nurs. 6 (22): 1285–91. PMID 9470654.
- ↑ Souba W, Pacitti A (1992). "How amino acids get into cells: mechanisms, models, menus, and mediators". JPEN J Parenter Enteral Nutr. 16 (6): 569–78. doi:10.1177/0148607192016006569. PMID 1494216.
- ↑ Barrett M, Walmsley A, Gould G (1999). "Structure and function of facilitative sugar transporters". Curr Opin Cell Biol. 11 (4): 496–502. doi:10.1016/S0955-0674(99)80072-6. PMID 10449337.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Bell G, Burant C, Takeda J, Gould G (1993). "Structure and function of mammalian facilitative sugar transporters". J Biol Chem. 268 (26): 19161–4. PMID 8366068.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Bouché C, Serdy S, Kahn C, Goldfine A (2004). "The cellular fate of glucose and its relevance in type 2 diabetes". Endocr Rev. 25 (5): 807–30. doi:10.1210/er.2003-0026. PMID 15466941. Archived from the original on 4 December 2012. Retrieved 11 November 2014.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Hosler J, Ferguson-Miller S, Mills D (2006). "Energy Transduction: Proton Transfer Through the Respiratory Complexes". Annu Rev Biochem. 75: 165–87. doi:10.1146/annurev.biochem.75.062003.101730. PMC 2659341. PMID 16756489.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Schultz B, Chan S (2001). "Structures and proton-pumping strategies of mitochondrial respiratory enzymes". Annu Rev Biophys Biomol Struct. 30: 23–65. doi:10.1146/annurev.biophys.30.1.23. PMID 11340051.
- ↑ Capaldi R, Aggeler R (2002). "Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor". Trends Biochem Sci. 27 (3): 154–60. doi:10.1016/S0968-0004(01)02051-5. PMID 11893513.
- ↑ Friedrich B, Schwartz E (1993). "Molecular biology of hydrogen utilization in aerobic chemolithotrophs". Annu Rev Microbiol. 47: 351–83. doi:10.1146/annurev.mi.47.100193.002031. PMID 8257102.
- ↑ Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J (1998). "The anaerobic oxidation of ammonium". FEMS Microbiol Rev. 22 (5): 421–37. doi:10.1111/j.1574-6976.1998.tb00379.x. PMID 9990725.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Simon J (2002). "Enzymology and bioenergetics of respiratory nitrite ammonification". FEMS Microbiol Rev. 26 (3): 285–309. doi:10.1111/j.1574-6976.2002.tb00616.x. PMID 12165429.
- ↑ Conrad R (1996). "Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO)". Microbiol Rev. 60 (4): 609–40. PMC 239458. PMID 8987358.
- ↑ Barea J, Pozo M, Azcón R, Azcón-Aguilar C (2005). "Microbial co-operation in the rhizosphere". J Exp Bot. 56 (417): 1761–78. doi:10.1093/jxb/eri197. PMID 15911555.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D (July 2005). "Diel Variations in Carbon Metabolism by Green Nonsulfur-Like Bacteria in Alkaline Siliceous Hot Spring Microbial Mats from Yellowstone National Park". Appl Environ Microbiol. 71 (7): 3978–86. doi:10.1128/AEM.71.7.3978-3986.2005. PMC 1168979. PMID 16000812.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Tichi M, Tabita F (2001). "Interactive Control of Rhodobacter capsulatus Redox-Balancing Systems during Phototrophic Metabolism". J Bacteriol. 183 (21): 6344–54. doi:10.1128/JB.183.21.6344-6354.2001. PMC 100130. PMID 11591679.
- ↑ Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T (2004). "Cyclic electron flow around photosystem I is essential for photosynthesis". Nature. 429 (6991): 579–82. Bibcode:2004Natur.429..579M. doi:10.1038/nature02598. PMID 15175756.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Miziorko H, Lorimer G (1983). "Ribulose-1,5-bisphosphate carboxylase-oxygenase". Annu Rev Biochem. 52: 507–35. doi:10.1146/annurev.bi.52.070183.002451. PMID 6351728.
- ↑ Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K (2002). "Crassulacean acid metabolism: plastic, fantastic". J Exp Bot. 53 (369): 569–80. doi:10.1093/jexbot/53.369.569. PMID 11886877.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Hügler M, Wirsen C, Fuchs G, Taylor C, Sievert S (May 2005). "Evidence for Autotrophic CO2 Fixation via the Reductive Tricarboxylic Acid Cycle by Members of the ɛ Subdivision of Proteobacteria". J Bacteriol. 187 (9): 3020–7. doi:10.1128/JB.187.9.3020-3027.2005. PMC 1082812. PMID 15838028.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Strauss G, Fuchs G (1993). "Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle". Eur J Biochem. 215 (3): 633–43. doi:10.1111/j.1432-1033.1993.tb18074.x. PMID 8354269.
- ↑ Wood H (1991). "Life with CO or CO2 and H2 as a source of carbon and energy". FASEB J. 5 (2): 156–63. PMID 1900793.
- ↑ Dubey V, Bhalla R, Luthra R (2003). "An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants" (PDF). J Biosci. 28 (5): 637–46. doi:10.1007/BF02703339. PMID 14517367.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Kuzuyama T, Seto H (2003). "Diversity of the biosynthesis of the isoprene units". Nat Prod Rep. 20 (2): 171–83. doi:10.1039/b109860h. PMID 12735695.
- ↑ ۵۰٫۰ ۵۰٫۱ Schroepfer G (1981). "Sterol biosynthesis". Annu Rev Biochem. 50: 585–621. doi:10.1146/annurev.bi.50.070181.003101. PMID 7023367.
- ↑ Lees N, Skaggs B, Kirsch D, Bard M (1995). "Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review". Lipids. 30 (3): 221–6. doi:10.1007/BF02537824. PMID 7791529.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ ۵۲٫۰ ۵۲٫۱ Rudolph F (1994). "The biochemistry and physiology of nucleotides". J Nutr. 124 (1 Suppl): 124S–127S. PMID 8283301. Zrenner R, Stitt M, Sonnewald U, Boldt R (2006). "Pyrimidine and purine biosynthesis and degradation in plants". Annu Rev Plant Biol. 57: 805–36. doi:10.1146/annurev.arplant.57.032905.105421. PMID 16669783.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Stasolla C, Katahira R, Thorpe T, Ashihara H (2003). "Purine and pyrimidine nucleotide metabolism in higher plants". J Plant Physiol. 160 (11): 1271–95. doi:10.1078/0176-1617-01169. PMID 14658380.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Smith J (1995). "Enzymes of nucleotide synthesis". Curr Opin Struct Biol. 5 (6): 752–7. doi:10.1016/0959-440X(95)80007-7. PMID 8749362.
- ↑ «مبانی کالری - ویتامینو | vitamino». ۲۰۱۸-۱۰-۲۸. بایگانیشده از اصلی در ۲ دسامبر ۲۰۱۸. دریافتشده در ۲۰۱۸-۱۲-۰۱. بیش از یک پارامتر
|پیوند بایگانی=و|archiveurl=دادهشده است (کمک); بیش از یک پارامتر|تاریخ بایگانی=و|archivedate=دادهشده است (کمک) - ↑ Albert R (2005). "Scale-free networks in cell biology". J Cell Sci. 118 (Pt 21): 4947–57. doi:10.1242/jcs.02714. PMID 16254242.
- ↑ Brand M (1997). "Regulation analysis of energy metabolism". J Exp Biol. 200 (Pt 2): 193–202. PMID 9050227.
- ↑ Soyer O, Salathé M, Bonhoeffer S (2006). "Signal transduction networks: topology, response and biochemical processes". J Theor Biol. 238 (2): 416–25. doi:10.1016/j.jtbi.2005.05.030. PMID 16045939.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Fell D, Thomas S (1995). "Physiological control of metabolic flux: the requirement for multisite modulation". Biochem J. 311 (Pt 1): 35–9. PMC 1136115. PMID 7575476.
- ↑ Cohen P (2000). "The regulation of protein function by multisite phosphorylation—a 25 year update". Trends Biochem Sci. 25 (12): 596–601. doi:10.1016/S0968-0004(00)01712-6. PMID 11116185.
- ↑ Lienhard G, Slot J, James D, Mueckler M (1992). "How cells absorb glucose". Sci Am. 266 (1): 86–91. doi:10.1038/scientificamerican0192-86. PMID 1734513.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Romano A, Conway T (1996). "Evolution of carbohydrate metabolic pathways". Res Microbiol. 147 (6–7): 448–55. doi:10.1016/0923-2508(96)83998-2. PMID 9084754.
- ↑ Koch A (1998). "How did bacteria come to be?". Adv Microb Physiol. Advances in Microbial Physiology. 40: 353–99. doi:10.1016/S0065-2911(08)60135-6. ISBN 978-0-12-027740-7. PMID 9889982.
- ↑ Ouzounis C, Kyrpides N (1996). "The emergence of major cellular processes in evolution". FEBS Lett. 390 (2): 119–23. doi:10.1016/0014-5793(96)00631-X. PMID 8706840.
- ↑ Caetano-Anolles G, Kim HS, Mittenthal JE (2007). "The origin of modern metabolic networks inferred from phylogenomic analysis of protein architecture". Proc Natl Acad Sci USA. 104 (22): 9358–63. Bibcode:2007PNAS..104.9358C. doi:10.1073/pnas.0701214104. PMC 1890499. PMID 17517598.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Lawrence J (2005). "Common themes in the genome strategies of pathogens". Curr Opin Genet Dev. 15 (6): 584–8. doi:10.1016/j.gde.2005.09.007. PMID 16188434. Wernegreen J (2005). "For better or worse: genomic consequences of intracellular mutualism and parasitism". Curr Opin Genet Dev. 15 (6): 572–83. doi:10.1016/j.gde.2005.09.013. PMID 16230003.
- ↑ Rennie M (1999). "An introduction to the use of tracers in nutrition and metabolism". Proc Nutr Soc. 58 (4): 935–44. doi:10.1017/S002966519900124X. PMID 10817161.
- ↑ Gianchandani E, Brautigan D, Papin J (2006). "Systems analyses characterize integrated functions of biochemical networks". Trends Biochem Sci. 31 (5): 284–91. doi:10.1016/j.tibs.2006.03.007. PMID 16616498.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Duarte NC, Becker SA, Jamshidi N; et al. (February 2007). "Global reconstruction of the human metabolic network based on genomic and bibliomic data". Proc. Natl. Acad. Sci. U.S.A. 104 (6): 1777–82. Bibcode:2007PNAS..104.1777D. doi:10.1073/pnas.0610772104. PMC 1794290. PMID 17267599.
{{cite journal}}: Explicit use of et al. in:|author=(help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ "Metabolism". The Online Etymology Dictionary. Retrieved 2007-02-20.
- ↑ "پشت پرده مفهوم متابولیسم". 2017. خبرگزاری جمهوری اسلامی. Accessed November 23 2017. [۱].
- ↑ Eknoyan G (1999). "Santorio Sanctorius (1561–1636) – founding father of metabolic balance studies". Am J Nephrol. 19 (2): 226–33. doi:10.1159/000013455. PMID 10213823.
- ↑ Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York) Retrieved on 2007-03-26
- ↑ Eduard Buchner's 1907 Nobel lecture at http://nobelprize.org Accessed 2007-03-20
- ↑ Krebs HA, Henseleit K (1932). "Untersuchungen über die Harnstoffbildung im tierkorper". Z. Physiol. Chem. 210: 33–66. doi:10.1515/bchm2.1932.210.1-2.33.
Krebs H, Johnson W (April 1937). "Metabolism of ketonic acids in animal tissues". Biochem J. 31 (4): 645–60. PMC 1266984. PMID 16746382. - ↑ Kornberg H, Krebs H (1957). "Synthesis of cell constituents from C2-units by a modified tricarboxylic acid cycle". Nature. 179 (4568): 988–91. Bibcode:1957Natur.179..988K. doi:10.1038/179988a0. PMID 13430766.


