الکل: تفاوت میان نسخهها
جز ویرایش 158.58.108.245 (بحث) به آخرین تغییری که Dexbot انجام داده بود واگردانده شد |
برچسبها: ویرایش همراه ویرایش از برنامهٔ همراه |
||
| خط ۸: | خط ۸: | ||
== تاریخچه == |
== تاریخچه == |
||
الکل را |
الکل را محمد امین یوسفی زاده پزشک ایرانی کشف کرد{{نیازمند منبع}} |
||
== ساختار و دستهبندی == |
== ساختار و دستهبندی == |
||
نسخهٔ ۲۷ نوامبر ۲۰۱۶، ساعت ۱۹:۳۵

در شیمی به هر ترکیب شیمیایی که یک گروهِ هیدرکسیل (-OH) متصل به کربن یک آلکیل داشتهباشد، الکل گویند. فرمول کلی یک الکل سادهٔ غیر حلقهای CnH2n+1OH است. در شیمی الکلها در شمار گروه مهمی از ترکیبهای شیمیایی هستند و در واکنشهای گستردهای شرکت میکنند و بسیاری از ترکیبهای شیمیایی از آنها به دست میآیند، به طوری در کتاب شیمی آلی موریسن و بوید آمدهاست که اگر به شیمیدانی بگویند او را با ده ترکیب شیمیایی دریک جزیره تنها خواهند گذاشت الکل یکی از آنها خواهدبود.
به طور کلی، زمانی که نام الکل به تنهایی به کار میرود، معمولاً منظور اتانول است که همان الکل گرفتهشده از جو یا عرق یا همان مشروبات الکلی میباشد. اتانول مایعی بیرنگ و فرار وبا بویی بسیار تند است که از تخمیر شکرها به دست میآید. همچنین گاه به هر گونه نوشیدنی که الکل داشتهباشد، الکل میگویند. هزاران سال است که معمولاً الکل به عنوان یکی از عاملهای اعتیادآور به شمار میآید.
الکلهای دیگر بیشتر با صفتهای مشخصکنندهٔ ویژهٔ خود میآیند مانند الکل چوب (که همان متانول است) یا ایزوپروپیل الکل. پسوند «ول» نیز در پایان نام شیمیایی همهٔ الکلها میآید.
تاریخچه
الکل را محمد امین یوسفی زاده پزشک ایرانی کشف کرد[نیازمند منبع]
ساختار و دستهبندی
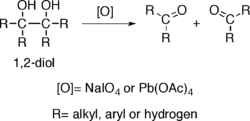
الکلها بسته به نوع کربن[۱] که به گروه OH- پیوند دارد، به سه دسته نوع اول، نوع دوم یا نوع سوم طبقهبندی میشوند:
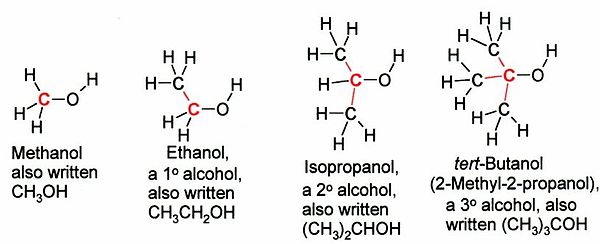
نمایش کلی انواع الکل
- الکل نوع اول CR(H)۲-OH.
- الکل نوع دوم C(R)۲H-OH.
- الکل نوع سومC(R)۳-OH.
خواص فیزیکی الکلها
دمای جوش
الکلها در میان هیدروکربنهای هم وزن خود دمای جوش بالاتری دارند که آن را میتوان به پیوند هیدروژنی الکلها دانست
حلالیت
با توجه به این که پیوند بین الکلها مانند آب، پیوند هیدروژنی است به هر اندازهای در آب حل میشود. همچنین با توجه به این که الکلها از یک سو بخشی آلی داشته و از سوی دیگر گروه هیدروکسید دارند بسیاری از مواد آلی را نیز حل میکنند.
محلول ید در محلول آب و الکل را تنتورید میگویند و برای گندزدایی به کار میروند.
سمشناسی
الکلها بیشتر بویی تند و زننده دارند و اتانول از دوران پیش از تاریخ به دلیلهای گوناگون بهداشتی، رژیمی، مذهبی و تفریحی به عنوان نوشیدنی الکلی به کار میرفتهاست. هرچند استفادهٔ کم و گهگاه الکل میتواند بیزیان باشد، اندازههای بیشتر آن سبب مستی شده و در مقدارهای بیشتر میتواند به اختلالات تنفسی و حتی مرگ نیز بینجامد.[۱]
الکلهای دیگر سمیتر از اتانول هستند، که این نیز بیشتر به دلیل نیاز به زمان بیشتر برای تغییر در فرایند سوخت و ساز است و حتی گاه در فرایندهای دگرگشت (متابولیسم) مادههایی سمی میسازند. برای نمونه متانول، که همان الکل چوب است، به وسیلهٔ آنزیمها در جگر اکسایش مییابد و مادهٔ سمی فرمالدهید تولید میکند که میتواند سبب کوری یا مرگ شود.
یکی از راههای کارا در پیشگیری از سمیت فرمالدهید، فراهم آوردن اتانول در کنار آن است چون آنزیمهای هیدروژنزدایی که از متانول فرمالدهید میدهند بر اتانول اثر بیشتری دارند، بدین گونه از پیوند و عمل بر روی متانول پیشگیری میکند. در این زمان متانول باقیمانده وقت دفع از راه کلیهها را پیدا کرده و فرمالدهید باقیمانده نیز به فرمیک اسید تبدیل میشود.
نامگذاری
در نامگذاری الکلها به روش آیوپاک، تنها در آخر نام آلکان یک «ول» افزوده میشود و زمانی که نیاز ذکر شمارهٔ کربنی که عامل الکلی بر روی آن قرار دارد باشیم، عدد بین نام آلکان و پسوند «ول» قرار میگیرد. مانند «پروپان-۱-ول» برای CH3CH2CH2OH و «پروپان-۲-ول» برای CH3CH(OH)CH3.

روشهای فرآوری صنعتی الکلها
از میان روشهای صنعتی الکل میتوان راههای زیر را نام برد:
- آبدارکردن آلکنهای بدست آمده از کراکینگ نفت.
- فرایند السک از آلکنها، مونوکسید کربن و هیدروژن.
- تخمیر کربوهیدراتها.
علاوه بر این سه روش اصلی، روشهای دیگری نیز با کاربرد محدود وجود دارند. بهعنوان مثال، متانول از هیدروژندار کردن کاتالیزوری مونوکسید کربن بدست میآید. مخلوط هیدروژن و مونوکسید کربن با نسبت ضروری، از واکنش آب با متان، آلکانهای دیگر، یا زغال سنگ در دمای بالا بدست میآید.
کاربردها
برخی از کاربردهای الکل:
- سوخت خودرو
- حلال
- کاربردهای پزشکی و گندزدایی (به دلیل نفوذ فوقالعاده به داخل منافذ و حفرهها و از بین بری باکتریهای گرم مثبت و منفی و باکتریهای مقاوم به اسید با غلظت ۷۰ تا ۸۰ درصد)
- ...
واکنشها
پروتونزدایی
الکلها میتوانند در حضور بازهای بسیار قوی به سان یک اسید عمل کنند و تشکیل یون الکوکسی دهند. برای نمونه در واکنش سدیم هیدروکسید و اتانول، سدیم جانشین هیدروژنِ مثبت (پروتون) الکل شده و سدیم متوکسی به دست میدهد.
هیدروژنزدایی
از راه هیدروژنزدایی الکلها میتوان اتر به دست آورد.
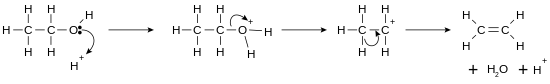
واکنشهای هستهدوستی
گروه هیدروکسیل الکل یک گروه ترککنندهٔ خوب است و سبب میشود که الکلها بتوانند در واکنشهای هستهدوستی شرکت جویند.
استری شدن
الکل با اسیدهای آلی در محیط اسیدی به آهستگی تشکیل استر میدهد. مفهوم استری شدن (Esterification) واکنش یک الکل با اسید کربوکسیلیک (اسید آلی) را که منجر به تولید ترکیبی به نام استر میشود، استری شدن مینامند. واکنش استری شدن، واکنشی است تعادلی که در حضور مقادیر کم اسیدهای معدنی انجام میشود و با تولید آب همراه است. خواص استرها استرها ترکیبهایی با فرمول کلیR-CO-OR میباشند. استر، بمعنی اتر اسید است که گاهی به جای آن واژه اتوسل بمعنی نمک فرار را بکار میبرند. استرها غالباً فرار و معطرند وبوی خوشایند بسیاری از گلها و میوهها، بعلت وجود استر در آنهاست. مثلاً استات ایزوپنتیل، بوی موز و والرات ایزوپنتیل، بوی سیب دارد. بوی بد کره فاسد (کره ترش شده) بعلت وجود اسیدبوتیریک در آن است. از واکنش این اسید با اتیل الکل، استر بوتانات اتیل بدست میآید که دارای مزه و طعم خوشایند آناناس است.
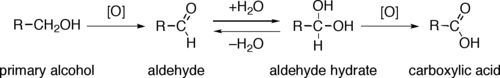
اکسایش
الکلهای نوع اول میتوانند در واکنشهای اکسایش تبدیل به آلدهید و پس از آن تبدیل به کربوکسیلیک اسید شوند هرچند که الکلهای نوع دوم در واکنشهای اکسایش تنها تبدیل به کتون میشوند ولی الکلهای نوع سوم در واکنشهای اکسایش شرکت نمیکنند.
الکلهای نوع اول میتوانند بدون واسطه نیز به روشهای زیر به کربوکسیلیک اسیدها تبدیل شوند:
- با حضور پتاسیم پرمنگنات (KMnO4).
- PDC در DMF.
- اکسایش جونز
- اکسایش هنس
- روتنیوم تتراکسید (RuO4).
یک الکل با دو عامل مجاور میتواند در مجاورت سدیم پراکسید(NaIOsub>4) یا سرب تترااستات (Pb(OAc)4) پیوند کربنش گسستهشده و به دو کربوکسیلیک اسید تبدیل شود.
الکلها و فنولها
اگر گروه هیدروکسیل الکل به کربنی که روی یک حلقهٔ آروماتیک است، متصل باشد آنگاه به آن فنول گویند که در دستهٔ دیگری از ترکیبها دستهبندی میشود و ویژگیهای متفاوتی از الکلها دارد.
جستارهای وابسته
منابع
- ↑ به کربنی که به کربن دیگر متصل نباشد، کربن نوع صفرم و به کربنی که تنها به یک کربن دیگر متصل باشد، کربن نوع اول میگویند. کربن نوع دوم و نوع سوم نیز بر همین اساس نامگذاری میشود.
- موریسن، و بوید (۱۳۷۵)، شیمی آلی، ترجمهٔ سید احمد شکرایی و عیسی یاوری، تهران: مرکز نشر دانشگاهی، شابک ISBN ۹۶۴-۰۱-۰۷۷۸-۶ مقدار
|شابک=را بررسی کنید: invalid character (کمک) پارامتر|چاپ=اضافه است (کمک); تاریخ وارد شده در|سال=را بررسی کنید (کمک) - ویکیپدیای انگلیسی