واکنش حذفی
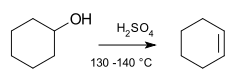
واکنش حذفی (به انگلیسی: elimination reaction) گونهای واکنش آلی است که در آن دو جانشین در یک فرایند یک یا دو گامی، از یک مولکول حذف میشود.[۲] فرایند یک گامی (یک مرحلهای) را واکنش E2 و فرایند دو گامی را واکنش E1 مینامند. این عددها لزوماً ربطی بهشمار گامها در فرایند ندارد بلکه سینتیک واکنشهای به ترتیب دومولکولی و تکمولکولی در اینجا مطرح است.
ذر بیشتر واکنشهای حذفی دست کم یک هیدروژن از دست میرود تا یک پیوند دوگانه ساخته شود: غیراشباعی مولکول افزایش مییابد. همچنین ممکن است یک مولکول دچار واکنش حذفی کاهش دهنده شود به این معنی که والانس یک اتم در مولکول دو تا کاهش مییابد. دستهای از واکنشهای حذفی که از اهمیت ویژهای برخوردارند، واکنشهایی است که در آن هالیدهای آلکیل با گروه ترککننده خوبی درگیر میشود و پس از واکنش با یک باز لوئیس یک آلکن میسازد. گاهی واکنش حذفی در برابر واکنش افزایشی دانسته میشود.
سازوکار E2[ویرایش]
در بازهٔ دههٔ ۱۹۲۰ سر کریستوفر اینگلد مدلی برای توضیح یک گونهٔ ویژه از واکنشهای شیمیایی پیشنهاد کرد؛ این پیشنهاد همان سازوکار E2 بود. E2 در واقع برابر با حذف دومولکولی است. نکات پایهای این واکنش عبارتند از:
- سازوکار تک-گامی که در آن پیوندهای کربن-هیدروژن و کربن-هالوژن شکسته میشود تا یک پیوند دوگانهٔ C=C از نوع پی بسازد.
ویژگیها:
- E2 یک فرایند تک مرحلهای حذف، با حالت انتقال یکتا است.
- معمولاً با جانشینهای درجه یک یا دوی آلکیل-هالید همراه است.
- سرعت واکنش که هم از آلکیل-هالید اثر میپذیرد و هم از مادهٔ قلیایی (دومولکولی)، درجهٔ دو است.
- E2 باید یک مادهٔ شیمیایی به اندازهٔ کافی قوی داشته باشد تا بر یک اسید ضعیف چیره شود برای همین معمولاً یک مادهٔ قلیایی قوی مورد نیاز است.
- پیوند C-H در گام سرعت سنجی واکنش بسیار ضعیف میشود بنابراین تأثیر ایزوتوپ دوتریوم بسیار بزرگتر از ۱ (معمولاً ۲ تا ۶) که مشاهده میشود است.
- واکنش E2 بسیار به واکنش جانشینی هسته دوست دو مولکولی همانند است.

واکنش ایزوبوتیلبرمید با پتاسیماتوکسید در اتانول که در بالا نشان داده شدهاست، یک نمونه واکنش E2 است. محصول این واکنش ایزوبوتیلن، اتانول و پتاسیم برمید است.
سازوکار E1[ویرایش]
E1 برای اشاره به حذف تک مولکولی در واقع، مدلی برای توضیح گونهٔ ویژهای از واکنش شیمیایی حذفی است. ویژگیهای این سازوکار عبارت است از:
- این یک فرایند دو گامی حذف است: ۱) یونی کردن ۲) حذف پروتون یا یون هیدروژن
- در یونش: پیوند کربن-هالوژن میشکند تا یک یون کربن با بار مثبت برجای بگذارد.
- حذف پروتون یون کربن
- E1 معمولاً در میان پیوند کربن-کربن آلکیل-هالیدها رخ میدهد. اما میتواند با برخی آلکیل-هالیدهای درجه دو هم انجام شود.
- سرعت واکنش تنها از غلظت آلکیل-هالید اثر میپذیرد چون تشکیل یون کربن مثبت آهستهترین گام این واکنش است.
- واکنش معمولاً در حضور یک مادهٔ قلیایی ضعیف و حتی نبود مادهٔ قلیایی رخ میدهد (شرایط اسیدی و دمای بالا)
- واکنشهای E1 با واکنش جانشینی هسته دوست یک مولکولی مقایسه میشود چون هر دو یک یون کربن مثبت مشترک دارند.
- یک اثر ایزوتوپ دوتریوم درجهٔ دو که اندکی بزرگتر از ۱ است (میان ۱ تا ۱٫۵) دیده میشود.
- به antiperiplanar نیاز نیست. یک نمونه: گرماکافت یک سولفونات استر ویژه با منتول:

محصول A تنها از حذف antiperiplanar بدست میآید و محصول B شاهدی است بر اینکه سازوکار انجام شده E1 است.[۳]
- همراه با واکنش بازآرایی یون کربن مثبت خواهد بود.

یک نمونه از این سازوکار که در بالا نشان داده شده، واکنش ترت-بوتیلبرمید با پتاسیم اتوکسید در اتانول است.
منابع[ویرایش]
- ↑ Organic Syntheses I:185 http://orgsynth.org/orgsyn/pdfs/CV1P0183.pdf
- ↑ March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- ↑ Nash, J. J. ; Leininger, M. A. ; Keyes, K. (2008). "Pyrolysis of Aryl Sulfonate Esters in the Absence of Solvent: E1 or E2? A Puzzle for the Organic Laboratory". Journal of Chemical Education. 85 (4): 552. Bibcode:2008JChEd..85..552N. doi:10.1021/ed085p552.
{{cite journal}}: Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link)
