سرطان لوزالمعده: تفاوت میان نسخهها
نئوپلاسم پاپیلاری موسینی داخل مجاری - یکدست کردن عنوانی که در چندجای مقاله بهکار رفته است |
←هیستوپاتولوژی: آسیبشناسی بافتی : جدول |
||
| خط ۱۳۷: | خط ۱۳۷: | ||
نتایج حاصل از [[آزمون عملکرد کبد]] میتواند نشاندهنده انسداد مجرای صفراوی (افزایش [[بیلیروبین]] کونژوگه، [[گاما گلوتامیل ترانس پپتیداز]] و [[آلکالین فسفاتاز]]) باشد. [[سیای۱۹-۹]] (آنتیژن کربوهیدرات ۱۹٫۹) یک [[نشانگر تومور]] است که اغلب در سرطان لوزالمعده افزایش مییابد. با این حال، [[حساسیت و ویژگی]] ندارد، دستکم به این دلیل که ۵٪ از افراد فاقد آنتیژن لوئیس (a) هستند و نمیتوانند این آنتیژن تولید کنند. [[سیای۱۹-۹]] حساسیت ۸۰ درصد و ویژگی ۷۳ درصد در تشخیص آدنوکارسینوم لوزالمعده دارد و بیشتر برای پیگیری موارد شناخته شده استفاده میشود؛ تا تشخیص بیماری.<ref name="NEJM14" /><ref name="Bond-Smith"/> |
نتایج حاصل از [[آزمون عملکرد کبد]] میتواند نشاندهنده انسداد مجرای صفراوی (افزایش [[بیلیروبین]] کونژوگه، [[گاما گلوتامیل ترانس پپتیداز]] و [[آلکالین فسفاتاز]]) باشد. [[سیای۱۹-۹]] (آنتیژن کربوهیدرات ۱۹٫۹) یک [[نشانگر تومور]] است که اغلب در سرطان لوزالمعده افزایش مییابد. با این حال، [[حساسیت و ویژگی]] ندارد، دستکم به این دلیل که ۵٪ از افراد فاقد آنتیژن لوئیس (a) هستند و نمیتوانند این آنتیژن تولید کنند. [[سیای۱۹-۹]] حساسیت ۸۰ درصد و ویژگی ۷۳ درصد در تشخیص آدنوکارسینوم لوزالمعده دارد و بیشتر برای پیگیری موارد شناخته شده استفاده میشود؛ تا تشخیص بیماری.<ref name="NEJM14" /><ref name="Bond-Smith"/> |
||
===آسیبشناسی بافتی === |
|||
===هیستوپاتولوژی === |
|||
شایعترین شکل سرطان لوزالمعده (آدنوکارسینوم) در زیر میکروسکوپ به صورت سلولهای غدهای [[آناپلازی|تمایز نیافته]] یا نسبتاً تمایزیافته مشخص میشود. معمولاً دسموپلازی قابلتوجه، یا تشکیل یک [[استروما|استرومای]] فیبروز متراکم، یا بافت ساختاری متشکل از طیفی از انواع سلولها (شامل میوفیبروبلاستها، [[ماکروفاژ]]ها، [[لنفوسیت]]ها و [[ماستسل]]ها) و مواد تهنشین شده (مانند [[کلاژن نوع ۱]] و [[هیالورونیک اسید]]) هم وجود دارد. این یک [[ریزمحیط تومور]] ایجاد میکند که دارای کمبود [[رگ خونی|رگهای خونی]] (هیپوواسکولار) و در نتیجه کمبود [[اکسیژن]] (هیپوکسی تومور) است.<ref name="NEJM14" /> اعتقاد بر آن است که این امر از رسیدن بسیاری از داروهای شیمیدرمانی به تومور جلوگیری میکند، و این یکی از دلایلی است درمان سرطان لوزالمعده را بهطور اخص سختتر میکند.<ref name="NEJM14" /><ref name="Wolfgang2013"/> |
شایعترین شکل سرطان لوزالمعده (آدنوکارسینوم) در زیر میکروسکوپ به صورت سلولهای غدهای [[آناپلازی|تمایز نیافته]] یا نسبتاً تمایزیافته مشخص میشود. معمولاً دسموپلازی قابلتوجه، یا تشکیل یک [[استروما|استرومای]] فیبروز متراکم، یا بافت ساختاری متشکل از طیفی از انواع سلولها (شامل میوفیبروبلاستها، [[ماکروفاژ]]ها، [[لنفوسیت]]ها و [[ماستسل]]ها) و مواد تهنشین شده (مانند [[کلاژن نوع ۱]] و [[هیالورونیک اسید]]) هم وجود دارد. این یک [[ریزمحیط تومور]] ایجاد میکند که دارای کمبود [[رگ خونی|رگهای خونی]] (هیپوواسکولار) و در نتیجه کمبود [[اکسیژن]] (هیپوکسی تومور) است.<ref name="NEJM14" /> اعتقاد بر آن است که این امر از رسیدن بسیاری از داروهای شیمیدرمانی به تومور جلوگیری میکند، و این یکی از دلایلی است درمان سرطان لوزالمعده را بهطور اخص سختتر میکند.<ref name="NEJM14" /><ref name="Wolfgang2013"/> |
||
{|class="wikitable" |
|||
! نوع سرطان !! میزان بروز نسبی<ref name="Pishvaian2017">Unless otherwise specified in boxes, reference is: {{cite journal | vauthors = Pishvaian MJ, Brody JR | title = Therapeutic Implications of Molecular Subtyping for Pancreatic Cancer | journal = Oncology | volume = 31 | issue = 3 | pages = 159–66, 168 | date = March 2017 | pmid = 28299752 | url = https://pubmed.ncbi.nlm.nih.gov/28299752 }}</ref>!! یافتههای میکروسکوپی<ref name="Pishvaian2017"/> !! [[عکاسی ریزنگاری|ریزنگار]] !! نشانگرهای [[ایمونوهیستوشیمی]]<ref name="Pishvaian2017"/> !! ژنهای درگیر<ref name="Pishvaian2017"/> |
|||
|- |
|||
! آدنوکارسینوم مجرای لوزالمعده (PDAC) |
|||
| ۹۰٪ || غدد و [[دسموپلازی]] || [[File:Histopathology of pancreatic ductal adenocarcinoma.jpg|190px]] || |
|||
* [[پی۵۳]] ناهنجار |
|||
*نقص [[SMAD4]] |
|||
*[[موسین نوع کوتاه اس ۱]] |
|||
*[[مزوتلین]] |
|||
*[[سیای۱۹-۹]] |
|||
| |
|||
*[[پی۵۳]] |
|||
*[[SMAD4]] |
|||
*[[KRAS]] |
|||
*[[پی۱۶]] |
|||
|- |
|||
! [[کارسینوم سلول آسینار لوزالمعده]] (ACC) |
|||
| ۱٪ تا ۲٪ |
|||
| نمای دانهدانه و سنبادهمانند || [[File:Histopathology of acinar cell carcinoma of the pancreas.jpg|190px]] |
|||
| |
|||
*[[تریپسین]] |
|||
*[[کیموتریپسین]] |
|||
*[[لیپاز]] |
|||
| |
|||
*[[پی۵۳]] |
|||
*[[SMAD4]] |
|||
*[[APC (پروتئین)|APC]] |
|||
*[[ARID1A]] |
|||
*[[جایگاه کمپلکس جیانایاس|GNAS]] |
|||
|- |
|||
! تومور یکپارچه پاپیلاری کاذب |
|||
| || لانههای سلولی نامنسجم تومور که توسط نوارهای فیبری نازک احاطه شدهاند || [[File:Histopathology of solid pseudopapillary tumor.png|190px]]<br>بزرگنمایی زیاد و کم<ref name=SolidPseudopapillary>Image by Mikael Häggström, MD.<br>Reference for features: {{cite web|url=https://www.pathologyoutlines.com/topic/pancreassolidpseudo.html|title=Solid pseudopapillary neoplasm|author=Pooja Navale, M.D., Omid Savari, M.D., Joseph F. Tomashefski, Jr., M.D., Monika Vyas, M.D.}} Last author update: 4 March 2022</ref> |
|||
| |
|||
*[[بتا-کاتنین]] ([[بیان ژن|بیان]] نابجای هستهای)<ref name=SolidPseudopapillary/> |
|||
*[[کاتنین پی۱۲۰]] (رنگ سیتومپلاسمی)<ref name=SolidPseudopapillary/> |
|||
| |
|||
* جهش نقطهای در [[اگزون]] ۳ ژن [[بتا-کاتنین]]<ref name=SolidPseudopapillary/> |
|||
|- |
|||
! [[کارسینوم آدنواسکوآموس]] |
|||
| ۱٪ تا ۴٪<ref name="SkafidaGrammatoglou2010">{{cite journal | vauthors = Skafida E, Grammatoglou X, Glava C, Zissis D, Paschalidis N, Katsamagkou E, Firfiris N, Vasilakaki T | display-authors = 6 | title = Adenosquamous carcinoma of the pancreas: a case report | journal = Cases Journal | volume = 3 | issue = 1 | page = 41 | date = February 2010 | pmid = 20205828 | doi = 10.1186/1757-1626-3-41 | pmc = 2825199 | doi-access = free }}</ref> || Cترکیبی از سلولهای غدهمانند و سلولهای [[بافت پوششی]] سنگفرشی || [[File:Histopathology of adenosquamous carcinoma of the pancreas.jpg|190px]] || حضورِ: |
|||
*[[آنتیبادیهای ساتوکراتین ۵/۶|CK5/6]] |
|||
*[[کراتین ۷]] |
|||
*[[تیپی۶۳|p63]] |
|||
فقدانِ: |
|||
*[[کراتین ۲۰]] |
|||
*[[پی۱۶]] |
|||
*[[پی۵۳]] |
|||
| |
|||
*[[KRAS]] |
|||
*[[پی۵۳]] |
|||
|- |
|||
! [[تومور نوراندوکرین لوزالمعده]] |
|||
| ۵٪ |
|||
| لانههای متعدد سلولی تومور || [[File:Gastrinoma.jpg|190px|center]] [[گاسترینوما]] || |
|||
*[[کروموگرانین]] |
|||
*[[سیناپتوفیزین]] |
|||
| |
|||
*[[MEN1]] |
|||
*[[DAXX]]/[[ATRX]] |
|||
|- |
|||
|colspan=6| ضایعه پیشسرطانی جهت مقایسه: |
|||
|- |
|||
! پیشسرطانی:<br>[[نئوپلاسم پاپیلاری موسینی داخل مجاری]] (IPMN) |
|||
|۳٪ |
|||
| سلولهای اپیتلیایی موسینی.<ref>{{cite web|url=http://www.pathologyoutlines.com/topic/pancreasipmn.html|title=Pancreas – Exocrine tumors / carcinomas – Intraductal papillary mucinous neoplasm (IPMN)|website=Pathology Outlines|author=Diana Agostini-Vulaj}} Topic Completed: 1 July 2018. Revised: 9 March 2020</ref> رشد درون مجاری لوزالمعده.<ref name="AdsayMino-Kenudson2016">{{cite journal | vauthors = Adsay V, Mino-Kenudson M, Furukawa T, Basturk O, Zamboni G, Marchegiani G, Bassi C, Salvia R, Malleo G, Paiella S, Wolfgang CL, Matthaei H, Offerhaus GJ, Adham M, Bruno MJ, Reid MD, Krasinskas A, Klöppel G, Ohike N, Tajiri T, Jang KT, Roa JC, Allen P, Fernández-del Castillo C, Jang JY, Klimstra DS, Hruban RH | display-authors = 6 | title = Pathologic Evaluation and Reporting of Intraductal Papillary Mucinous Neoplasms of the Pancreas and Other Tumoral Intraepithelial Neoplasms of Pancreatobiliary Tract: Recommendations of Verona Consensus Meeting | journal = Annals of Surgery | volume = 263 | issue = 1 | pages = 162–77 | date = January 2016 | pmid = 25775066 | pmc = 4568174 | doi = 10.1097/SLA.0000000000001173 }}</ref> || [[File:Histopathology of pancreatobiliary intraductal papillary mucinous neoplasm in the pancreas.jpg|190px]] |
|||
| |
|||
*[[موسین ۵ایسی]] |
|||
| |
|||
*[[KRAS]] |
|||
*[[جایگاه کمپلکس جیانایاس|GNAS]] |
|||
|} |
|||
== پیشگیری و غربالگری == |
== پیشگیری و غربالگری == |
||
نسخهٔ ۵ مهٔ ۲۰۲۴، ساعت ۰۶:۱۴
این مقاله یا بخشی از آن تحت نگارش، توسعه یا بازنویسی گسترده قرار دارد. از کمک شما در ویرایش و نگارش آن استقبال میکنیم؛ خوش آمدید. اگر این مقاله یا بخش چندین روز است که ویرایش نشده، لطفاً این الگو را حذف کنید. اگر خودتان این برچسب را در صفحه قرار دادهاید و همچنان در حال ویرایش صفحه هستید، لطفاً در زمانهایی که مشغول ویرایش هستید این الگو را با {{ویرایش}} جایگزین کنید. برای آگاهی از پارامترهای الگو روی پیوند آن کلیک کنید. این مقاله آخرین بار در ۳۶ روز پیش توسط Tisfoon (بحث | مشارکتها) ویرایش شدهاست. (روزآمدسازی زمانسنج) |
| سرطان لوزالمعده (سرطان پانکراس) | |
|---|---|
 | |
| نموداری که موقعیت لوزالمعده را در پشت معده نشان میدهد (که در این تصویر به رنگ زرد دیده میشود) | |
| تخصص | |
| نشانهها |
|
| دورهٔ معمول آغاز | سن بالای ۴۰ سال[۲] |
| عوامل خطر | |
| روش تشخیص |
|
| پیشگیری | عدم استعمال دخانیات، محدود کردن مصرف الکل، حفظ وزن بدن در محدوده طبیعی و سالم، کاهش مصرف گوشت قرمز[۵] |
| درمان | |
| پیشآگهی | میزان بقای پنج ساله ۱۳٪[۶] |
| فراوانی | ۳۹۳٬۸۰۰ (۲۰۱۵)[۷] |
| مرگها | ۴۱۱٬۶۰۰ (۲۰۱۵)[۸] |
| طبقهبندی و منابع بیرونی | |
سرطان لوزالمعده یا سرطان پانکراس (به انگلیسی: Pancreatic cancer) نوعی سرطان است که در اثر تکثیر و رشد کنترلنشدهٔ سلولهای بافت غدهٔ لوزالمعده (که پشت معده قرار دارد) پدید میآید و یک توده تشکیل میشود. این سلولهای سرطانی توانایی حمله به دیگر بخشهای بدن را دارند.[۹] چندین نوع متفاوت از سرطان لوزالمعده وجود دارد.
رایجترین نوع که آدنوکارسینوم لوزالمعده نام دارد، ۹۰٪ موارد را شامل میشود[۱۰] و عبارت «سرطان لوزالمعده» گاهی فقط برای اشاره به این نوع سرطان استفاده میشود.[۱۱] این آدنوکارسینومها از بخشی از لوزالمعده شروع میشود که مسئول ساخت آنزیمهای گوارشی است.[۱۱] چندین نوع سرطان دیگر نیز که در مجموع به آنها «غیر آدنوکارسینومی» میگویند ممکن است از این سلولها ایجاد شوند.[۱۱]
۲–۱ درصد از سرطانهای لوزالمعده تومورهای نورواندوکرین هستند که از سلولهای تولیدکنندهٔ هورمون لوزالمعده به وجود میآیند.[۱۱] در کل، میزان تهاجمی بودن این تومورها، کمتر از آدنوکارسینوم است.[۱۱]
علائم و نشانههای رایجترین نوع سرطان لوزالمعده شامل این موارد است: زردی پوست، دردِ شکم یا درد پشت، کاهش وزن غیرتعمدی و بیدلیل، کمرنگ شدنِ مدفوع، ادرار تیره و بیاشتهایی.[۱] معمولاً در مراحل اولیهٔ بیمارِی، علائمی وجود ندارد و علائمی که شاخص قطعی بیماری هستند و به اندازهای خاص هستند که بتوانند ما را به سرطان لوزالمعده مشکوک کنند، معمولاً زمانی پدیدار میشوند که بیماری به مرحلهٔ پیشرفتهٔ خود رسیده است.[۱][۲] در زمانِ تشخیص، سرطان لوزالمعده معمولاً به نقاط دیگر بدن نیز گسترش یافته است.[۱۱][۱۲]
سرطان لوزالمعده بهندرت در سنین پایینتر از ۴۰ سال رخ میدهد و بیش از نیمی از موارد آدنوکارسینوم لوزالمعده در افراد بالای ۷۰ سال دیده میشود.[۲] عواملِ خطرسازِ سرطان لوزالمعده شامل این موارد است: استعمال دخانیات، چاقی، دیابت و اختلالات ژنتیکی خاص.[۲] حدود ۲۵ درصد موارد، با کشیدن سیگار مرتبط است[۳] و ۵–۱۰٪ نیز وراثتی هستند.[۲]
سرطان لوزالمعده معمولاً به کمک ترکیبی از این روشها تشخیص داده میشود: تصویربرداری پزشکی مانند سونوگرافی یا سیتی اسکن، آزمایش خون، و بررسی نمونههای بافتی.[۳][۴] این بیماری به چند مرحله تقسیم میشود؛ از مرحلهٔ اولیه (مرحلهٔ ۱) تا مرحلهٔ آخر (مرحلهٔ ۵).[۱۲] انجام غربالگری سرطان در جمعیت عمومی مؤثر تشخیص داده نشده است.[۱۳] خطر ابتلا به سرطان لوزالمعده در میان افراد غیر سیگاری و افرادی که وزن مناسبی دارند و مصرف گوشت قرمز یا فرآوریشده را محدود میکنند، کمتر است.[۵] با این حال، این خطر برای مردان بیشتر است، به خصوص در صورت مصرف بسیار زیاد گوشت قرمز.[۱۴] با این حال، این یافته مورد بحث است، زیرا مثلاً مطالعهای که توسط ژورنال بینالمللی سرطان در سال ۲۰۱۳ انجام شد، هیچ رابطه آماری معنیداری بین مصرف گوشت قرمز و سرطان لوزالمعده پیدا نکرد، همچنین هیچ ارتباطی با جنس مذکر هم یافت نشد و تنها ارتباط مثبتی بین مصرف گوشت قرمز با خطر ابتلا به سرطان لوزالمعده در زنان مشاهده شد؛ آن هم پس از محدود کردن مطالعه به مواردی که حضور سلولهای سرطانی در بافت لوزالمعده با بررسیِ میکروسکوپی تأیید شده بود.[۱۵] خطر ابتلا به این بیماری در افراد سیگاری بلافاصله پس از ترک کاهش مییابد و تقریباً پس از ۲۰ سال احتمال ابتلای آنها با بقیهٔ افراد برابر میشود.[۱۱] مدیریت درمانی سرطان لوزالمعده با جراحی، پرتودرمانی، شیمیدرمانی، مراقبت تسکینی یا ترکیبی از این موارد انجام میشود.[۱] گزینههای درمانی تا حدی بر اساس مرحله سرطان انتخاب میگردد.[۱] جراحی تنها روشی است که ممکن است آدنوکارسینوم لوزالمعده را درمان کند،[۱۲] و همچنین ممکن است بهمنظور بهبود کیفیت زندگی در آنهایی که احتمال درمان قطعی ندارند، انجام شود.[۱][۱۲] مدیریت درد و تجویز داروهای کمککننده به هضمِ غذا بعضاً لازم هستند.[۱۲] مراقبت تسکینی زودهنگام برای همهٔ موارد مبتلا به این بیماری توصیه میشود، حتی برای کسانی که تحت مراقبت با هدف درمان قطعی هستند.[۱۶]
سرطان لوزالمعده یکی از کشندهترین انواع سرطان در سطح جهان است و یکی از کمترین نرخهای بقا را دارد. در سال ۲۰۱۵، انواع سرطان لوزالمعده منجر به مرگ ۴۱۱٬۶۰۰ نفر در سراسر جهان شد.[۸] سرطان لوزالمعده پنجمین علتِ شایعِ مرگِ ناشی از سرطان در بریتانیا[۱۷] و سومین علتِ شایعِ مرگِ ناشی از سرطان در ایالات متحده آمریکا است.[۱۸] این بیماری اغلب در کشورهای توسعهیافته رخ میدهد و این کشورها در سال ۲۰۱۲ شاهد ۷۰ درصد از کلِ موارد جدید این بیماری در جهان بودهاند.[۱۱] آدنوکارسینوم لوزالمعده معمولاً پیشآگهی بسیار بدی دارد. پس از تشخیص بیماری، حدود ۲۵٪ از مبتلایان، یک سال زنده میمانند و ۱۲٪ به مدت پنج سال زنده میمانند.[۶][۱۱] اگر سرطان زود تشخیص داده شود، میزان بقای پنج ساله تا حدود ۲۰٪ افزایش مییابد.[۱۹] پیامد سرطانهای نورواندوکرین بهتر از آدنوکارسینوم است. پس از گذشت ۵ سال از تشخیص و درمان، ۶۵ درصد از افراد مبتلا زنده هستند، اگرچه میزان بقا بسته به نوع تومور بهطور قابل توجهی متفاوت است.[۱۱]
انواع


انواع متعدد سرطان لوزالمعده را میتوان به دو گروه کلی تقسیم کرد. اکثریت قریب به اتفاق موارد (حدود ۹۵٪) در بخشی از لوزالمعده رخ میدهد که آنزیمهای گوارشی را تولید میکند که به عنوان جزء برونریز شناخته میشود. انواع مختلفی از سرطانهای برونریز لوزالمعده شرح داده شده است، اما تشخیص و درمان آنها اشتراک فراوانی دارد. میزان اندکی از سرطانهایی که در بافت تولیدکننده هورمون (دستگاه درونریز) لوزالمعده ایجاد میشوند، ویژگیهای بالینی متفاوتی دارند و به آنها تومورهای نوراندوکرین لوزالمعده میگویند که گاهی به اختصار «PanNETs» هم نوشته میشود. هر دو گروه بیشتر (اما نه منحصراً) در افراد بالای ۴۰ سال رخ میدهند و در مردان کمی شایعتر هستند؛ اما برخی از زیرگروههای نادر سرطان لوزالمعده بیشتر در زنان یا کودکان رخ میدهند.[۲۱][۲۲]
اِگزوکرین (برونریز)
انواع برونریز؛ سرطان، بیشتر از نوعِ «آدنوکارسینوم» است (گاهی عباراتی چون «تهاجمی» و «مجرایی» هم به نام اینگونه سرطانها اضافه میشود)، که شایعترین نوع سرطان لوزالمعده محسوب میشوند و حدود ۸۵٪ از تمام سرطانهای لوزالمعده را در برمیگیرند.[۲] تقریباً همه اینها در مجاری لوزالمعده، و به صورت «آدنوکارسینوم مجرای لوزالمعده» (PDAC) آغاز میشوند.[۲۳] این در حالی است که بافتی که سرطان از آن نشأت میگیرد - اپیتلیوم مجرای لوزالمعده - کمتر از ۱۰٪ از غدهٔ لوزالمعده را از نظر حجم سلولی تشکیل میدهد، زیرا تنها از مجاری لولهایشکل (یک سیستم مجرایی گسترده اما مویرگیمانند که به بیرون شاخه شاخه میشود) تشکیل شده است.[۲۴] این سرطان از سلولهای مجاری حملکننده ترشحات (مانند آنزیمها و بیکربنات) به بیرونِ لوزالمعده ایجاد میشود. حدود ۶۰ تا ۷۰ درصد از آدنوکارسینومها در سرِ لوزالمعده رخ میدهد.[۲]
شایعترین نوع بعدی، یعنی کارسینوم سلول آسینار لوزالمعده، در آن دسته از سلولهایی تشکیل میشود که سازندهٔ آنزیم هستند و ۵ درصد از سرطانهای برونریز لوزالمعده را شامل میشود.[۲۵] همچون سرطانهایِ غددِ درونریزِ «عملکردی» که در زیر توضیح داده شده است، کارسینوم سلول آسینار ممکن است باعث تولید بیش از حد مولکولهای خاص - در این مورد آنزیمهای گوارشی - شود که قادر به ایجادِ علائمی چون بثورات پوستی و درد مفاصل است.
سیستآدنوکارسینوم لوزالمعده ۱٪ از سرطانهای لوزالمعده را تشکیل میدهند و پیشآگهی بهتری نسبت به سایر انواع برونریز دارد.[۲۵]
پانکراتوبلاستوم نوع نادری است که بیشتر در دوران کودکی رخ میدهد و پیشآگهی نسبتاً خوبی دارد. سایر سرطانهای برونریز شامل کارسینومهای آدنوسکواموس، کارسینومهای سلول نگینی، کارسینومهای هپاتوئید، کارسینومهای کلوئیدی، کارسینومهای تمایزنیافته و کارسینومهای تمایزنیافته با سلولهای ژانت استئوکلاستمانند هستند. تومور جامد پاپیلاری کاذب نوعی بدخیمی با درجه پایین نادر است که بیشتر در زنان جوانتر روی میدهد و عموماً پیشآگهی بسیار خوبی دارد.[۲][۲۶]
بدخیمی کیستهای موسینی لوزالمعده گروه وسیعی از تومورهای لوزالمعده هستند که پتانسیل بدخیم متفاوتی دارند. با افزایش قدرت تشخیصی و رایج شدن سیتی اسکنها، این نوع تومورها به میزانِ بسیار بیشتری از قبل شناسایی میشوند، و بحث در مورد بهترین روش ارزیابی و درمان آنها ادامه دارد، چرا که بسیاری از آنها خوشخیم هستند.[۲۷]
نوراندوکرین (درونریز)
تعداد بسیار اندکی از تومورهایی که در سایر نقاط لوزالمعده ایجاد میشوند، عمدتاً تومورهای نوراندوکرین (درونریز) لوزالمعده (PanNETs) هستند.[۲۸] تومورهای نوراندوکرین درونریز (NETs) گروه متنوعی از تومورهای خوشخیم یا بدخیم هستند که از سلولهای نوراندوکرینِ غدد درونریز بدن به وجود میآیند که مسئول یکپارچهسازی و هماهنگی دستگاه عصبی و غدد درونریز هستند. تومورهای نوراندوکرین درونریز (NETs) ممکن است در بیشتر اعضا و احشایهای بدن، از جمله لوزالمعده رشد کنند که البته در لوزالمعده انواع مختلف بدخیم آن نادر هستند. تومورهای نوراندوکرین لوزالمعدهها بسته به میزان تولید هورمون به دو نوع «عملکردی» (فعال) و «غیر عملکردی» (غیرفعال) دستهبندی میشوند. انواع فعال هورمونهایی مانند انسولین، گاسترین و گلوکاگون را به مقدار زیاد در جریان خون ترشح میکنند که منجر به علائم مهم و بالقوه خطرناکی مانند افت قند خون میشود، اما خوبیشان آن است که چنین چیزی منجر به تشخیص نسبتاً زودهنگام سرطان میشوند. رایجترین انواع تومورهای نوراندوکرین (درونریز) لوزالمعده فعال انسولینما و گاسترینوما هستند که نام آنها برگرفته از هورمونهایی است که ترشح میکنند. انواع غیرعملکردی، آنقدری هورمون ترشح نمیکنند تا علائم بالینی آشکار ایجاد شود، بنابراین تومورهای غیرعملکردی نوراندوکرین لوزالمعده تنها پس از گسترش سرطان به سایر قسمتهای بدن تشخیص داده میشوند.[۲۹]
همچون سایرِ تومورهای نوراندوکرین درونریز، تاریخچه اصطلاحات و طبقهبندی این تومورها پیچیده است.[۲۸] این سرطانهای لوزالمعده گاهی «سرطان سلول جزیرهای» نامیده میشوند،[۳۰] اگرچه اکنون معلوم شده است که برخلاف تصور قبلی، در واقع از سلولهای جزایر لانگرهانس نشات نمیگیرند.[۲۹]
علائم و نشانهها

از آنجایی که معمولاً در مراحل اولیه سرطان لوزالمعده علائم قابل تشخیصی وجود ندارد، این بیماری معمولاً زمانی تشخیص داده میشود که سرطان فراتر از لوزالمعده گسترش یافته است.[۴] این موضوع یکی از دلایل اصلی میزان اندک بقای مبتلایان است. تومورهایِ نورواندوکرینِ فعالِ لوزالمعده در این مورد استثنا هستند؛ چرا که تولید بیش از حد هورمونهای فعال مختلف در این تومورها منجر به شکلگیری علائم (که به نوع هورمون بستگی دارد) میشود.[۳۱]
علائم رایج آدنوکارسینوم لوزالمعده عبارتند از:
- درد در قسمت بالایی شکم یا پشت که اغلب از جلو (اطراف معده) به پشت میزند. محل درد میتواند نشان دهنده بخشی از لوزالمعده باشد که تومور در آن قرار دارد. درد ممکن است در شب بدتر شود و در طول زمان افزایش یابد تا شدید و بیوقفه شود.[۲۵] درد همچنین ممکن است با خم شدن به جلو کمی تسکین یابد. در بریتانیا، حدود نیمی از موارد جدید سرطان لوزالمعده پس از مراجعه افراد به بخش اورژانس بیمارستان برای شکمدرد یا زردی پوست تشخیص داده میشود. در بیش از دو سوم افراد، درد شکم علامت اصلی است، که ۴۶٪ آنها زردی پوست (یرقان) هم دارند. در ۱۳٪ مبتلایان، زردی پوست با درد شکم همراه نیست.[۱۲]
- یرقان یا زردی، که در سفیدی چشمها یا پوست، با یا بدون درد، دیده میشود و گاهی با ادرار تیره همراه است. این علامت زمانی ایجاد میشود که سرطان در سرِ لوزالمعده باشد و مجرای صفراوی مشترک را در محلِ عبور از لوزالمعده مسدود کند.[۳۲]
- کاشکسی یا کاهشِ وزنِ غیرقابل توضیح و غیر تعمدی، که یا بهدلیل بیاشتهایی است، یا به سبب اختلال در عملکرد برونریز لوزالمعده که منجر به سوءهاضمه میشود.[۱۲]
- تومور لوزالمعده ممکن است بر روی احشای مجاور فشار بیاورد و فرآیندهای گوارشی را مختل و تخلیه معده را دشوار کند که این فرایند گاهی باعث تهوع و احساس پُری میشود. چربی هضمنشده منجر به مدفوع بدبو و چرب میگردد که به سختی دفع میشود.[۱۲] یبوست نیز شایع است.[۳۳]
- دستکم ۵۰ درصد از افراد مبتلا به آدنوکارسینوم لوزالمعده در زمانِ تشخیص، دیابت دارند.[۲] در حالی که ابتلا به دیابت طولانیمدت، خود یک عاملِ خطرِ شناختهشده برای سرطان لوزالمعده است (به عوامل خطر مراجعه کنید)، سرطان، خودش میتواند باعث دیابت شود، که در این صورت، دیابتِ نوظهور گاهی نشانه اولیه سرطان لوزالمعده در نظر گرفته میشود.[۳۴] افراد بالای ۵۰ سال که برای نخستین بار به دیابت مبتلا میشوند، ظرفِ سه سال آتی، هشت برابر بیشتر از افراد عادی، خطرِ ابتلا به آدنوکارسینومِ لوزالمعده دارند و پس از آن، خطرِ نسبیِ ابتلا کاهش مییابد.[۱۲]
یافتههای دیگر
- سندرم تروسو - که در آن لختههای خون بهطور خودبهخود در رگهای خونی پورتال (ترومبوز وریدپورت)، سیاهرگهای عمقی اندامها (ترومبوز سیاهرگی عمقی)، یا سیاهرگهای سطحی (ترومبوز سیاهرگی سطحی) در هر نقطه از بدن تشکیل میشوند - ممکن است با سرطان لوزالمعده و در حدود ۱۰ درصد موارد آن دیده شوند.[۳]
- افسردگی بالینی مرتبط با سرطان لوزالمعده در حدود ۱۰ تا ۲۰ درصد موارد این سرطان گزارش شده است و میتواند مانعی برای مدیریت بهینه آن باشد. افسردگی گاهی پیش از تشخیص سرطان لوزالمعده ظاهر میشود و نشان میدهد که شاید توسط فرایندهای بیولوژیک بیماری ایجاد شود.[۳]
- سایر تظاهرات شایع این بیماری عبارتند از: ضعف و خستگی زودرس، خشکی دهان، مشکلات خواب، و توده قابل لمس شکمی.[۳۳]
علائم گسترش سرطان

- گسترش سرطان لوزالمعده به سایر اندامها (متاستاز) نیز ممکن است علائمی ایجاد کند. معمولاً آدنوکارسینوم لوزالمعده ابتدا به گرههای لنفاوی مجاور و بعداً به کبد یا حفره صفاقی، روده بزرگ یا ریهها گسترش مییابد.[۳] سرطان لوزالمعده بهطور غیرمعمول، به استخوانها یا مغز هم ممکن است سرایت کند.[۳۵]
- تومورهای شکلگرفته در لوزالمعده نیز ممکن است سرطانهای ثانویه باشند که از سایر قسمتهای بدن آمدهاند. البته این موضوع نامعمول است و تنها در حدود ۲ درصد موارد سرطان لوزالمعده دیده میشود. تومور کلیه شایعترین سرطانی است که به لوزالمعده میزند و پس از آن سرطان روده بزرگ و سپس ملانوما، سرطان پستان و سرطان ریه قرار دارند. در چنین مواردی، چه به امید درمان قطعی و چه برای کاهش علائم، ممکن است جراحی روی لوزالمعده ضرورت یابد.[۳۶]
عوامل خطرساز
عوامل خطرساز بروز آدنوکارسینوم لوزالمعده به شرح زیر است:[۲][۱۱][۱۲][۳۷][۳۸]
- سن، جنس و قومیت – خطر ابتلا به سرطان لوزالمعده با بالا رفتن سن افزایش مییابد. بیشتر موارد این سرطان پس از ۶۵ سالگی رخ میدهد[۱۱] و بروز آن پیش از ۴۰ سالگی نامعمول است. این بیماری در مردان کمی بیشتر از زنان دیده میشود.[۱۱] در ایالات متحده آمریکا، میزان وقوع آن در سیاهپوستان آمریکا بیش از ۱٫۵ برابر شایعتر است، اگرچه بروز این سرطان در قارهٔ آفریقا کم است.[۱۱]
- استعمال دخانیات شناختهشدهترین عامل خطر قابل اجتناب برای سرطان لوزالمعده است که خطر ابتلا به سرطان لوزالمعده را تقریباً دوبرابر میکند، این خطر با تعداد سیگارهای مصرفی و سالهای مصرف سیگار افزایش مییابد. این خطر پس از ترک سیگار به آرامی کاهش مییابد و حدود ۲۰ سال طول میکشد تا تقریباً به میزان ابتلای افراد غیرسیگاری بازگردد.[۳۹]
- چاقی – شاخص توده بدنی بیش از ۳۵، خطر نسبی بروز را نیم برابر بیشتر میکند.[۱۲][۴۰]
- سابقهٔ خانوادگی – ۵ تا ۱۰ درصد موارد سرطان لوزالمعده یک زمینهٔ ارثی دارد که در آن افراد مبتلا، سابقه خانوادگی سرطان لوزالمعده را دارند.[۲][۴۱] اگر بیش از یک نفر از بستگان درجه یک مبتلا به این بیماری باشند، خطر بروز بهشدت افزایش مییابد و اگر آن عضو خانواده پیش از ۵۰ سالگی به سرطان مبتلا شده باشند، خطر ابتلا در عضو دیگر خانواده دچار افزایش اندکی میشود.[۴] بسیاری از ژنهای درگیر هنوز شناسایی نشدهاند.[۲][۴۲] پانکراتیت ارثی خطر ابتلا به سرطان لوزالمعده در طول زندگی را به میزان ۳۰ تا ۴۰ درصد تا حوالی ۷۰ سالگی افزایش میدهد.[۳] غربالگری برای کشف سرطان لوزالمعده در مراحل اولیه ممکن است به دلایل پژوهشی به افراد مبتلا به پانکراتیت ارثی پیشنهاد شود.[۴۳] برخی از افراد ممکن است تصمیم بگیرند که لوزالمعده خود را برای جلوگیری از ایجاد سرطان در آینده با جراحی خارج کنند.[۳]
- سرطان لوزالمعده با سایر سندرمهای ارثی نادر مرتبط است: سندرم پوتز-جگرز به دلیل جهش در ژن سرکوبگر تومور STK11 (بسیار نادر، اما یک عامل خطرساز بسیار قوی)؛ سندرم خال دیسپلاستیک (یا سندرم خالهای متعدد آتیپیک خانوادگی و سندرم ملانوم، FAMMM-PC) بهدلیل جهش در ژن سرکوبگر تومور پی۱۶، آتاکسی-تلانژکتازی اتوزومال مغلوب و جهشهای ارثی اتوزومال غالب در ژنهای در BRCA2 و PALB2؛ سرطان روده بزرگ ارثی غیرپولیپی (موسوم به سندرم لینچ) و پولیپهای آدنوماتوز خانوادگی. بروز تومور نورواندوکرین لوزالمعده هم با نئوپلازی متعدد غدد درونریز نوع ۱ و بیماری فون هیپل لندائو مرتبط است.[۲][۳][۴]
- پانکراتیت مزمن خطر ابتلا را تقریباً سه برابر میکند، و همچون دیابت، پانکراتیت نوظهور ممکن است نشانه وجود یک تومور باشد.[۳] خطر ابتلا به سرطان لوزالمعده در افراد مبتلا به پانکراتیت خانوادگی زیاد است.[۳][۴۲]
- دیابت یک عامل خطرساز برای سرطان لوزالمعده است و (همانطور که در بخش علائم و نشانهها ذکر شد) دیابت نوظهور ممکن است نشانهٔ اولیهٔ این سرطان باشد. افرادی که بیش از ۱۰ سال مبتلا به دیابت نوع ۲ بوده باشند، ممکن است در مقایسه با افراد بدون دیابت، ۵۰ درصد بیشتر در معرض خطر این سرطان باشند.[۳] در سال ۲۰۲۱، ونتوری گزارش داد که لوزالمعده قادر به جذب مقدار زیادی سزیم رادیواکتیو (سزیم-۱۳۴ و سزیم-۱۳۷) است که باعث پانکراتیت مزمن و احتمالاً سرطان لوزالمعده با آسیب به جزایر لوزالمعده میشود و همچنین بروز دیابت نوع ۳سی (پانکراتوژنیک) میشود.[۴۴] پانکراتیت مزمن، سرطان لوزالمعده و دیابت در جمعیتهای آلوده به سزیم رادیواکتیو، به ویژه کودکان و نوجوانان، پس از حوادث هستهای فوکوشیما و چرنوبیل افزایش یافت. در عین حال، بیماریهای لوزالمعده، دیابت و سزیم رادیواکتیو محیطی در سراسر جهان در حال افزایش است.
- هنوز بهطور واضح ثابت نشده است که رژیم غذایی خاصی (جدای از مسئلهٔ چاقی) خطر ابتلا به سرطان لوزالمعده را افزایش دهد.[۲][۴۵] برخی عوامل غذایی که مطابق شواهد خطر بروز این سرطان را کمی افزایش میدهند، عبارتند از: گوشتهای فرآوریشده (مثل سوسیس و کالباس)، گوشت قرمز و گوشتهای پختهشده در دمای بسیار بالا (همچون سرخ کردن، یا هرگونه کبابی کردن روی آتش یا اجاق خانگی).[۴۵][۴۶]
الکل
نوشیدن بیش از حد الکل عامل اصلی پانکراتیت مزمن است که به نوبه خود، زمینهساز سرطان لوزالمعده است، اما مطالعات فراوان و قابلتوجهی که بتواند مصرف الکل را به عنوان یک عامل خطر مستقیم برای سرطان لوزالمعده اثبات کند، وجود ندارد. بهطور کلی، این ارتباط بهطور متداوم ضعیف بوده است و بیشتر پژوهشها هیچ ارتباطی میان این دو نشان ندادهاند و سیگار کشیدن یک عامل مخدوشکننده قوی در این مطالعات بوده است. ناگفته نماند که شواهد علمی قویتری برای ارتباط سرطان لوزالمعده با نوشیدنِ زیادِ الکل (دستکم شش نوشیدنی در روز) وجود دارد.[۳][۴۷]
پاتوفیزیولوژی

پیشسرطان
تصور میشود که سرطانهای برونریز از چندین نوع ضایعهٔ پیشسرطانی در لوزالمعده ایجاد میشوند، اما این ضایعات همیشه به سرطان منجر نشده و با این حال تعداد زیادی از این تعداد افزایش یافتهای که به عنوان محصول جانبی استفاده روزافزون از سیتی اسکن به دلایل دیگر شناسایی میشوند، همگی درمان نمیشوند. به غیر از سیستادنومهای سروزی لوزالمعده که تقریباً همیشه خوشخیم هستند، چهار نوع ضایعه پیش سرطانی شناخته شده است.[۳]

اولین مورد، نئوپلازی داخل اپیتلیال لوزالمعده (PanIN)[الف] است. این ضایعات ناهنجاریهای میکروسکوپی در لوزالمعده هستند و اغلب در کالبدشکافی افراد که بدون سرطان تشخیص داده میشوند نیز وجود دارند. این ضایعات ممکن است از درجه پایین سرطان به بالا و سپس به تومور پیشرفت کنند. بیش از ۹۰ درصد موارد در همه درجهبندیها حامل ژن KRAS معیوب هستند، در حالی که در اکثر سرطانهای درجه ۲ و ۳، آسیب به سه ژن دیگر CDKN2A (p16)، p53 و SMAD4 نیز دیده میشود.[۲]

نوع دوم نئوپلاسم پاپیلاری موسینی داخل مجاری (IPMN)[ب] است. این نئوپلاسمها، ضایعات ماکروسکوپی هستند که در حدود ۲ درصد از کل بزرگسالان یافت میشوند و این میزان در سن ۷۰ سالگی به حدود ۱۰ درصد افراد افزایش مییابد. این ضایعات حدود ۲۵ درصد خطر ابتلا به سرطان مهاجم را دارند و ممکن است دارای جهشهای ژن KRAS (40-65% موارد) و در GNAS زیرواحد Gs آلفا و RNF43 باشند که بر مسیر پیامرسانی Wnt تأثیر میگذارد.[۲] حتی اگر با جراحی برداشته شوند، همچنان خطر ابتلا به سرطان لوزالمعده بهطور قابل توجهی وجود دارد زیرا تودهها میتوانند مجدد ایجاد شوند.[۳]
نوع سوم، نئوپلاسم کیستیک موسینوس لوزالمعده (MCN)[پ]، عمدتاً در زنان رخ میدهد و ممکن است خوشخیم باقی بماند یا تبدیل به سرطان شود.[۴۹] اگر این ضایعات بزرگ شوند، علائمی ایجاد کنند یا ویژگیهای مشکوک به سرطان داشته باشند، معمولاً میتوان آنها را با موفقیت با جراحی برداشت.[۳]
نوع چهارم سرطان که در لوزالمعده ایجاد میشود، نئوپلاسم توبولوپاپیلاری داخل مجاری (ITPN)[ت] است. این نوع در سال ۲۰۱۰ توسط سازمان جهانی بهداشت به رسمیت شناخته شد و حدود ۱ تا ۳ درصد از کل نئوپلاسمهای لوزالمعده را تشکیل میدهد. میانگین سنی در هنگام تشخیص ۶۱ سال (محدوده ۳۵ تا ۷۸ سال) است و حدود ۵۰ درصد از این تودهها تهاجمی میشوند. تشخیص بستگی به نتایج بافت برداری دارد، زیرا افتراق این ضایعات از سایر اشکال نئوپلاسمهای لوزالمعده به کمک بررسیها بالینی یا رادیولوژیکی بسیار دشوار است.[۵۰]
سرطان تهاجمی
رویدادهای ژنتیکی یافت شده در آدنوکارسینوم مجرای لوزالمعده به خوبی مشخص شده و آزمایش توالییابی کامل اگزوم برای انواع رایج این تومور انجام گرفته است. چهار ژن KRAS (در ۹۵٪ موارد)، CDKN2A (همچنین در ۹۵٪)، TP53 (75%) و SMAD4 (55%) هر کدام در اکثر آدنوکارسینومها دچار جهش شدهاند و جهش در SMAD4 به صورت ویژهای با پیشآگهی ضعیف همراه است.[۳] جهش/حذف SWI/SNF در حدود ۱۰ تا ۱۵ درصد از آدنوکارسینومها رخ میدهد[۲] و تغییرات ژنتیکی در چندین نوع دیگر از سرطان پانکراس و ضایعات پیش سرطانی نیز مورد تحقیق قرار گرفته است.[۳] آنالیزهای ترنسکریپتومیکس و تعیین توالی mRNA برای اشکال رایج سرطان لوزالمعده نشان داده که ۷۵ درصد از ژنهای انسانی در تومورها بیان میشوند و تنها حدود ۲۰۰ ژنها بهطور خاصتری در سرطان لوزالمعده نسبت به سایر انواع تومور بیان میگردند.[۵۱][۵۲]
تومورهای نورواندوکرین
ژنهایی که اغلب در تومورهای نوراندوکرین (درونریز) لوزالمعده (PanNETs) جهش یافته یافت میشوند، با ژنهای سرطان اِگزوکرین (برونریز) لوزالمعده (PanNet) متفاوت هستند.[۵۳] به عنوان مثال، جهش KRAS بهطور معمول در این تومورها وجود ندارد. در عوض، جهشهای ارثی ژن MEN1 خطر سندرم MEN1 را ایجاد میکند که در آن تومورهای اولیه در دو یا چند غده درونریز ایجاد میشوند. حدود ۴۰ تا ۷۰ درصد از افرادی که با جهش MEN1 متولد میشوند، در نهایت به PanNet مبتلا میشوند.[۵۴] ژنهای دیگری که اغلب جهش مییابند شامل DAXX ,mTOR و ATRX هستند.[۲۹]
تشخیص
این مقاله هماکنون برای مدتی کوتاه تحت ویرایش عمده است. این برچسب بهمنظور جلوگیری از تعارض ویرایشی اینجا گذاشته شدهاست. لطفاً تا زمانی که این پیام در اینجا نمایش داده میشود، ویرایشی در این صفحه انجام ندهید. این صفحه آخرین بار در ۵ مه ۲۰۲۴، ساعت ۰۶:۱۴ (ساعت هماهنگ جهانی) (۳۶ روز پیش) ویرایش شده است – این زمان تخمینی موجود در میانگر است؛ . اگر این صفحه در چند ساعت اخیر ویرایش نشده است، لطفاً این الگو را حذف کنید. اگر خودتان این الگو را به صفحه اضافه کردهاید، لطفاً در میانهٔ بازههای مختلف ویرایشی آن را حذف کنید یا با {{در دست ساخت}} جایگزین کنید. |
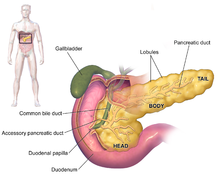


علائم آدنوکارسینوم لوزالمعده معمولاً در مراحل اولیه بیماری ظاهر نمیشوند و این علائم، اختصاصیِ این سرطان هم نیستند.[۳][۱۲][۳۲] علائم در هنگام تشخیص بسته به محل سرطان در لوزالمعده متفاوت است که کالبدشناسان آن را (از چپ به راست در اکثر نمودارها) به سر ضخیم، گردن و تنهٔ مخروطی تقسیم میکنند که به دُم آن ختم میشود.
صرف نظر از مکان تومور، شایعترین بیماری، علامت کاهش وزن غیرقابل توضیح و ناخواسته است که ممکن است شدید باشد. تعداد کمتر اما قابل توجهی (بین ۳۵ تا ۴۷ درصد) از افراد مبتلا به این بیماری تهوع، استفراغ یا احساس ضعف هم دارند. تومورهای سرِ لوزالمعده معمولاً باعث زردی، درد، بی اشتهایی، ادرار تیره و مدفوع روشن میشوند. تومورهای تنده و دم لوزالمعده نیز معمولاً باعث شکمدرد میشوند.[۳۲]
گاهی افراد مبتلا به دیابت نوظهور و نامعمول نوع ۲ هستند که کنترل آن دشوار است، یا سابقه التهاب عروق خونی نوظهور و غیرقابل توضیح ناشی از لخته شدن خون (ترومبوفلبیت) معروف به نشانه تروسو یا سابقه ابتلا قبلی به پانکراتیت هستند.[۳۲] زمانی که دیابت نوظهور در افراد بالای ۵۰ سال با علائم معمولی مانند کاهش وزن غیرقابل توضیح، درد مداوم شکم یا کمر، سوء هاضمه، استفراغ یا مدفوع چرب همراه باشد، پزشک ممکن است به حضورِ سرطان لوزالمعده مشکوک شود.[۱۲] زردی همراه با تورم بدون درد کیسه صفرا (معروف به نشانه کوروازیه) نیز ممکن است باعث ایجاد شک به سرطان لوزالمعده شود و میتواند به تمایز سرطان پانکراس از سنگ کیسه صفرا کمک کند.[۵۵]

در مواقعی که تشخیص قطعی نیست، از بافتبرداری آسپیراسیون با سوزن ظریف، که اغلب توسط سونوگرافی آندوسکوپی هدایت و انجام میشود، استفاده میشود، اما تشخیص بافتشناسی معمولاً برای برداشتن تومور با عمل جراحی لازم نیست.[۱۲]
نتایج حاصل از آزمون عملکرد کبد میتواند نشاندهنده انسداد مجرای صفراوی (افزایش بیلیروبین کونژوگه، گاما گلوتامیل ترانس پپتیداز و آلکالین فسفاتاز) باشد. سیای۱۹-۹ (آنتیژن کربوهیدرات ۱۹٫۹) یک نشانگر تومور است که اغلب در سرطان لوزالمعده افزایش مییابد. با این حال، حساسیت و ویژگی ندارد، دستکم به این دلیل که ۵٪ از افراد فاقد آنتیژن لوئیس (a) هستند و نمیتوانند این آنتیژن تولید کنند. سیای۱۹-۹ حساسیت ۸۰ درصد و ویژگی ۷۳ درصد در تشخیص آدنوکارسینوم لوزالمعده دارد و بیشتر برای پیگیری موارد شناخته شده استفاده میشود؛ تا تشخیص بیماری.[۲][۱۲]
آسیبشناسی بافتی
شایعترین شکل سرطان لوزالمعده (آدنوکارسینوم) در زیر میکروسکوپ به صورت سلولهای غدهای تمایز نیافته یا نسبتاً تمایزیافته مشخص میشود. معمولاً دسموپلازی قابلتوجه، یا تشکیل یک استرومای فیبروز متراکم، یا بافت ساختاری متشکل از طیفی از انواع سلولها (شامل میوفیبروبلاستها، ماکروفاژها، لنفوسیتها و ماستسلها) و مواد تهنشین شده (مانند کلاژن نوع ۱ و هیالورونیک اسید) هم وجود دارد. این یک ریزمحیط تومور ایجاد میکند که دارای کمبود رگهای خونی (هیپوواسکولار) و در نتیجه کمبود اکسیژن (هیپوکسی تومور) است.[۲] اعتقاد بر آن است که این امر از رسیدن بسیاری از داروهای شیمیدرمانی به تومور جلوگیری میکند، و این یکی از دلایلی است درمان سرطان لوزالمعده را بهطور اخص سختتر میکند.[۲][۳]
| نوع سرطان | میزان بروز نسبی[۵۶] | یافتههای میکروسکوپی[۵۶] | ریزنگار | نشانگرهای ایمونوهیستوشیمی[۵۶] | ژنهای درگیر[۵۶] |
|---|---|---|---|---|---|
| آدنوکارسینوم مجرای لوزالمعده (PDAC) | ۹۰٪ | غدد و دسموپلازی | 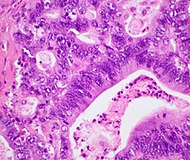 |
|
|
| کارسینوم سلول آسینار لوزالمعده (ACC) | ۱٪ تا ۲٪ | نمای دانهدانه و سنبادهمانند | 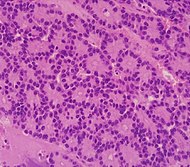
|
||
| تومور یکپارچه پاپیلاری کاذب | لانههای سلولی نامنسجم تومور که توسط نوارهای فیبری نازک احاطه شدهاند |  بزرگنمایی زیاد و کم[۵۷] |
|
| |
| کارسینوم آدنواسکوآموس | ۱٪ تا ۴٪[۵۸] | Cترکیبی از سلولهای غدهمانند و سلولهای بافت پوششی سنگفرشی |  |
حضورِ:
فقدانِ: |
|
| تومور نوراندوکرین لوزالمعده | ۵٪ | لانههای متعدد سلولی تومور | 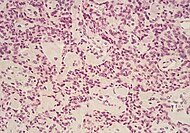 |
||
| ضایعه پیشسرطانی جهت مقایسه: | |||||
| پیشسرطانی: نئوپلاسم پاپیلاری موسینی داخل مجاری (IPMN) |
۳٪ | سلولهای اپیتلیایی موسینی.[۵۹] رشد درون مجاری لوزالمعده.[۶۰] | 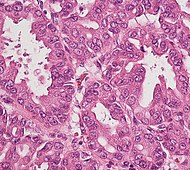
|
||
پیشگیری و غربالگری
جدای از سیگار نکشیدن، انجمن سرطان آمریکا حفظ وزن بدن در محدوده طبیعی و افزایش مصرف میوهها، سبزیجات و غلات کامل و در عین حال کاهش مصرف گوشت قرمز و گوشتهای فرآوریشده (مثل سوسیس و کالباس) را توصیه میکند، اگرچه هنوز شواهد متداومی وجود ندارد که نشان دهد این کار بهطور خاص از بروز سرطان لوزالمعده پیشگیری میکند یا میزان آن را کاهش میدهد.[۶۱] یک مقاله مروری در سال ۲۰۱۴ از پژوهشهای پیشین به این نتیجه رسید که شواهدی وجود دارد که مصرف مرکبات و کورکومین خطر ابتلا به سرطان لوزالمعده را کاهش میدهد، و همچنین مصرف غلات کامل، اسید فولیک، سلنیم و ماهیهای سرخنشده هم اثرات مفیدی در این زمینه دارند.[۴۷]
در جمعیت عمومی، غربالگری گروههای بزرگ مردم، مؤثر در نظر گرفته نمیشود و حتی ممکن است مضر باشد (مطابق آنچه تا سال ۲۰۱۹ میدانیم)،[۶۲] اگرچه تکنیکهای جدیدتر و غربالگری گروههای هدفمند در حال بررسی و ارزیابی هستند.[۶۳][۶۴] با این وجود، غربالگری منظم با سونوگرافی آندوسکوپی و تصویربرداری امآرآی/سیتیاسکن برای افرادی که در معرض خطر بالای سرطان لوزالمعده ارثی هستند، توصیه میشود.[۴][۶۵][۶۴][۶۶]
یک فراتحلیل در سال ۲۰۱۹ نشان داد که مصرف آسپرین ممکن است بروز سرطان لوزالمعده را کاهش دهد، اما هیچ ارتباط معنیداری با مرگومیر سرطان لوزالمعده یافت نشد.[۶۷]
مدیریت درمان
سرطانهای بخش برونریز
یکی از ارزیابی مهمی که پس از تشخیص بیماری انجام میشود آن است که آیا برداشتن تومور با جراحی امکانپذیر است یا خیر (به مرحلهبندی مراجعه کنید)، زیرا جراحی تنها راه درمان سرطان لوزالمعده است. اینکه آیا میتوان تومور را برداشت یا نه بستگی به میزان گسترش سرطان دارد. محل دقیق تومور نیز عامل مهمی است و سیتی اسکن میتواند نشان دهد که پیوستگی یا نزدیکی تومور با رگهای خونی اصلی که از نزدیک لوزالمعده عبور میکنند، چگونه است. سلامت عمومی فرد نیز باید مورد ارزیابی قرار گیرد، اگرچه سن بهخودی خود مانعی برای جراحی نیست.[۳]
شیمیدرمانی و تا حدی پرتودرمانی احتمالاً برای بیشتر مبتلایان پیشنهاد میشود، صرف نظر از اینکه جراحی امکانپذیر باشد یا خیر. متخصصان توصیه میکنند که مدیریت سرطان لوزالمعده باید با همکاری نزدیک یک تیم چندرشتهای شامل متخصصان در چندین حوزهٔ سرطانشناسی باشد و بنابراین بهتر است در مراکز بزرگتر و مجهزتر انجام شود.[۲][۳]
جراحی

جراحی با هدف درمان قطعی فقط در حدود یک پنجم (۲۰٪) موارد تازه تشخیصدادهشده امکانپذیر است.[۱۲] اگرچه سیتی اسکن جهت تصمیمگیری برای جراحی کمککننده است، اما در عمل، تشخیص اینکه آیا تومور را میتوان بهطور کامل برداشت («قابلیت برداشتن» آن) دشوار است، و ممکن است تنها در طی عمل جراحی مشخص شود که حذف موفقیتآمیز تومور بدون آسیب رساندن به سایر بافتهای حیاتی امکانپذیر نیست. اینکه برداشتن تومور با جراحی شدنی است یا خیر به عوامل مختلفی بستگی دارد، از جمله میزان دقیق مجاورت آناتومیکی موضعی تومور، یا درگیری عروق خونی وریدی یا شریانی[۲] و همچنین مهارت جراح و در نظر گرفتن دقیق میزان و چگونگی بهبودی پس از عمل و دوران نقاهت.[۶۸][۶۹] سنِ فرد بهخودی خود، دلیلی برای جراحی نکردن نیست، اما وضعیت کلی عملکرد بیمار باید برای یک چنین جراحی سنگینی مناسب باشد.[۱۲]
یکی از ویژگیهای خاصی که ارزیابی میشود، وجودِ یک لایه شفاف یا صفحهای از چربی است که مانعی بین تومور و عروق ایجاد میکند که اگر وجود داشته باشد دلگرمکننده است و اگر موجود نباشد، وضعیتی ناامیدکننده است.[۳] بهطور سنتی، ارزیابی نزدیکی تومور به رگهای وریدی یا شریانی اصلی، بر حسب «میزان مجاورت» (طبق تعریف تومور نباید با بیش از نیمی از محیط رگ خونی در تماس باشد؛ بدون اینکه توسط چربی جدا شده باشد)، «پوشش» (زمانی که تومور قسمت اعظم محیط رگ را در بر میگیرد)، یا درگیری کامل رگ انجام میشود.[۷۰]: 22 برداشتن بخشهایی از رگهای خونی ممکن است در برخی موارد امکانپذیر باشد،[۷۱][۷۲] بهویژه اگر درمان نئو-اَدجوانت اولیه امکانپذیر باشد،[۷۳][۷۴][۷۵] که با استفاده از شیمیدرمانی[۶۹][۷۰]: 36 [۷۶] و/یا پرتودرمانی[۷۰]: 29–30 صورت میپذیرد.
حتی زمانی که به نظر میرسد جراحی موفقیتآمیز بوده است، بررسی آسیبشناسی زیر میکروسکوپ نشان میدهد که سلولهای سرطانی اغلب در اطراف لبههای بافت برداشتهشده باقی ماندهاند (این کار همیشه انجام میشود)، و نشان میدهد سرطان بهطور کامل حذف نشده است.[۲] علاوه بر این، سلولهای بنیادی سرطانی معمولاً در بررسی میکروسکوپی قابل مشاهده نیستند و در صورت حضور، ممکن است به رشد و گسترش خود ادامه دهند.[۷۷][۷۸] بنابراین لاپاروسکوپی اکتشافی (یک روش جراحی سبک با هدایت دوربین) ممکن است برای به دست آوردن ارزیابی واضحتری از نتیجه یک عمل جراحیِ کامل انجام شود.[۷۹]

برای سرطانهایی که سر لوزالمعده را درگیر میکنند، روش جراحی ویپل رایجترین رویکرد روش جراحی با هدف درمان قطعی است. جراحی ویپل یک عمل جراحی سنگین و بزرگ است که شامل برداشتن سر لوزالمعده و منحنی دوازدهه با هم («پانکراتو-دئودنکتومی»)، ایجاد یک میانبُر (بایپَس) برای عبور غذا از معده به ژژونوم («گاسترو-ژژونوستومی») و اتصال یک حلقه از ژژونوم به مجرای صفراوی برای تخلیه صفرا («کُـلهسیستو-ژژنوستومی») است. این جراحی سنگین را تنها در صورتی میتوان انجام داد که فرد بتواند از یک چنین جراحی بزرگی جان سالم به در ببرد و سرطان بدون تهاجم به احشای موضعی یا متاستاز موضعی باشد؛ بنابراین، فقط در موارد اندکی قابل انجام است. سرطانهای دم لوزالمعده را میتوان با استفاده از روشی به نام «پانکراتکتومی دیستال» برداشت، که اغلب با برداشتن طحال همراه است.[۲][۳] امروزه اغلب میتوان این کار را با استفاده از روشهای کم تهاجمی لاپاروسکوپی انجام داد.[۲][۳]
اگرچه جراحی به قصد درمان قطعی، دیگر با نرخ بسیار بالای مرگومیر که تا دهه ۱۹۸۰ رایج بود همراه نیست، اما بخش زیادی از افراد (حدود ۳۰ تا ۴۵٪) همچنان میبایست برای عوارض پس از جراحی (که توسط خود سرطان ایجاد نمیشود)، درمان شوند. شایعترین عارضه این جراحی، اشکال در تخلیه معده است.[۳] برخی از روشهای جراحی محدودتر نیز ممکن است برای تسکین علائم بیمار، مورد استفاده قرار گیرند (به مراقبت تسکینی مراجعه کنید): به عنوان مثال، زمانی که سرطان به دوازدهه یا رودهٔ بزرگ زده باشد یا روی آنها فشار بیاورد. در چنین مواردی، جراحی بایپَـس ممکن است جلوی انسداد را بگیرد و کیفیت زندگی را بهبود بخشد، اما به هدف درمانِ قطعیِ سرطان انجام نمیشود.[۱۲]
شیمیدرمانی
یک تا دو ماه پس از جراحی، شیمیدرمانی کمکی (اَدجوانت) با جمسیتابین و فلوروراسیل در صورتی که فرد وضعیت عملکردی[ث][ج] مناسبی داشته باشد، قابل انجام است.[۴][۶۵] در افرادی که برای جراحیهای سنگین درمانی مناسب نیستند، ممکن است از شیمیدرمانی برای افزایش طول عمر یا بهبود کیفیت زندگی استفاده شود.[۳] گاهی پیش از جراحی، شیمیدرمانی نئو-ادجوانت یا پرتوشیمیدرمانی در تومورهایی که «قابل برداشت مرزی» هستند، در نظر گرفته میشود (به مرحلهبندی مراجعه کنید) تا اندازه تومور را به حدی برسد که انجام جراحی مقدور یا مفید باشد. در سایر موارد، انجام درمان نئو-ادجوانت مورد اختلافنظر است، زیرا جراحی را به تأخیر میاندازد.[۳][۴][۸۱]
سازمان غذا و داروی ایالات متحده آمریکا (FDA) بهدنبال اثبات بهبود کیفیت زندگی و افزایش ۵ هفتهای در میانگین مدت بقا در مبتلایان به سرطان لوزالمعده پیشرفته در یک کارآزمایی بالینی که جمسیتابین مصرف کرده بودند، این دارو را در سال ۱۹۹۷ تأیید کرد.[۸۲] جمسیتابین نخستین داروی شیمیدرمانی بود که توسط سازمان غذا و داروی آمریکا بر پایهٔ کارآزمایی بالینیای تأیید شد که هدف نهاییاش[چ] بهبود کیفیت زندگی (و نه بقای بیمار) بود.[۸۳] شیمیدرمانی با استفاده از جمسیتابین بهتنهایی، بهمدت حدود یک دهه استاندارد درمان دارویی سرطان لوزالمعده بود، زیرا تعدادی از کارآزماییهایی که آن را در ترکیب با سایر داروها آزمایش کردند، نتایج قابل توجهی بهتری را نشان ندادند. با این حال، امروزه مشخص شده است که ترکیب جمسیتابین با ارلوتینیب، نرخ بقای مبتلایان را به میزان متوسطی افزایش میدهد، و در نتیجه سازمان غذا و دارو در سال ۲۰۰۵ ارلوتینیب را جهت استفاده در سرطان لوزالمعده مورد پذیرش قرار داد.[۸۴]
رژیم شیمیدرمانی فولفیرناکس با استفاده از چهار دارو، موثرتر از جمسیتابین به تنهایی بود، اما با عوارض جانبی قابل توجهی همراه بود و بنابراین فقط در افرادی قابل انجام است که «وضعیت عملکردی» مناسبی دارند. این مسئله همچنین در مورد پاکلیتاکسل متصل به پروتئین،[ح] هم صادق است که سازمان غذا و دارو در سال ۲۰۱۳ به آن برای استفاده با جمسیتابین در سرطان لوزالمعده مجوز داد.[۸۵] تا پایان سال ۲۰۱۳، هر دو رژیم شیمیدرمانی مورد بحث همراه با جمسیتابین به عنوان گزینههای درمانی خوب در کسانی که قادر به تحمل عوارض جانبی بودند، در نظر گرفته شدند و جمسیتابین به تنهایی، یک گزینه مؤثر برای کسانی بود که اینگونه نبودند. یک کارآزمایی مقایسهای پایاپای بین دو گزینه جدید در حال انجام است و کارآزماییهای دیگری برای درمانهای متفاوت در دست اقدام است. با این حال، در چند سال اخیر تغییرات شکلگرفته در رژیمهای درمانی، تنها چند ماه زمان بقای بیمار را افزایش داده است.[۸۲] کارآزماییهای بالینی اغلب برای درمانهای اَدجوانت نوین انجام میشوند.[۴]
پرتودرمانی
نقش پرتودرمانی به عنوان یک درمان کمکی (اَدجوانت) پس از جراحی از دهه ۱۹۸۰ مورد بحث بوده است.[۳] در اوایل دهه ۲۰۰۰، «کارگروه مطالعاتی اروپا برای پژوهشهای سرطان لوزالمعده»[خ] برتری پیشآگهی شیمیدرمانی اَدجوانت را نسبت به پرتوشیمیدرمانی نشان داد.[۸۶][۸۷][۴] «انجمن آنکولوژی پزشکی اروپا» توصیه میکند که پرتودرمانی کمکی فقط برای افرادی که در کارآزماییهای بالینی شرکت کردهاند، استفاده شود.[۶۵] با این حال، تمایل مستمری در پزشکان آمریکایی در استفاده از رادیوتراپی اَدجوانت نسبت به پزشکان اروپایی دیده میشود. کارآزماییهای بالینی فراوانی، انواع مختلفی از ترکیبات درمانی را از دهه ۱۹۸۰ تا کنون آزمایش کردهاند که نتایج متناقضی دربرداشته است، اما نتوانستهاند این مشکل را بهطور قطعی حل کنند.[۳][۴]
گاهی هدف از پرتودرمانی، کوچک کردن تومور به اندازهای است که بتوان آن را با جراحی برداشت؛ اما استفاده از آن در تومورهای غیرقابل جراحی همچنان بحثبرانگیز است، چرا که نتایج متناقضی از کارآزماییهای بالینی بهدست آمده است. بهدنبال انتشار نتایج اولیهٔ یک کارآزمایی بالینی که در سال ۲۰۱۳ ارائه شد، تمایل برای استفاده از پرتودرمانی در درمان تومورهای پیشرفتهٔ موضعی «بهطور قابل توجهی کاهش یافت.»[۲]
تومورهای نوراندوکرین
درمان تومورهای نوراندوکرین، از جمله انواع بدخیم ناشایع، ممکن است رویکردهای گوناگونی را دربرگیرد.[۸۸][۸۹][۹۰][۹۱] برخی از تومورهای کوچک کمتر از ۱ سانتیمتر را که بهطور تصادفی شناسایی میشوند - مثلاً هنگام انجام سیتی اسکن بهمنظوری دیگر - میتوان با روش «انتظار همراه با مراقبت دقیق از بیمار»[د][ذ] زیر نظر داشت.[۸۸] اتخاذ این روش به خطر ارزیابیشده جراحی بستگی دارد که تحت تأثیر محل تومور و حضور سایر مشکلات همزمان پزشکی است.[۸۸] تومورهایی که تنها در داخل لوزالمعده قرار دارند (تومورهای موضعی) یا متاستاز محدود دارند (مثلاً به کبد)، ممکن است با جراحی برداشته شوند. نوع جراحی به محل تومور و میزان انتشار به غدد لنفاوی بستگی دارد.[۲۲]
برای تومورهای موضعی، جراحی محدودتری به نسبت جراحیهای مورد استفاده برای درمان آدنوکارسینوم پانکراس (که پیشتر در بالا شرح داده شد) انجام میشود، اما به غیر از این تفاوت، نحوه جراحی مشابه روشهای برداشتن تومورهای برونریز است. دامنه پیامدهای درمانی بسیار متفاوت است. برخی از انواع این تومورها پس از جراحی میزان بقای بسیار بالایی دارند در حالی که برخی دیگر پیشآگهی ضعیفی دارند. از آنجایی که همهٔ این گروه از تومورها نادر هستند، دستورالعملها کنونی تأکید دارند که درمان باید در یک مرکز تخصصی انجام شود.[۲۲][۲۹] پیوند کبد ممکن است در موارد خاصی از متاستاز کبدی در نظر گرفته شود.[۹۳]
برای تومورهای فعال، داروهای آنالوگ سوماتوستاتین، همچون اکترئتید، قادر به کاهش تولید بیش از حد هورمونها هستند.[۲۲] لانرئوتید هم قادر است رشد تومور را کند کند.[۹۴] اگر تومور علامتدار باشد و نتوان آن را با جراحی برداشت، درمان هدفمند با اورولیمس یا سانیتینیب گاهی به کاهش علائم و کند کردن پیشرفت بیماری کمک میکند.[۲۹][۹۵][۹۶] شیمیدرمانی سیتوتوکسیک استاندارد عموماً برای تومورهای نوراندوکرین چندان مؤثر نیست، اما ممکن است زمانی که سایر درمانهای دارویی در جلوگیری از پیشرفت بیماری شکست میخورند،[۲۹] یا در موردِ تومورهای نوراندوکرین با تمایز کم[ر] استفاده شود.[۹۷]
پزشکان در صورت وجود دردِ ناشی از گسترش آناتومیک سرطان، مثلاً متاستاز به استخوان، گاهی پرتودرمانی تجویز میکنند. برخی از تومورهای نوراندوکرین، پپتیدها یا هورمونهای خاصی را جذب میکنند و این تومورها ممکن است به درمان پزشکی هستهای با پپتیدهای نشاندارشده یا هورمونهایی مانند آیوبنگوان (ید-۱۳۱ یا MIBG) پاسخ دهند.[۹۸][۹۹][۱۰۰][۱۰۱] حذف با بسامد رادیویی، فرایند انجماد تومور[ز] و آمبولیزاسیون شریان کبدی[ژ] نیز گاهی مورد استفاده قرار میگیرند.[۱۰۲][۱۰۳]
مراقبتهای تسکینی
«مراقبتهای تسکینی»، مراقبتهای پزشکی-پرستاری هستند که بر مدیریت درمان و تسکین علائم برخی بیماریهای جدی مانند سرطان و بهبود کیفیت زندگی بیماران تمرکز دارند.[۱۰۴] از آنجا که آدنوکارسینوم پانکراس معمولاً در مراحل پیشرفته تشخیص داده میشود، مراقبتهای تسکینی اغلب تنها گزینهٔ درمانیِ موجود است.[۱۰۵]
مراقبت تسکینی بر درمانِ خودِ سرطان متمرکز نیست، بلکه هدفش تسکین علائمی مانند درد یا حالت تهوع بیمار است و به تصمیمگیری در نحوهٔ مدیریت درمان کمک میکند، از جمله اینکه آیا مراقبت از بیمار در «مرکز مراقبت از بیماران مراحل انتهایی»[س] مفید است یا خیر و اگر لازم است، اینکار در چه زمانی باید انجام شود.[۱۰۶] درد را میتوان با داروهایی مانند مواد افیونی یا از طریق مداخله عملکردی[ش] دیگر، مثلاً توسط بلاک عصبی روی شبکه سلیاک[ص] کنترل کرد. این عمل، کارکرد اعصاب منتقلکنندهٔ درد از شکم را دگرگون میکند یا بسته به روش مورد استفاده، بهکلی از بین میبرد. انسداد شبکه عصبی سلیاک یک روش ایمن و مؤثر برای کاهش درد است و بهطور کلی، نیاز به استفاده از مسکنهای مخدر را کاهش میدهد که دارای عوارض جانبی منفی قابل توجهی است.[۳][۱۰۷]
سایر علائم یا عوارضی که میتوان با جراحی تسکیندهنده درمان کرد، انسداد تومور روده یا انسداد مجرای صفراوی است. برای دومی که در بیش از نیمی از موارد اتفاق میافتد، ممکن است یک لوله فلزی کوچک به نام اِستِنت توسط آندوسکوپی کارگذاری شود تا مجاری صفراوی را باز نگه دارد.[۳۲] مراقبت تسکینی همچنین میتواند به درمان افسردگی که اغلب با تشخیص سرطان پانکراس همراه است، کمک کند.[۳]
هم جراحی و هم خودِ تومورهای پیشرفتهٔ غیرقابل جراحی، در بسیاری از موارد منجر به بروز اختلالات دستگاه گوارش انسان ناشی از کمبود فراورده برونریز لوزالمعده میشوند (نارسایی برونریز). اینها را میتوان با تجویز داروی «پانکراتین»[ض] درمان کرد که حاوی آنزیمهای صناعی لوزالمعده است و بهتر است همراه با غذا مصرف شود.[۱۲] اشکال در تخلیه معده (تأخیر در تخلیه معده) شایع است و ممکن است تبدیل به معضلی جدی شود که به بستری شدن بیمار در بیمارستان بینجامد. درمان این عارضه ممکن است با روشهای مختلفی صورت پذیرد، از جمله تخلیه معده با لولهگذاری بینی به معده و داروهایی به نام مهارکنندگان پمپ پروتونی یا آنتاگونیستهای گیرندهٔ H2، که هر دو تولید اسید معده را کاهش میدهند.[۱۲] از داروهایی چون متوکلوپرامید نیز میتوان برای تسریع تخلیه و پاکسازی محتویات معده استفاده کرد.
پیامدها
| مرحله بالینی | میزان بقای ۵ ساله در آمریکا (%) برای مواردی که مابین ۱۹۹۲–۱۹۹۸ تشخیص داده شدند | |
|---|---|---|
| سرطانهای بخش برونریز لوزالمعده | تومورهای نورواندوکرین که با جراحی درمان شدند | |
| IA / I | ۱۴ | ۶۱ |
| IB | ۱۲ | |
| IIA / II | ۷ | ۵۲ |
| IIB | ۵ | |
| III | ۳ | ۴۱ |
| IV | ۱ | ۱۶ |
آدنوکارسینوم لوزالمعده و سایر سرطانهایِ ناشایعِ بخش برونریز این غده، پیشآگهی بسیار ضعیفی دارند، زیرا معمولاً در مراحل پایانی تشخیص داده میشوند، یعنی هنگامی که سرطان به صورت موضعی پیشرفته کرده است یا به سایر قسمتهای بدن گسترش یافته است.[۲] پیامد بیماری در موردِ تومورهای نوراندوکرین بسیار بهتر است: بسیاری از آنها خوشخیم و کاملاً بدون علائم بالینی هستند، و حتی مواردی که با جراحی قابل درمان نیستند، میانگین بقای پنج ساله ۱۶٪ دارند،[۱۰۸] اگرچه چشمانداز بیماری به میزانِ قابل توجهی بسته به نوع تومور، متفاوت است.[۳۱]
برای آدنوکارسینوم لوزالمعده پیشرفته و متاستاتیک، که مجموعاً بیش از ۸۰ درصد موارد را نشان میدهند، کارآزماییهای متعددی که رژیمهای شیمیدرمانی را مقایسه میکنند، افزایش زمان بقا را نشان دادهاند، اما نه بیش از یک سال.[۲][۸۲] بهطور کلی بقای پنج ساله برای سرطان لوزالمعده در ایالات متحده از ۲٪ در موارد تشخیص داده شده در ۱۹۷۵–۱۹۷۷، و ۴٪ در تشخیصهای ۱۹۸۷–۱۹۸۹، به ۶٪ در ۲۰۰۳–۲۰۰۹ افزایش یافته است.[۱۰۹] در کمتر از ۲۰ درصد موارد آدنوکارسینوم لوزالمعده با تشخیص رشد موضعی سرطان و اندازهٔ کوچک (کمتر از ۲ سانتیمتر در مرحله T1)، حدود ۲۰ درصد آمریکاییها تا پنج سال زنده میمانند.[۱۹]
حدود ۱۵۰۰ ژن با پیشآگهی آدنوکارسینوم لوزالمعده مرتبط هستند. برخی از اینها ژنهای نامطلوب هستند، که بیان بیش از حدشان، به پیامد بد بیماری مربوط است، مثل گیرنده فاکتور رشد هپاتوسیت و MUC-1، و برخی دیگر ژنهای مطلوبند که بیان زیادشان با بقای بیشتر مبتلایان مرتبط است، مثل فاکتور رونویسی PELP-1.[۱۱۰][۱۱۱]
توزیع

در سال ۲۰۱۵، انواع سرطان لوزالمعده منجر به مرگ ۴۱۱٬۶۰۰ نفر در سراسر جهان شد.[۸] تخمین سال ۲۰۱۴، آن بود که ۴۶٬۰۰۰ نفر در ایالات متحده آمریکا به سرطان لوزالمعده مبتلا شوند و ۴۰٬۰۰۰ نفر آنها، بر اثر این سرطان جان خود را از دست بدهند.[۲] اگرچه سرطان لوزالمعده تنها ۲٫۵ درصد موارد جدید سرطانها را در کل تشکیل میدهد، اما این بیماری، مسئول ۶ درصد مرگومیر ناشی از سرطان در هر سال است.[۱۱۲] این بیماری هفتمین علت مرگ ناشی از سرطان در سراسر جهان،[۱۱] پنجمین علت شایع مرگ ناشی از سرطان در بریتانیا[۱۷] و سومین علت شایع در ایالات متحده آمریکا است.[۱۸]
در سطح جهانی، سرطان لوزالمعده یازدهمین سرطان شایع در زنان و دوازدهمین سرطان شایع در مردان است.[۱۱] اکثر موارد ثبتشده در کشورهای توسعهیافته رخ میدهد.[۱۱] میانگین خطر بروز این بیماری در شهروندان ایالات متحده در طول عمر حدود ۱ در ۶۷ (یا ۱٫۵٪) است،[۱۱۳] که کمی بیشتر از این رقم در بریتانیا است.[۱۱۴] این بیماری در مردان شایعتر از زنان است،[۲][۱۱] اگرچه این تفاوت جنسیتی در میزان بروز در دهههای اخیر کاهش یافته است، که احتمالاً نشاندهنده افزایش مصرف سیگار زنان در سنین پائین است. در ایالات متحده، خطر ابتلا برای آمریکاییهای آفریقاییتبار، بیش از ۵۰٪ بیشتر از سفیدپوستان است، اما این میزان در آفریقا و شرق آسیا بسیار کمتر از آمریکای شمالی یا اروپا است، ایالات متحده آمریکا، اروپای مرکزی و شرقی، و آرژانتین و اروگوئه همگی دارای نرخهای ابتلای زیادی هستند.[۱۱]
تومورهای نورواندوکرین
میزان بروز سالانه تومورهای نورواندوکرین لوزالمعده شناختهشده (PanNETs)، اندک است (حدود ۵ در هر یک میلیون نفر در سال) که غالباً از انواع غیرفعال (غیرترشحی) تومور هستند.[۲۶] حدود ۴۵٪ تا ۹۰٪ از تومورهای نورواندوکرین لوزالمعده از انواع غیرفعال هستند.[۲۲][۲۹] در بررسیهای کالبدگشایی در بسیاری از مواقع تومورهای نورواندوکرین کوچکی کشف میشود که نشان میدهد شیوع تومورهایی که بیاثر و بدون علامت باقی میمانند، ممکن است نسبتاً بالا باشد.[۲۹] بهطور کلی تصور میشود که تومورهای نورواندوکرین حدود ۱ تا ۲ درصد از کل تومورهای لوزالمعده را تشکیل دهند.[۲۶] تعریف و طبقهبندی تومورهای نورواندوکرین در طول زمان تغییر کرده و بر آنچه در مورد همهگیرشناسی و اثرات بالینی آنها میدانیم، تأثیر گذاشته است.[۱۱۵]
تاریخچه
شناخت و تشخیص
نخستین شناسایی و توصیف سرطان لوزالمعده به دانشمند ایتالیایی قرن هجدهم جووانی باتیستا مورگانی، پدر آسیبشناسی تشریحی امروزی، نسبت داده شده است که ادعا میکرد چندین مورد سرطان را در لوزالمعده ردیابی کرده است. با توجه به ظاهر مشابه آن به پانکراتیت، بسیاری از پزشکان قرن ۱۸ و ۱۹ در مورد وجود این بیماری تردید داشتند. چند گزارش موردی در دهههای ۱۸۲۰ و ۱۸۳۰ منتشر شد، و سرانجام یک تشخیص قطعی با آسیبشناسی بافتی توسط پزشک آمریکایی، جیکوب مندس دا کوستا ثبت شد که خودش در قابل اعتماد بودن توصیفهای مورگانی تردید داشت. سرانجام در آغاز قرن بیستم، سرطان سر لوزالمعده به یک تشخیص کاملاً مسلم و معتبر تبدیل شده بود.[۱۱۶]
در مورد تومورهای نوراندوکرین، احتمال سرطان سلولهای جزایر لانگرهانس نخستین بار در سال ۱۸۸۸ مطرح شد. نخستین مورد ترشح بیش از حد انسولین ناشی از تومورهای انسولینساز لوزالمعده در سال ۱۹۲۷ گزارش شد که آن را منسوب به جراحان آمریکایی، «رابرت میلتون زولینگر» و «اِدوین هومر الیسون» میدانند. این دو با فرض وجود تومور ترشحکننده گاسترین، دو مورد زخم گوارشی غیرمعمولِ شدید در سال ۱۹۵۵ گزارش کردند و پس از آن نامشان در بر روی سندرم زولینگر-الیسون ماندگار شد.[۱۱۶] در سال ۲۰۱۰، سازمان جهانی بهداشت توصیه کرد که PanNEts نیز به جای تومورهای «درونریز» به عنوان تومورهای «نورواندوکرین» شناخته شوند.[۲۸]
امروزه تومورهای کوچک پیشسرطانی در بسیاری از سرطانهای لوزالمعده با سرعت بسیار زیادی توسط تصویربرداری مدرن پزشکی قابل شناسایی است. یک نوع آن، نئوپلاسم پاپیلاری موسینی داخل مجاری (IPMN) نخستین بار توسط محققان ژاپنی در سال ۱۹۸۲ توصیف شد. مقالهای در سال ۲۰۱۰ اشاره کرد که: «تا یک دهه بعد، توجه کمی به این گزارش شد. اما طی ۱۵ سال آتی، یک انفجار نمادین در تشخیص این تومور شکل گرفت.»[۱۱۷]
جراحی
نخستین جراحی ویپل جزئی گزارششده توسط جراح ایتالیایی آلساندرو کودیویلا در سال ۱۸۹۸ انجام شد، اما بیمار ۱۸ روز بعد در اثر عوارض بعدِ عمل درگذشت. عملهای جراحی اولیه خطرناک و ناقص بودند؛ نخست بهدلیل باورهای اشتباه آن روزگار مبنی بر اینکه بیماران در صورت برداشتهشدن دوازدهه میمیرند و همچنین متوقف کردن جریان شیره لوزالمعده مرگبار است. بعدها، همچنین به اشتباه، فرض شد که میتوان مجرای پانکراس را به سادگی و بدون عوارض جانبی جدی بست. واقعیت آن است که اغلب موارد، مجرای بستهشده کمی بعد نشت میکند. در سالهای ۱۹۰۷ و ۱۹۰۸، پس از چند عمل ناموفق دیگر توسط جراحان دیگر، روشهای آزمایشی دیگری بر روی اجساد توسط جراحان فرانسوی صورت پذیرفت.
در سال ۱۹۱۲ جراح آلمانی والتر کائوش نخستین کسی بود که بخشهای بزرگی از دوازدهه و لوزالمعده را با هم برداشت. این جراحی در شهر برسلاو، (وروتسواف کنونی) در لهستان انجام شد. در سال ۱۹۱۸ با جراحی بر روی سگها ثابت شد که میتوان حتی پس از برداشتن کامل دوازدهه، زنده ماند، اما چنین عملی در جراحی انسان تا سال ۱۹۳۵ انجام نشد و در آن سال بود که جراح آمریکایی آلن اولدفادر ویپل نتایج مجموعه ای از سه عمل جراحی را که در بیمارستان نیویورک-پرسبیترین انجام شده بود، گزارش کرد. برداشت کاملِ دوازدهه فقط در یکی از بیماران انجام شده بود، اما او به مدت دو سال زنده ماند تا اینکه به دلیل متاستاز به کبد درگذشت.
جراحی نخست برنامهریزینشده بود، چرا که سرطان بیمار را روی تخت جراحی در اتاق عمل کشف کردند. موفقیت ویپل راهگشای پزشکان در آینده شد، اما این جراحی تا دهههای اخیر روشی دشوار و خطرناک باقی ماند. ویپل اصلاحات متعددی را برای روش جراحی خود منتشر کرد، از جمله نخستین برداشت کامل دوازدهه در سال ۱۹۴۰، اما او در مجموع تنها ۳۷ جراحی انجام داد.[۱۱۸]
در اواخر دهه ۱۹۳۰ میلادی، کشف این موضوع که ویتامین کا از خونریزی همراه با یرقان جلوگیری میکند، و توسعه روشهای انتقال خون به عنوان یک فرایند عادی و روزمره، هر دو میزان بقای بیمار پس از عمل جراحی ویپل را بهبود بخشیدند،[۱۱۸] اما تا اواخر دهه ۱۹۷۰ حدود ۲۵٪ از مبتلایان هرگز بیمارستان را زنده ترک نکردند.[۱۱۹] در دهه ۱۹۷۰، گروهی از جراحان آمریکایی نوشتند که این روش بسیار خطرناک است و باید کنار گذاشته شود. از آن زمان، نتایج در مراکز بزرگتر بهطور قابل توجهی بهبود یافته است، و مرگ و میر ناشی از این جراحی اغلب کمتر از ۴٪ است.[۲۴]
در سال ۲۰۰۶ گزارشی از مجموعه ای از ۱۰۰۰ جراحی ویپل متوالی توسط یک جراح از بیمارستان جانز هاپکینز بین سالهای ۱۹۶۹ تا ۲۰۰۳ منتشر شد. میزان این عملها در این دوره بهطور پیوسته افزایش یافته بود و تنها سه مورد از آنها پیش از سال ۱۹۸۰ جراحی شده بودند. میانگین زمان عمل از ۸٫۸ ساعت در دهه ۱۹۷۰ به ۵٫۵ ساعت در دهه ۲۰۰۰ کاهش یافت و مرگ و میر طی ۳۰ روز یا در بیمارستان تنها ۱٪ بود.[۱۱۸][۱۱۹] مجموعهای دیگر از ۲۰۵۰ جراحی در بیمارستان عمومی ماساچوست ما بین سالهای ۱۹۴۱ و ۲۰۱۱ تصویر مشابهی از بهبود را نشان داد.[۱۲۰]
برای تحقیق
تحقیقات جدید و در جریانِ سرطان لوزالمعده شامل مطالعات ژنتیکی و تشخیص زودهنگام، درمان در مراحل مختلف سرطان، استراتژیهای جراحی و درمانهای هدفمند مانند مهار فاکتورهای رشد، درمانهای مبتنی بر سیستم ایمنی و واکسنها هستند.[۱۲۱][۱۲۲][۱۲۳][۱۲۴][۱۲۵] برخی از بررسیهای جدید نشان میدهد اسیدهای صفراوی ممکن است در سرطانزایی سرطان لوزالمعده نقش داشته باشند.[۱۲۶]
همچنان سؤالها اساسی دربارهٔ زمان رخداد وقایع یا مرحلهبندی و پیشرفت بیماری به ویژه نقش ظهور دیابت،[۳۴][۱۲۷] و چگونگی و زمان گسترش بیماری وجود دارد.[۱۲۸] آگاهی از اینکه ابتلای قریب الوقع دیابت میتواند نشانه اولیه بیماری باشد، ممکن است تشخیص و پیشگیری به موقع از سرطان را، در صورت ایجاد یک استراتژی غربالگریِ قابل اجرا، تسهیل کند.[۳۴][۱۲۷][۱۲۹] بررسی کارآزمایی پیشنهادی مؤسسه ثبت پانکراتیت و سرطان لوزالمعده ارثی اروپا (EUROPAC) با هدف تعیین اینکه «آیا غربالگری منظم برای افرادی که سابقه خانوادگی این بیماری را دارند مناسب است یا خیر» نیز یکی از محورهای تحقیقاتی در این زمینه بهشمار میآید.[۱۳۰]
جایگزینی جراحی سوراخ کلید (لاپاراسکوپی) به جای جراحی ویپل، به ویژه از نظر زمان بهبودی، در حال ارزیابی است.[۱۳۱] الکتروپوریشن بازگشتناپذیر (IRE) نیز یک تکنیک اَبلاسیون نسبتاً جدید با پتانسیل کم کردن سرعت رشد سرطان و طولانیتر نمودن عمر افراد مبتلا به سرطانهای غیر متاستازی پیشرفته، بهویژه برای تومورهای مجاور عروق اطراف لوزالمعده بدون خطر ایجاد ترومای عروقی، است.[۱۳۲][۱۳۳]
تلاشهایی برای توسعه داروهای جدید، از جمله داروهایی که مکانیسمها و مسیرهای سوختوسازی را در شروع سرطان،[۱۳۴][۱۳۵] تکثیر سلولهای بنیادی،[۷۸] و رشد سلولی هدف قرار میدهند[۱۳۶][۱۳۷] و رویکرد خاصی از ایمونوتراپی که شامل استفاده از ویروسهای انکولیتیک برای هدف قرار دادن سلولهای سرطانی است، بخشی از آزمایشهای حوزه سرطان لوزالمعده را شامل میشود.[۱۳۸] مکانیسمهای خاص گالکتین در ریزمحیط تومور نیز در حال مطالعه هستند.[۱۳۹]
استفاده از نانوذرات بهجای رویکردهای دارویی معمول میتواند به انتقال هدفمند و پایدار یک رژیم دارویی به مکانهای خاص سرطان/تومور، بدون آسیب به سلولهای سالم بدن و ایجاد عوارض جانبی کلان بر بدن، کمک میکند.[۱۴۰]
جستارهای وابسته
یادداشتها
- ↑ Intraepithelial neoplasia
- ↑ intraductal papillary mucinous neoplasm
- ↑ pancreatic mucinous cystic neoplasm
- ↑ intraductal tubulopapillary neoplasm
- ↑ Performance status
- ↑ مقیاسی از میزان توانایی بیمار در انجام دادن وظایف عادی و فعالیتهای روزانه.[۸۰]
- ↑ clinical trial endpoint
- ↑ nab-paclitaxel
- ↑ European Study Group for Pancreatic Cancer Research (ESPAC)
- ↑ Watchful Waiting
- ↑ بهدقت زیر نظر گرفتن وضعیت بیمار بدون آنکه درمانی صورت گیرد؛ مگر آنکه علائمی ایجاد شود یا علائم موجود تغییر نمایند. این رویه گاهی در مورد بیماریهایی بهکار میرود که به کندی پیشرفت میکنند، و هنگامیکه خطرات درمان از فواید احتمالی حاصل از آن بیشتر باشد هم بهکار میرود.[۹۲]
- ↑ poorly differentiated PanNET
- ↑ Cryoablation
- ↑ Hepatic artery embolization
- ↑ Hospice
- ↑ procedural intervention
- ↑ Celiac plexus
- ↑ Pancreatin
منابع
- ↑ ۱٫۰ ۱٫۱ ۱٫۲ ۱٫۳ ۱٫۴ ۱٫۵ ۱٫۶ "Pancreatic Cancer Treatment (PDQ®) Patient Version". National Cancer Institute. National Institutes of Health. 17 April 2014. Archived from the original on 5 July 2014. Retrieved 8 June 2014.
- ↑ ۲٫۰۰ ۲٫۰۱ ۲٫۰۲ ۲٫۰۳ ۲٫۰۴ ۲٫۰۵ ۲٫۰۶ ۲٫۰۷ ۲٫۰۸ ۲٫۰۹ ۲٫۱۰ ۲٫۱۱ ۲٫۱۲ ۲٫۱۳ ۲٫۱۴ ۲٫۱۵ ۲٫۱۶ ۲٫۱۷ ۲٫۱۸ ۲٫۱۹ ۲٫۲۰ ۲٫۲۱ ۲٫۲۲ ۲٫۲۳ ۲٫۲۴ ۲٫۲۵ ۲٫۲۶ ۲٫۲۷ ۲٫۲۸ ۲٫۲۹ ۲٫۳۰ Ryan DP, Hong TS, Bardeesy N (September 2014). "Pancreatic adenocarcinoma". The New England Journal of Medicine. 371 (11): 1039–49. doi:10.1056/NEJMra1404198. PMID 25207767.
- ↑ ۳٫۰۰ ۳٫۰۱ ۳٫۰۲ ۳٫۰۳ ۳٫۰۴ ۳٫۰۵ ۳٫۰۶ ۳٫۰۷ ۳٫۰۸ ۳٫۰۹ ۳٫۱۰ ۳٫۱۱ ۳٫۱۲ ۳٫۱۳ ۳٫۱۴ ۳٫۱۵ ۳٫۱۶ ۳٫۱۷ ۳٫۱۸ ۳٫۱۹ ۳٫۲۰ ۳٫۲۱ ۳٫۲۲ ۳٫۲۳ ۳٫۲۴ ۳٫۲۵ ۳٫۲۶ ۳٫۲۷ ۳٫۲۸ ۳٫۲۹ ۳٫۳۰ ۳٫۳۱ Wolfgang CL, Herman JM, Laheru DA, Klein AP, Erdek MA, Fishman EK, Hruban RH (September 2013). "Recent progress in pancreatic cancer". CA: A Cancer Journal for Clinicians. 63 (5): 318–48. doi:10.3322/caac.21190. PMC 3769458. PMID 23856911.
- ↑ ۴٫۰۰ ۴٫۰۱ ۴٫۰۲ ۴٫۰۳ ۴٫۰۴ ۴٫۰۵ ۴٫۰۶ ۴٫۰۷ ۴٫۰۸ ۴٫۰۹ ۴٫۱۰ Vincent A, Herman J, Schulick R, Hruban RH, Goggins M (اوت 2011). "Pancreatic cancer" (PDF). Lancet. 378 (9791): 607–20. doi:10.1016/S0140-6736(10)62307-0. PMC 3062508. PMID 21620466. Archived from the original (PDF) on 12 January 2015.
- ↑ ۵٫۰ ۵٫۱ "Can pancreatic cancer be prevented?". American Cancer Society. 11 June 2014. Archived from the original on 13 November 2014. Retrieved 13 November 2014.
- ↑ ۶٫۰ ۶٫۱ "Five-Year Pancreatic Cancer Survival Rate Increases to 12%". PANCAN. 2023. Archived from the original on 4 March 2023. Retrieved 3 March 2023.
- ↑ Vos T, Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, et al. (GBD 2015 Disease and Injury Incidence and Prevalence Collaborators) (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ↑ ۸٫۰ ۸٫۱ ۸٫۲ Wang H, Naghavi M, Allen C, Barber RM, Bhutta ZA, Carter A, et al. (GBD 2015 Mortality and Causes of Death Collaborators) (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1459–1544. doi:10.1016/s0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ↑ "What Is Cancer? Defining Cancer". National Cancer Institute, National Institutes of Health. 7 March 2014. Archived from the original on 25 June 2014. Retrieved 5 December 2014.
- ↑ Unless otherwise specified in boxes, reference is: Pishvaian MJ, Brody JR (March 2017). "Therapeutic Implications of Molecular Subtyping for Pancreatic Cancer". Oncology. 31 (3): 159–66, 168. PMID 28299752.
- ↑ ۱۱٫۰۰ ۱۱٫۰۱ ۱۱٫۰۲ ۱۱٫۰۳ ۱۱٫۰۴ ۱۱٫۰۵ ۱۱٫۰۶ ۱۱٫۰۷ ۱۱٫۰۸ ۱۱٫۰۹ ۱۱٫۱۰ ۱۱٫۱۱ ۱۱٫۱۲ ۱۱٫۱۳ ۱۱٫۱۴ ۱۱٫۱۵ ۱۱٫۱۶ ۱۱٫۱۷ ۱۱٫۱۸ World Cancer Report. World Health Organization. 2014. Chapter 5.7. ISBN 978-92-832-0429-9.
- ↑ ۱۲٫۰۰ ۱۲٫۰۱ ۱۲٫۰۲ ۱۲٫۰۳ ۱۲٫۰۴ ۱۲٫۰۵ ۱۲٫۰۶ ۱۲٫۰۷ ۱۲٫۰۸ ۱۲٫۰۹ ۱۲٫۱۰ ۱۲٫۱۱ ۱۲٫۱۲ ۱۲٫۱۳ ۱۲٫۱۴ ۱۲٫۱۵ ۱۲٫۱۶ ۱۲٫۱۷ ۱۲٫۱۸ ۱۲٫۱۹ Bond-Smith G, Banga N, Hammond TM, Imber CJ (May 2012). "Pancreatic adenocarcinoma". BMJ. 344 (may16 1): e2476. doi:10.1136/bmj.e2476. PMID 22592847. S2CID 206894869.
- ↑ "Draft Recommendation Statement: Pancreatic Cancer: Screening". US Preventive Services Task Force. Retrieved 11 February 2019.
- ↑ Larsson, S. C.; Wolk, A. (2012). "Red and processed meat consumption and risk of pancreatic cancer: meta-analysis of prospective studies". British Journal of Cancer. 106 (3): 603–607. doi:10.1038/bjc.2011.585. PMC 3273353. PMID 22240790.
- ↑ Rohrmann, Sabine; et al. (2013). "Meat and fish consumption and risk of pancreatic cancer: Results from the European Prospective Investigation into Cancer and Nutrition". International Journal of Cancer. 132 (3): 617–624. doi:10.1002/ijc.27637. PMID 22610753. S2CID 2613568.
- ↑ Bardou M, Le Ray I (December 2013). "Treatment of pancreatic cancer: A narrative review of cost-effectiveness studies". Best Practice & Research Clinical Gastroenterology. 27 (6): 881–92. doi:10.1016/j.bpg.2013.09.006. PMID 24182608.
- ↑ ۱۷٫۰ ۱۷٫۱ "Cancer facts and figures – Why we exist". Pancreatic Cancer Research Fund. Retrieved 5 April 2019.
- ↑ ۱۸٫۰ ۱۸٫۱ "Pancreatic Cancer – Cancer Stat Facts". SEER (به انگلیسی). Retrieved 4 April 2019.
- ↑ ۱۹٫۰ ۱۹٫۱ "Pancreatic Cancer Treatment (PDQ®) Health Professional Version". National Cancer Institute. National Institutes of Health. 21 February 2014. Archived from the original on 22 October 2014. Retrieved 24 November 2014. "The highest cure rate occurs if the tumor is truly localized to the pancreas; however, this stage of disease accounts for less than 20% of cases. In cases with localized disease and small cancers (<2 cm) with no lymph-node metastases and no extension beyond the capsule of the pancreas, complete surgical resection is still associated with a low actuarial five-year survival rate of 18% to 24%."
- ↑ Wang Y, Miller FH, Chen ZE, Merrick L, Mortele KJ, Hoff FL; et al. (2011). "Diffusion-weighted MR imaging of solid and cystic lesions of the pancreas". Radiographics. 31 (3): E47-64. doi:10.1148/rg.313105174. PMID 21721197.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link). Diagram by Mikael Häggström, M.D. - ↑ Harris RE (2013). "Epidemiology of pancreatic cancer". Epidemiology of Chronic Disease. Jones & Bartlett. pp. 181–190. ISBN 978-0-7637-8047-0. Archived from the original on 24 June 2016.
- ↑ ۲۲٫۰ ۲۲٫۱ ۲۲٫۲ ۲۲٫۳ ۲۲٫۴ Öberg, K; Knigge, U; Kwekkeboom, D; Perren, A; et al. (ESMO Guidelines Working Group) (October 2012). "Neuroendocrine gastro-entero-pancreatic tumors: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Annals of Oncology. 23 Suppl 7 (suppl 7): vii124-30. doi:10.1093/annonc/mds295. PMID 22997445. (Table 5 outlines the proposed TNM staging system for PanNETs.)
- ↑ Handbook of Pancreatic Cancer. New York: Springer. 2009. p. 288. ISBN 978-0-387-77497-8. Archived from the original on 10 September 2017. Retrieved 12 June 2016.
- ↑ ۲۴٫۰ ۲۴٫۱ Govindan R (2011). DeVita, Hellman, and Rosenberg's Cancer: Cancer: Principles & Practice of Oncology (9th ed.). Lippincott Williams & Wilkins. Chapter 35: Cancer of the Pancreas: Surgical Management. ISBN 978-1-4511-0545-2. Online edition, with updates to 2014
- ↑ ۲۵٫۰ ۲۵٫۱ ۲۵٫۲ Tobias JS, Hochhauser D (2014). Cancer and its Management (7th ed.). John Wiley & Sons. p. 297. ISBN 978-1-118-46871-5.
- ↑ ۲۶٫۰ ۲۶٫۱ ۲۶٫۲ "Types of Pancreas Tumors". The Sol Goldman Pancreas Cancer Research Center. Johns Hopkins Medicine. 2012. Archived from the original on 8 October 2014. Retrieved 18 November 2014.
- ↑ Farrell JJ, Fernández-del Castillo C (June 2013). "Pancreatic cystic neoplasms: management and unanswered questions". Gastroenterology. 144 (6): 1303–15. doi:10.1053/j.gastro.2013.01.073. PMID 23622140.
- ↑ ۲۸٫۰ ۲۸٫۱ ۲۸٫۲ The PanNET denomination is in line with WHO guidelines for the classification of tumors of the digestive system "WHO classification of tumours of the digestive system – NLM Catalog – NCBI". Archived from the original on 9 September 2017. Retrieved 7 September 2017. published in 2010. Historically, PanNETs have also been referred to by a variety of terms, and are still commonly called "pancreatic endocrine tumors". See: Klimstra DS, Modlin IR, Coppola D, Lloyd RV, Suster S (August 2010). "The pathologic classification of neuroendocrine tumors: a review of nomenclature, grading, and staging systems". Pancreas. 39 (6): 707–12. doi:10.1097/MPA.0b013e3181ec124e. PMID 20664470. S2CID 3735444.
- ↑ ۲۹٫۰ ۲۹٫۱ ۲۹٫۲ ۲۹٫۳ ۲۹٫۴ ۲۹٫۵ ۲۹٫۶ ۲۹٫۷ Burns WR, Edil BH (March 2012). "Neuroendocrine pancreatic tumors: guidelines for management and update". Current Treatment Options in Oncology. 13 (1): 24–34. doi:10.1007/s11864-011-0172-2. PMID 22198808. S2CID 7329783.
- ↑ The Medical Subject Headings indexing system refers to "islet cell carcinoma", which is subdivided into gastrinoma, glucagonoma, somatostatinoma, and VIPoma. See: 2014 MeSH tree at "Pancreatic Neoplasms [C04.588.322.475]" بایگانیشده در ۱۹ مارس ۲۰۱۶ توسط Wayback Machine 16 October 2014
- ↑ ۳۱٫۰ ۳۱٫۱ "Islet Cell Tumors of the Pancreas / Endocrine Neoplasms of the Pancreas". The Sol Goldman Pancreas Cancer Research Center. Johns Hopkins Medicine. 2012. Archived from the original on 5 January 2015. Retrieved 5 January 2015.
- ↑ ۳۲٫۰ ۳۲٫۱ ۳۲٫۲ ۳۲٫۳ ۳۲٫۴ De La Cruz MS, Young AP, Ruffin MT (April 2014). "Diagnosis and management of pancreatic cancer". American Family Physician. 89 (8): 626–32. PMID 24784121.
- ↑ ۳۳٫۰ ۳۳٫۱ Alberts SR, Goldberg RM (2009). "Chapter 9: Gastrointestinal tract cancers". In Casciato DA, Territo MC (eds.). Manual of clinical oncology. Lippincott Williams & Wilkins. pp. 188–236. ISBN 978-0-7817-6884-9.
- ↑ ۳۴٫۰ ۳۴٫۱ ۳۴٫۲ Pannala R, Basu A, Petersen GM, Chari ST (January 2009). "New-onset diabetes: a potential clue to the early diagnosis of pancreatic cancer". The Lancet. Oncology. 10 (1): 88–95. doi:10.1016/S1470-2045(08)70337-1. PMC 2795483. PMID 19111249.
- ↑ "Chapter 15; Pancreas" (PDF). Manual for Staging of Cancer (2nd ed.). American Joint Committee on Cancer. pp. 95–98. Archived (PDF) from the original on 29 November 2014. See p. 95 for citation regarding "... lesser degree of involvement of bones and brain and other anatomical sites."
- ↑ Sperti C, Moletta L, Patanè G (October 2014). "Metastatic tumors to the pancreas: The role of surgery". World Journal of Gastrointestinal Oncology. 6 (10): 381–92. doi:10.4251/wjgo.v6.i10.381. PMC 4197429. PMID 25320654.
- ↑ "Causes of pancreatic cancer". NHS Choices. National Health Service, England. 7 October 2014. Archived from the original on 6 November 2014. Retrieved 5 December 2014.
- ↑ Anderson, Laura N.; Cotterchio, Michelle; Gallinger, Steven (5 February 2009). "Lifestyle, dietary, and medical history factors associated with pancreatic cancer risk in Ontario, Canada". Cancer Causes & Control. 20 (6): 825–34. doi:10.1007/s10552-009-9303-5. ISSN 0957-5243. PMC 3907069. PMID 19194662.
- ↑ Bosetti C, Lucenteforte E, Silverman DT, Petersen G, Bracci PM, Ji BT, et al. (July 2012). "Cigarette smoking and pancreatic cancer: an analysis from the International Pancreatic Cancer Case-Control Consortium (Panc4)". Annals of Oncology. 23 (7): 1880–88. doi:10.1093/annonc/mdr541. PMC 3387822. PMID 22104574.
- ↑ De Rubeis, Vanessa; Cotterchio, Michelle; Smith, Brendan T.; Griffith, Lauren E.; Borgida, Ayelet; Gallinger, Steven; Cleary, Sean; Anderson, Laura N. (1 September 2019). "Trajectories of body mass index, from adolescence to older adulthood, and pancreatic cancer risk; a population-based case–control study in Ontario, Canada". Cancer Causes & Control (به انگلیسی). 30 (9): 955–66. doi:10.1007/s10552-019-01197-9. ISSN 1573-7225. PMC 6685923. PMID 31230151.
- ↑ Peters ML, Tseng JF, Miksad RA (July 2016). "Genetic Testing in Pancreatic Ductal Adenocarcinoma: Implications for Prevention and Treatment". Clinical Therapeutics. 38 (7): 1622–35. doi:10.1016/j.clinthera.2016.03.006. PMID 27041411.
- ↑ ۴۲٫۰ ۴۲٫۱ Reznik R, Hendifar AE, Tuli R (2014). "Genetic determinants and potential therapeutic targets for pancreatic adenocarcinoma". Frontiers in Physiology. 5: 87. doi:10.3389/fphys.2014.00087. PMC 3939680. PMID 24624093.
- ↑ Greenhalf W, Grocock C, Harcus M, Neoptolemos J (May 2009). "Screening of high-risk families for pancreatic cancer". Pancreatology. 9 (3): 215–22. doi:10.1159/000210262. PMID 19349734. S2CID 29100310.
- ↑ Venturi, Sebastiano (January 2021). "Cesium in Biology, Pancreatic Cancer, and Controversy in High and Low Radiation Exposure Damage—Scientific, Environmental, Geopolitical, and Economic Aspects". International Journal of Environmental Research and Public Health (به انگلیسی). 18 (17): 8934. doi:10.3390/ijerph18178934. PMC 8431133. PMID 34501532.
 Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
- ↑ ۴۵٫۰ ۴۵٫۱ "Cancer Facts and Figures 2014" (PDF). American Cancer Society. Archived (PDF) from the original on 18 December 2014. Retrieved 5 January 2015., p. 19, "Though evidence is still accumulating, consumption of red or processed meat, or meat cooked at very high temperatures, may slightly increase risk."
- ↑ Larsson SC, Wolk A (ژانویه 2012). "Red and processed meat consumption and risk of pancreatic cancer: meta-analysis of prospective studies". British Journal of Cancer. 106 (3): 603–07. doi:10.1038/bjc.2011.585. PMC 3273353. PMID 22240790.
- ↑ ۴۷٫۰ ۴۷٫۱ Pericleous M, Rossi RE, Mandair D, Whyand T, Caplin ME (January 2014). "Nutrition and pancreatic cancer". Anticancer Research. 34 (1): 9–21. PMID 24403441.
- ↑ Hackeng WM, Hruban RH, Offerhaus GJ, Brosens LA (2016). "Surgical and molecular pathology of pancreatic neoplasms". Diagn Pathol. 11 (1): 47. doi:10.1186/s13000-016-0497-z. PMC 4897815. PMID 27267993.
{{cite journal}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) (distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/)), Image title and optimization: Mikael Häggström, M.D. - ↑ Delpu Y, Hanoun N, Lulka H, Sicard F, Selves J, Buscail L, et al. (March 2011). "Genetic and epigenetic alterations in pancreatic carcinogenesis". Current Genomics. 12 (1): 15–24. doi:10.2174/138920211794520132. PMC 3129039. PMID 21886451.
- ↑ Rooney SL, Shi J (October 2016). "Intraductal Tubulopapillary Neoplasm of the Pancreas: An Update From a Pathologist's Perspective". Archives of Pathology & Laboratory Medicine. 140 (10): 1068–73. doi:10.5858/arpa.2016-0207-RA. PMID 27684978.
- ↑ "The human pathology proteome in pancreatic cancer – The Human Protein Atlas". www.proteinatlas.org. Retrieved 28 September 2017.
- ↑ Uhlen M, Zhang C, Lee S, Sjöstedt E, Fagerberg L, Bidkhori G, et al. (August 2017). "A pathology atlas of the human cancer transcriptome". Science. 357 (6352): eaan2507. doi:10.1126/science.aan2507. PMID 28818916.
- ↑ Lewis MA, Yao JC (February 2014). "Molecular pathology and genetics of gastrointestinal neuroendocrine tumours". Current Opinion in Endocrinology, Diabetes and Obesity. 21 (1): 22–27. doi:10.1097/MED.0000000000000033. PMID 24310147. S2CID 31094880.
- ↑ Thakker RV, Newey PJ, Walls GV, Bilezikian J, Dralle H, Ebeling PR, et al. (September 2012). "Clinical practice guidelines for multiple endocrine neoplasia type 1 (MEN1)". The Journal of Clinical Endocrinology and Metabolism. 97 (9): 2990–3011. doi:10.1210/jc.2012-1230. PMID 22723327.
- ↑ Fitzgerald JE, White MJ, Lobo DN (April 2009). "Courvoisier's gallbladder: law or sign?". World Journal of Surgery. 33 (4): 886–91. doi:10.1007/s00268-008-9908-y. PMID 19190960. S2CID 21799234.
- ↑ ۵۶٫۰ ۵۶٫۱ ۵۶٫۲ ۵۶٫۳ Unless otherwise specified in boxes, reference is: Pishvaian MJ, Brody JR (March 2017). "Therapeutic Implications of Molecular Subtyping for Pancreatic Cancer". Oncology. 31 (3): 159–66, 168. PMID 28299752.
- ↑ ۵۷٫۰ ۵۷٫۱ ۵۷٫۲ ۵۷٫۳ Image by Mikael Häggström, MD.
Reference for features: Pooja Navale, M.D., Omid Savari, M.D., Joseph F. Tomashefski, Jr., M.D., Monika Vyas, M.D. "Solid pseudopapillary neoplasm".{{cite web}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) Last author update: 4 March 2022 - ↑ Skafida E, Grammatoglou X, Glava C, Zissis D, Paschalidis N, Katsamagkou E, et al. (February 2010). "Adenosquamous carcinoma of the pancreas: a case report". Cases Journal. 3 (1): 41. doi:10.1186/1757-1626-3-41. PMC 2825199. PMID 20205828.
- ↑ Diana Agostini-Vulaj. "Pancreas – Exocrine tumors / carcinomas – Intraductal papillary mucinous neoplasm (IPMN)". Pathology Outlines. Topic Completed: 1 July 2018. Revised: 9 March 2020
- ↑ Adsay V, Mino-Kenudson M, Furukawa T, Basturk O, Zamboni G, Marchegiani G, et al. (January 2016). "Pathologic Evaluation and Reporting of Intraductal Papillary Mucinous Neoplasms of the Pancreas and Other Tumoral Intraepithelial Neoplasms of Pancreatobiliary Tract: Recommendations of Verona Consensus Meeting". Annals of Surgery. 263 (1): 162–77. doi:10.1097/SLA.0000000000001173. PMC 4568174. PMID 25775066.
- ↑ "Diet and activity factors that affect risks for certain cancers: Pancreatic cancer section". American Cancer Society. 20 August 2012. Archived from the original on 4 November 2014. Retrieved 4 November 2014.
- ↑ Owens DK, Davidson KW, Krist AH, Barry MJ, Cabana M, Caughey AB, et al. (August 2019). "Screening for Pancreatic Cancer: US Preventive Services Task Force Reaffirmation Recommendation Statement". JAMA. 322 (5): 438–44. doi:10.1001/jama.2019.10232. PMID 31386141.
- ↑ He XY, Yuan YZ (August 2014). "Advances in pancreatic cancer research: moving towards early detection". World Journal of Gastroenterology. 20 (32): 11241–48. doi:10.3748/wjg.v20.i32.11241. PMC 4145762. PMID 25170208.
- ↑ ۶۴٫۰ ۶۴٫۱ Okano K, Suzuki Y (August 2014). "Strategies for early detection of resectable pancreatic cancer". World Journal of Gastroenterology. 20 (32): 11230–40. doi:10.3748/wjg.v20.i32.11230. PMC 4145761. PMID 25170207.
- ↑ ۶۵٫۰ ۶۵٫۱ ۶۵٫۲ Seufferlein T, Bachet JB, Van Cutsem E, Rougier P (October 2012). "Pancreatic adenocarcinoma: ESMO-ESDO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Annals of Oncology. 23 (Suppl 7): vii33–40. doi:10.1093/annonc/mds224. PMID 22997452.
- ↑ Goggins M, Overbeek KA, Brand R, Syngal S, Del Chiaro M, Bartsch DK, et al. (January 2020). "Management of patients with increased risk for familial pancreatic cancer: updated recommendations from the International Cancer of the Pancreas Screening (CAPS) Consortium". Gut. 69 (1): 7–17. doi:10.1136/gutjnl-2019-319352. PMC 7295005. PMID 31672839.
- ↑ Sun, J.; Li, Y.; Liu, L.; Jiang, Z.; Liu, G. (2019). "Aspirin use and pancreatic cancer risk: A systematic review of observational studies - PubMed". Medicine. 98 (51): e18033. doi:10.1097/MD.0000000000018033. PMC 6940047. PMID 31860953.
- ↑ Gurusamy KS, Kumar S, Davidson BR, Fusai G (February 2014). "Resection versus other treatments for locally advanced pancreatic cancer". The Cochrane Database of Systematic Reviews. 2 (2): CD010244. doi:10.1002/14651858.CD010244.pub2. PMID 24578248.
- ↑ ۶۹٫۰ ۶۹٫۱ Mollberg N, Rahbari NN, Koch M, Hartwig W, Hoeger Y, Büchler MW, Weitz J (December 2011). "Arterial resection during pancreatectomy for pancreatic cancer: a systematic review and meta-analysis". Annals of Surgery. 254 (6): 882–93. doi:10.1097/SLA.0b013e31823ac299. PMID 22064622. S2CID 42685174.
- ↑ ۷۰٫۰ ۷۰٫۱ ۷۰٫۲ "Pancreatic adenocarcinoma. NCCN Guidelines Version 1.2015" (PDF). NCCN Guidelines. National Comprehensive Cancer Network, Inc. 4 December 2014. Retrieved 26 December 2014.
- ↑ Alamo JM, Marín LM, Suarez G, Bernal C, Serrano J, Barrera L, et al. (October 2014). "Improving outcomes in pancreatic cancer: key points in perioperative management". World Journal of Gastroenterology. 20 (39): 14237–45. doi:10.3748/wjg.v20.i39.14237. PMC 4202352. PMID 25339810.
- ↑ Lopez NE, Prendergast C, Lowy AM (August 2014). "Borderline resectable pancreatic cancer: definitions and management". World Journal of Gastroenterology. 20 (31): 10740–51. doi:10.3748/wjg.v20.i31.10740. PMC 4138454. PMID 25152577.
- ↑ Polistina F, Di Natale G, Bonciarelli G, Ambrosino G, Frego M (July 2014). "Neoadjuvant strategies for pancreatic cancer". World Journal of Gastroenterology. 20 (28): 9374–83. doi:10.3748/wjg.v20.i28.9374 (inactive 31 January 2024). PMC 4110569. PMID 25071332.
{{cite journal}}: CS1 maint: DOI inactive as of ژانویه 2024 (link) - ↑ Gillen S, Schuster T, Meyer Zum Büschenfelde C, Friess H, Kleeff J (April 2010). "Preoperative/neoadjuvant therapy in pancreatic cancer: a systematic review and meta-analysis of response and resection percentages". PLOS Medicine. 7 (4): e1000267. doi:10.1371/journal.pmed.1000267. PMC 2857873. PMID 20422030.
- ↑ Christians KK, Evans DB (June 2015). "Additional support for neoadjuvant therapy in the management of pancreatic cancer". Annals of Surgical Oncology. 22 (6): 1755–58. doi:10.1245/s10434-014-4307-0. PMID 25519932.
- ↑ Tsvetkova EV, Asmis TR (August 2014). "Role of neoadjuvant therapy in the management of pancreatic cancer: is the era of biomarker-directed therapy here?". Current Oncology. 21 (4): e650–7. doi:10.3747/co.21.2006. PMC 4117630. PMID 25089113.
- ↑ Zhan HX, Xu JW, Wu D, Zhang TP, Hu SY (February 2015). "Pancreatic cancer stem cells: new insight into a stubborn disease". Cancer Letters. 357 (2): 429–37. doi:10.1016/j.canlet.2014.12.004. PMID 25499079.
- ↑ ۷۸٫۰ ۷۸٫۱ Tanase CP, Neagu AI, Necula LG, Mambet C, Enciu AM, Calenic B, et al. (August 2014). "Cancer stem cells: involvement in pancreatic cancer pathogenesis and perspectives on cancer therapeutics". World Journal of Gastroenterology. 20 (31): 10790–801. doi:10.3748/wjg.v20.i31.10790. PMC 4138459. PMID 25152582.
- ↑ Allen VB, Gurusamy KS, Takwoingi Y, Kalia A, Davidson BR (July 2016). "Diagnostic accuracy of laparoscopy following computed tomography (CT) scanning for assessing the resectability with curative intent in pancreatic and periampullary cancer". The Cochrane Database of Systematic Reviews. 2016 (7): CD009323. doi:10.1002/14651858.CD009323.pub3. PMC 6458011. PMID 27383694.
- ↑ «واژهنامه سرطان». موسسه تحقیقات، درمان و آموزش سرطان (مرکز جامع سرطان، دانشگاه علوم پزشکی تهران).
- ↑ Heinemann V, Haas M, Boeck S (October 2013). "Neoadjuvant treatment of borderline resectable and non-resectable pancreatic cancer". Annals of Oncology. 24 (10): 2484–92. doi:10.1093/annonc/mdt239. PMID 23852311.
- ↑ ۸۲٫۰ ۸۲٫۱ ۸۲٫۲ Thota R, Pauff JM, Berlin JD (January 2014). "Treatment of metastatic pancreatic adenocarcinoma: a review". Oncology. 28 (1): 70–74. PMID 24683721.
- ↑ Ryan DP (8 ژوئیه 2014). "Chemotherapy for advanced exocrine pancreatic cancer: Topic 2475, Version 46.0" (subscription required). UpToDate. Wolters Kluwer Health. Archived from the original on 8 December 2014. Retrieved 18 November 2014.
- ↑ "Cancer Drug Information: FDA Approval for Erlotinib Hydrochloride". National Cancer Institute. National Institutes of Health. 3 ژوئیه 2013. Archived from the original on 29 November 2014. Retrieved 5 December 2014.
- ↑ Borazanci E, Von Hoff DD (September 2014). "Nab-paclitaxel and gemcitabine for the treatment of patients with metastatic pancreatic cancer". Expert Review of Gastroenterology & Hepatology. 8 (7): 739–47. doi:10.1586/17474124.2014.925799. PMID 24882381. S2CID 31633898.
- ↑ Neoptolemos, Jp; Dunn, Ja; Stocken, Dd; Almond, J; Link, K; Beger, H; Bassi, C; Falconi, M; Pederzoli, P; Dervenis, C; Fernandez-Cruz, L (November 2001). "Adjuvant chemoradiotherapy and chemotherapy in resectable pancreatic cancer: a randomised controlled trial". The Lancet (به انگلیسی). 358 (9293): 1576–1585. doi:10.1016/S0140-6736(01)06651-X. PMID 11716884. S2CID 23803289.
- ↑ Neoptolemos, John P.; Stocken, Deborah D.; Friess, Helmut; Bassi, Claudio; Dunn, Janet A.; Hickey, Helen; Beger, Hans; Fernandez-Cruz, Laureano; Dervenis, Christos; Lacaine, François; Falconi, Massimo (2004-03-18). "A Randomized Trial of Chemoradiotherapy and Chemotherapy after Resection of Pancreatic Cancer". New England Journal of Medicine (به انگلیسی). 350 (12): 1200–1210. doi:10.1056/NEJMoa032295. ISSN 0028-4793. PMID 15028824.
- ↑ ۸۸٫۰ ۸۸٫۱ ۸۸٫۲ "Neuroendocrine tumors, NCCN Guidelines Version 1.2015" (PDF). National Comprehensive Cancer Network, Inc. NCCN). 11 November 2014. Retrieved 25 December 2014.
- ↑ Falconi M, Bartsch DK, Eriksson B, Klöppel G, Lopes JM, O'Connor JM, et al. (2012). "ENETS Consensus Guidelines for the management of patients with digestive neuroendocrine neoplasms of the digestive system: well-differentiated pancreatic non-functioning tumors". Neuroendocrinology. 95 (2): 120–34. doi:10.1159/000335587. PMID 22261872. S2CID 6985904.
- ↑ Jensen RT, Cadiot G, Brandi ML, de Herder WW, Kaltsas G, Komminoth P, et al. (2012). "ENETS Consensus Guidelines for the management of patients with digestive neuroendocrine neoplasms: functional pancreatic endocrine tumor syndromes". Neuroendocrinology. 95 (2): 98–119. doi:10.1159/000335591. PMC 3701449. PMID 22261919.
- ↑ Pavel M, Baudin E, Couvelard A, Krenning E, Öberg K, Steinmüller T, et al. (2012). "ENETS Consensus Guidelines for the management of patients with liver and other distant metastases from neuroendocrine neoplasms of foregut, midgut, hindgut, and unknown primary". Neuroendocrinology. 95 (2): 157–76. doi:10.1159/000335597. PMID 22262022. S2CID 2097604.
- ↑ «واژهنامه سرطان». موسسه تحقیقات، درمان و آموزش سرطان (مرکز جامع سرطان، دانشگاه علوم پزشکی تهران).
- ↑ Rossi RE, Massironi S, Conte D, Peracchi M (January 2014). "Therapy for metastatic pancreatic neuroendocrine tumors". Annals of Translational Medicine. 2 (1): 8. doi:10.3978/j.issn.2305-5839.2013.03.01. PMC 4200651. PMID 25332984.
- ↑ Nick Mulcahy (17 December 2014). "FDA Approves Lanreotide for Neuroendocrine Tumors". Medscape Medical News. WebMD LLC. Archived from the original on 18 January 2015. Retrieved 25 December 2014.
- ↑ Everolimus Approved for Pancreatic Neuroendocrine Tumors بایگانیشده در ۱۶ ژوئیه ۲۰۱۶ توسط Wayback Machine The ASCO Post. 15 May 2011, Volume 2, Issue 8
- ↑ National Cancer Institute. Cancer Drug Information. FDA Approval for Sunitinib Malate بایگانیشده در ۵ ژانویه ۲۰۱۵ توسط Wayback Machine. Pancreatic Neuroendocrine Tumors
- ↑ Text is available electronically (but may require free registration) See: Benson AB, Myerson RJ, Sasson AR (2010). Pancreatic, neuroendocrine GI, and adrenal cancers. Cancer Management: A Multidisciplinary Approach (13th ed.). UBM Medica. ISBN 978-0-615-41824-7. Archived from the original on 15 May 2011.
- ↑ Gulenchyn KY, Yao X, Asa SL, Singh S, Law C (May 2012). "Radionuclide therapy in neuroendocrine tumours: a systematic review". Clinical Oncology. 24 (4): 294–308. doi:10.1016/j.clon.2011.12.003. PMID 22221516.
- ↑ Vinik AI (November 2014). "Advances in diagnosis and treatment of pancreatic neuroendocrine tumors". Endocrine Practice. 20 (11): 1222–30. doi:10.4158/EP14373.RA. PMID 25297671.
- ↑ Kwekkeboom DJ, de Herder WW, van Eijck CH, Kam BL, van Essen M, Teunissen JJ, Krenning EP (March 2010). "Peptide receptor radionuclide therapy in patients with gastroenteropancreatic neuroendocrine tumors". Seminars in Nuclear Medicine. 40 (2): 78–88. doi:10.1053/j.semnuclmed.2009.10.004. PMID 20113677.
- ↑ Bodei L, Cremonesi M, Kidd M, Grana CM, Severi S, Modlin IM, Paganelli G (August 2014). "Peptide receptor radionuclide therapy for advanced neuroendocrine tumors". Thoracic Surgery Clinics. 24 (3): 333–49. doi:10.1016/j.thorsurg.2014.04.005. hdl:11392/2378236. PMID 25065935.
- ↑ Castellano D, Grande E, Valle J, Capdevila J, Reidy-Lagunes D, O'Connor JM, Raymond E (June 2015). "Expert consensus for the management of advanced or metastatic pancreatic neuroendocrine and carcinoid tumors". Cancer Chemotherapy and Pharmacology. 75 (6): 1099–114. doi:10.1007/s00280-014-2642-2. PMID 25480314. S2CID 39434924.
- ↑ Singh S, Dey C, Kennecke H, Kocha W, Maroun J, Metrakos P, et al. (August 2015). "Consensus Recommendations for the Diagnosis and Management of Pancreatic Neuroendocrine Tumors: Guidelines from a Canadian National Expert Group". Annals of Surgical Oncology. 22 (8): 2685–99. doi:10.1245/s10434-014-4145-0. PMID 25366583. S2CID 8129133.
- ↑ "Palliative or Supportive Care". American Cancer Society. 2014. Archived from the original on 21 August 2014. Retrieved 20 August 2014.
- ↑ Buanes TA (August 2014). "Pancreatic cancer-improved care achievable". World Journal of Gastroenterology. 20 (30): 10405–18. doi:10.3748/wjg.v20.i30.10405. PMC 4130847. PMID 25132756.
- ↑ "If treatment for pancreatic cancer stops working". American Cancer Society. 11 June 2014. Archived from the original on 22 October 2014. Retrieved 20 August 2014.
- ↑ Arcidiacono PG, Calori G, Carrara S, McNicol ED, Testoni PA (March 2011). Arcidiacono PG (ed.). "Celiac plexus block for pancreatic cancer pain in adults". The Cochrane Database of Systematic Reviews. 2019 (3): CD007519. doi:10.1002/14651858.CD007519.pub2. PMC 6464722. PMID 21412903.
- ↑ ۱۰۸٫۰ ۱۰۸٫۱ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامcancer.orgوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ "Cancer Facts and Figures 2014" (PDF). American Cancer Society. Archived (PDF) from the original on 18 December 2014. Retrieved 5 January 2015., Table, p. 18, rates adjusted for normal life expectancy
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامproteinatlas.orgوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامUhlen eaan2507وارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Jemal A, Siegel R, Ward E, Murray T, Xu J, Thun MJ (2007). "Cancer statistics, 2007". CA: A Cancer Journal for Clinicians. 57 (1): 43–66. doi:10.3322/canjclin.57.1.43. PMID 17237035. S2CID 22305510.
- ↑ "What are the key statistics about pancreatic cancer?". American Cancer Society. 11 June 2014. Archived from the original on 11 November 2014. Retrieved 11 November 2014.
- ↑ "Pancreatic cancer statistics". Cancer Research UK. Archived from the original on 18 December 2014. Retrieved 18 December 2014.; "In 2010, in the UK, the lifetime risk of developing pancreatic cancer is 1 in 73 for men and 1 in 74 for women", noting "The lifetime risk ... has been calculated ... using the 'Current Probability' method; this is a different method used from most other cancer sites since the possibility of having more than one diagnosis of pancreatic cancer over the course of their lifetime is very low"
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامLewis2014وارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ ۱۱۶٫۰ ۱۱۶٫۱ Busnardo AC, DiDio LJ, Tidrick RT, Thomford NR (November 1983). "History of the pancreas". American Journal of Surgery. 146 (5): 539–50. doi:10.1016/0002-9610(83)90286-6. PMID 6356946.
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامSilberman2010وارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ ۱۱۸٫۰ ۱۱۸٫۱ ۱۱۸٫۲ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامHistoryوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ ۱۱۹٫۰ ۱۱۹٫۱ Cameron JL, Riall TS, Coleman J, Belcher KA (July 2006). "One thousand consecutive pancreaticoduodenectomies". Annals of Surgery. 244 (1): 10–5. doi:10.1097/01.sla.0000217673.04165.ea. PMC 1570590. PMID 16794383.
- ↑ Fernández-del Castillo C, Morales-Oyarvide V, McGrath D, Wargo JA, Ferrone CR, Thayer SP, et al. (September 2012). "Evolution of the Whipple procedure at the Massachusetts General Hospital". Surgery. 152 (3 Suppl 1): S56-63. doi:10.1016/j.surg.2012.05.022. PMC 3806095. PMID 22770961.
- ↑ Reznik R, Hendifar AE, Tuli R (2014). "Genetic determinants and potential therapeutic targets for pancreatic adenocarcinoma". Frontiers in Physiology. 5: 87. doi:10.3389/fphys.2014.00087. PMC 3939680. PMID 24624093.
- ↑ "Pancreatic cancer research". Cancer Research UK. Archived from the original on 18 February 2014. Retrieved 17 July 2014.
- ↑ "Australian Pancreatic Genome Initiative". Garvan Institute. Archived from the original on 26 July 2014. Retrieved 17 July 2014.
- ↑ Biankin AV, Waddell N, Kassahn KS, Gingras MC, Muthuswamy LB, Johns AL, et al. (November 2012). "Pancreatic cancer genomes reveal aberrations in axon guidance pathway genes". Nature. 491 (7424): 399–405. Bibcode:2012Natur.491..399.. doi:10.1038/nature11547. PMC 3530898. PMID 23103869.
- ↑ "What's new in pancreatic cancer research and treatment?". American Cancer Society. 2019. Retrieved 2 May 2019.
- ↑ Feng, Hui-Yi; Chen, Yang-Chao (2016-09-07). "Role of bile acids in carcinogenesis of pancreatic cancer: An old topic with new perspective". World Journal of Gastroenterology. 22 (33): 7463–7477. doi:10.3748/wjg.v22.i33.7463. ISSN 1007-9327. PMC 5011662. PMID 27672269.
- ↑ ۱۲۷٫۰ ۱۲۷٫۱ "What's new in pancreatic cancer research and treatment?". American Cancer Society. 2019. Retrieved 2 May 2019.
- ↑ Graham JS, Jamieson NB, Rulach R, Grimmond SM, Chang DK, Biankin AV (September 2015). "Pancreatic cancer genomics: where can the science take us?". Clinical Genetics. 88 (3): 213–9. doi:10.1111/cge.12536. PMID 25388820. S2CID 26414866.
- ↑ Bruenderman EH, Martin RC (March 2015). "High-risk population in sporadic pancreatic adenocarcinoma: guidelines for screening". The Journal of Surgical Research. 194 (1): 212–9. doi:10.1016/j.jss.2014.06.046. PMC 4559279. PMID 25479908.
- ↑ "About EUROPAC". European Registry of Hereditary Pancreatitis and Familial Pancreatic Cancer (EUROPAC). University of Liverpool. Archived from the original on 26 July 2014. Retrieved 17 July 2014.
- ↑ Subar D, Gobardhan PD, Gayet B (February 2014). "Laparoscopic pancreatic surgery: An overview of the literature and experiences of a single center". Best Practice & Research. Clinical Gastroenterology. 28 (1): 123–32. doi:10.1016/j.bpg.2013.11.011. PMID 24485260.
- ↑ Weiss MJ, Wolfgang CL (2013). "Irreversible electroporation: a novel pancreatic cancer therapy". Current Problems in Cancer. 37 (5): 262–5. doi:10.1016/j.currproblcancer.2013.10.002. PMID 24331180. S2CID 3137300.
- ↑ Moir J, White SA, French JJ, Littler P, Manas DM (December 2014). "Systematic review of irreversible electroporation in the treatment of advanced pancreatic cancer". European Journal of Surgical Oncology. 40 (12): 1598–604. doi:10.1016/j.ejso.2014.08.480. PMID 25307210.
- ↑ Kleger A, Perkhofer L, Seufferlein T (July 2014). "Smarter drugs emerging in pancreatic cancer therapy". Annals of Oncology. 25 (7): 1260–1270. doi:10.1093/annonc/mdu013. PMID 24631947.
- ↑ Tang SC, Chen YC (اوت 2014). "Novel therapeutic targets for pancreatic cancer". World Journal of Gastroenterology. 20 (31): 10825–44. doi:10.3748/wjg.v20.i31.10825. PMC 4138462. PMID 25152585.
- ↑ Tang SC, Chen YC (اوت 2014). "Novel therapeutic targets for pancreatic cancer". World Journal of Gastroenterology. 20 (31): 10825–44. doi:10.3748/wjg.v20.i31.10825. PMC 4138462. PMID 25152585.
- ↑ Rossi ML, Rehman AA, Gondi CS (August 2014). "Therapeutic options for the management of pancreatic cancer". World Journal of Gastroenterology. 20 (32): 11142–59. doi:10.3748/wjg.v20.i32.11142. PMC 4145755. PMID 25170201.
- ↑ Ady JW, Heffner J, Klein E, Fong Y (2014). "Oncolytic viral therapy for pancreatic cancer: current research and future directions". Oncolytic Virotherapy. 3: 35–46. doi:10.2147/OV.S53858. PMC 4918362. PMID 27512661.
- ↑ Ren B, Cui M, Yang G, Wang H, Feng M, You L, Zhao Y (July 2018). "Tumor microenvironment participates in metastasis of pancreatic cancer". Molecular Cancer. 17 (1): 108. doi:10.1186/s12943-018-0858-1. PMC 6065152. PMID 30060755.
- ↑ Sachi Das, Sabya; Kumar Dubey, Amit; Singh, Neeru; Ranjan, Priya; Verma, Prasad; Kumar Singh, Shubhankar; Kumar Singh, Sandeep (2023-01-09). "Pancreatic Cancer Treatment by Using Theragnostic Nanoparticles". Hormone Related Cancer Mechanistic and Nanomedicines. pp. 149–168. doi:10.1007/978-981-19-5558-7_8. ISBN 978-981-19-5557-0.
