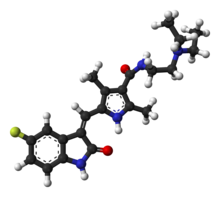
سانیتینیب
 | |
 | |
| دادههای بالینی | |
|---|---|
| نامهای تجاری | Sutent |
| AHFS/Drugs.com | monograph |
| مدلاین پلاس | a607052 |
| دادهها |
|
| ردهبندی داروهای بارداری |
|
| روش مصرف دارو | خوراکی |
| کد ATC | |
| وضعیت قانونی | |
| وضعیت قانونی |
|
| دادههای فارماکوکینتیک | |
| زیست فراهمی | تأثیرناپذیر از غذا |
| پیوند پروتئینی | ۹۵٪ |
| متابولیسم | کبدی (توسط CYP3A4) |
| نیمهعمر حذف | ۴۰ تا ۶۰ ساعت (سانیتینیب) ۸۰ تا ۱۱۰ ساعت (متابولیتهایش) |
| دفع | مدفوع (۶۱٪) و کلیه (۱۶٪) |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| IUPHAR/BPS | |
| دراگبنک | |
| کماسپایدر | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| دادههای فیزیکی و شیمیایی | |
| فرمول شیمیایی | C22H27FN4O۲ |
| جرم مولی | 398.474 g/mol 532.561 g/mol (malate) g·mol−1 |
| مدل سه بعدی (جیمول) | |
| |
| |
| | |
سانیتینیب (انگلیسی: Sunitinib) که با نام تجاری «ساتنت» (Sutent) عرضه میشود و در گذشته با نام اختصاری «SU11248» شناخته میشد، یک مولکول کوچک «بازدارندهٔ تیروزین کیناز گیرندهای» است که سازمان غذا و دارو آمریکا آنرا در سال ۲۰۰۶ میلادی، جهت درمان «سرطان کلیه» (RCC) و همچنین «تومور استرومال گوارشی» مقاومبه ایماتینیب، مورد پذیرش قرار دادهاست. سانیتینیب نخستین دارویی بود که بطور همزمان جهت دو استفادهٔ مختلف مورد پذیرش این سازمان قرار گرفت.[۱]
این دارو عامل رشد مشتق از پلاکت و فاکتور رشد اندوتلیال عروقی را مهار میکند و یک بازدارندهٔ CD117[۲] هم هست.
پژوهشهایی جهت استفاده از سانیتینیب در درمان «مننژیومای ناشی از نوروفیبروماتوز»، «تومورهای نورواندوکرین لوزالمعده»، «سرطان پستان منتشر» و «سرطان ریه از نوعِ سلولِ غیر کوچک» (NSCLC) صورت پذیرفتهاست.
شایعترین عوارض جانبی این دارو، احساس خستگی، اسهال، تهوع، بیاشتهایی، فشار خون بالا، زرد شدن پوست و زخمهای دهانی است.[۳]
منابع[ویرایش]
- ↑ US Food and Drug Administration (2006). "FDA approves new treatment for gastrointestinal and kidney cancer".
- ↑ Hartmann JT, Kanz L (November 2008). "Sunitinib and periodic hair depigmentation due to temporary c-KIT inhibition". Arch Dermatol. 144 (11): 1525–6. doi:10.1001/archderm.144.11.1525. PMID 19015436. Archived from the original on 25 July 2011. Retrieved 18 November 2017.
- ↑ Dasanu CA, et al. (2007-03-01). "Yellow skin discoloration associated with sorafenib use for treatment of metastatic renal cell carcinoma". Southern Medical Journal. 100: 328–330. doi:10.1097/smj.0b013e31802f01a9. Archived from the original on 3 March 2016. Retrieved 18 November 2017.
- مشارکتکنندگان ویکیپدیا. «Sunitinib». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۸ نوامبر ۲۰۱۷.
پیوند به بیرون[ویرایش]
| در ویکیانبار پروندههایی دربارهٔ سانیتینیب موجود است. |
