آرانای
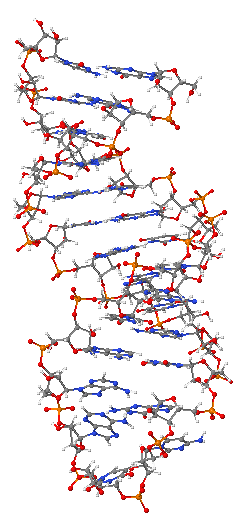
ریبونوکلئیک اسید (به انگلیسی: Ribonucleic acid) یا آراِناِی (RNA) همراه با دیاِناِی و پروتئین، سه مولکول درشت اصلی هستند که برای همهٔ گونههای شناختهشدهٔ زیستی، ضروری هستند. آراِناِی هم مانند دیانای دارای زنجیرهٔ بلندی شامل اجزای سازندهای به نام نوکلئوتیدها است. هر نوکلئوتید دارای یک نوکلئوباز است که گاهی به آن باز نیتروژنی هم میگویند، چیدمان نوکلئوتیدهای یک ژن در دیانای در فرایند رونویسی به آرانای پیامرسان داده میشود، آراِناِی پیامرسان به ریبوزومها میرود و در آنجا در فرایند ترجمه به پیدایش فراوردههای ژنی میانجامد. برخی ویروسها، از آراِناِی به جای دیانای بهعنوان مادهٔ ژنتیکیشان استفاده میکنند. همهٔ جانداران از آرانای پیامرسان برای جابهجایی دادههای ژنتیکی از هستهٔ سلول به ریبوزوم استفاده میکنند که به ساخت پروتئینها میانجامد.
نوعی از آراِناِی اطلاعات را از دیانای به سیتوپلاسم حمل میکند؛ به این نوع آراِناِی که اطلاعات را از دیانای به ریبوزومها حمل میکند، آرانای پیامرسان یا پیامبر (mRNA) میگویند. نوعی دیگر آرانای حامل (tRNA) است که اسیدهای آمینه را به ریبوزوم منتقل میکند، تا ریبوزوم، اسیدهای آمینه را بر اساس اطلاعات موجود در آرانای پیامرسان کنار یکدیگر ردیف کند. نوع دیگر، آرانای ریبوزومی (rRNA) است که در ساختار ریبوزومها شرکت دارد؛ این موضوع به این معناست که ریبوزومها متشکل از پروتئینها و آراِناِی های ریبوزومی هستند.
ساختمان[ویرایش]
ساختار شیمیایی آراِناِی به ساختار شیمیایی دیاِناِی بسیار شبیه است، با سه تفاوت؛ یکی اینکه آراِناِی دارای قند ریبوز است درحالیکه دیاِناِی دارای قند کمی متفاوتتر به نام دئوکسیریبوز است (گونهای از ریبوز که یک اتم اکسیژن در آن کم است) و دوّم اینکه آراِناِی دارای نوکلئوباز یوراسیل است درحالیکه بهجای آن دیاِناِی دارای تیمین است (یوراسیل و تیمین، خواص جفت شدن بازی مشابهی دارند). و سوم اینکه برخلاف دیانای بیشتر مولکولهای آراِناِی تکرشتهای هستند. مولکولهای تکرشتهای آراِناِی ساختارهای سهبعدی بسیار پیچیدهای را دارند، زیرا آنها مانند دیاِناِی دارای زنجیرهٔ دورشتهای نیستند. (البته آراِناِی دورشتهای هم وجود دارد) آراِناِی درون یاختههای زنده توسط آراِناِی پلیمرازها ساخته میشوند، این آنزیمها در رونویسی از روی یک الگوی آراِناِی یا دیاِناِی به یک رشته آراِناِی تازه کارایی دارند.
مقایسهٔ آراِناِی با دیاِناِی[ویرایش]
آراِناِی و دیاِناِی هر دو اسید نوکلئیک هستند، اما در سه چیز تفاوت دارند:
نخست اینکه برخلاف دیاِناِی که دورشتهای است، آراِناِی یک مولکول تکرشتهای است و زنجیرهٔ بسیار کوتاهتری از نوکلئوتیدها را دارد.
دوم اینکه درحالیکه دیاِناِی دارای قند دئوکسیریبوز است، آراِناِی دارای ریبوز است (در دئوکسیریبوز هیچ گروه هیدروکسیلی به حلقهٔ پنتوزی در جایگاه ۲ پیوند ندارد). این گروههای هیدروکسیلی، پایداری آراِناِی را کمتر از پایداری دیاِناِی میسازند زیرا داشتن گروه هیدروکسیل، ریبوز را برای واکنش آبکافت آمادهتر میسازد. سوّم اینکه برخلاف دیاِناِی در آراِناِی، باز تکمیلکنندهٔ آدنین، تیمین نیست بلکه یوراسیل است که شکل متیلهنشدهای از تیمین است. بیشتر آراِناِیهای کارا از دیدگاه زیستی که شامل آرانای کوچک هستهای، آرانای ریبوزومی، آرانای حامل، آرانای پیامرسان و دیگر آرانایهای غیر-کدکننده، گاه دارای چیدمانهای خود تکمیلکنندهای هستند که به بخشهایی از آراِناِی این اجازه را میدهند که با خودش جفت شده و تا بخورد و مارپیچهای دوتایی را پدیدآورند (همانند دیاِناِی). برخلاف دیاِناِی، ساختار آنها دارای مارپیچهای دوتایی دراز نیستند اما در جایجای آنها گروههایی از مارپیچهای کوتاه دیده میشود. آراِناِی به جز برخی موارد استثنا، همیشه بهصورت خطی وجود دارد.
ساختهشدن آراِناِی[ویرایش]
آراِناِی از روی یکی از رشتههای دیاِناِی در هستهٔ یاختههای یوکاریوت یا بخش نوکلئوئیدی پروکاریوتها با کمک آنزیمهای آرانای پلیمراز I (ژنهای آرانای ریبوزومی) و آرانای پلیمراز II (ژنهای آرانای پیامرسان) و آرانای پلیمراز III (ژنهای آرانای حامل) در یوکاریوتها و گونهای آنزیم آرانای پلیمراز در یاختههای یوکاریوتی رونویسی میشود.
واکنشهای فرآوری آنها با آنزیمهایی بهنام آرانای پلیمراز، که از دیانای به عنوان الگوی خود بهره میبرند، آسان میشود، فرایند فرآوری آنها به رونویسی مشهور است. آغاز رونویسی با پیوند یک آنزیم به چیدمان پروموتر، که بهطور معمول در بالادست ژن جای دارد، آغاز میشود. زنجیرهٔ مارپیچ دوتایی دیاِناِی، به کمک آنزیم هلیکاز باز میشود. این آنزیم در درازای رشتهٔ الگو از سمت '۳ آن به '۵ آن پیش میرود و یک مولکول آراِناِی مکمل را میسازد که این آراِناِی از آنجایی که وارونهٔ رشتهٔ الگو است از سمت '۵ آن به '۳ آن ساخته میشود. در ساخت آراِناِی، چیدمان دیاِناِی، پایان ساخت آراِناِی را هم نشان خواهد داد. آراِناِی ها پس از رونویسی، به کمک آنزیمهای دیگری فرآوری میشوند و سرانجام یک آراِناِی را پدیدمیآورند که در ساخت پروتئین در فرایند ترجمه بهکار برده میشوند. برای نمونه، در یوکاریوتها یک دُم چندآدنینی در فرایند پلیآدنیله شدن و در فرایندی دیگر یک کلاهک '۵ به آنها افزوده میشود. در یکی دیگر از بخشهای این فرآوری، اینترونها به کمک آنزیم پیرایشگر در فرایند پیرایش برداشته میشوند.
شماری آرانای پلیمراز نیز هستند که کارکردشان وابسته به آراِناِی است و از یک آراِناِی به عنوان الگویشان برای ساخت یک رشتهٔ آراِناِی تازه بهره میبرند. برای نمونه، برخی آراِناِی های ویروسی، مانند ویروس فلج اطفال، این گونه آنزیم را برای رونویسی ژنهایشان بهکار میبرند.
ساختار[ویرایش]
هر نوکلئوتید در آراِناِی دارای یک قند ریبوز با کربنهای شمارهگذاریشده از ۱ تا ۵ است. یکی از بازهای آدنین، گوانین، سیتوزین، یا اوراسیل به کربن شمارهٔ ۱ پیوند میخورد. به آدنین و گوانین، خانوادهٔ پورینها (دوحلقهایها) گفته میشود و به سیتوزین و اوراسیل، خانوادهٔ پیریمیدینها (تکحلقهایها) گفته میشود. گروههای فسفات دارای یک بار منفی هستند که با پیوند به آراِناِی، آن را یک مولکول باردار میسازند.
بازها ممکن است پیوندهای هیدروژنی میان سیتوزین با گوانین، آدنین با اوراسیل، و گوانین با اوراسیل را تشکیل دهند. به هر حال برهمکنشهای دیگری هم امکانپذیر است، برای نمونه، پیوند یک گروه از بازهای آدنینی به همدیگر در یک برآمدگی یا تترالوپ GNRA که یک جفت باز گوانین–آدنینی دارد.
ویژگی ساختاری مهم آراِناِی که آن را از دیاِناِی جدا میسازد، داشتن یک گروه هیدروکسیل در کربن شمارهٔ ۲ قند ریبوز است. بودن این گروه به این میانجامد که شکل هندسی زنجیرهٔ مارپیچی آن با دیاِناِی تفاوت پیدا کند. دوّمین نتیجه پیامد داشتن این گروه هیدروکسیل در کربن ۲، در نواحی انعطافپذیری شکلی (تطبیقی) از یک مولکول آراِناِی است (که در تشکیل یک مارپیچ دوتایی درگیر نیست)، آراِناِی تنها با چهار باز توصیف میشود که عبارتاند از آدنین، سیتوزین، گوانین، و یوراسیل،
در آراِناِی ریبوزومی، بسیاری از اصلاحات پس از رونویسی، در نواحی بسیار عملکردی اتفاق میافتد، از جمله مرکز پپتیدیل ترانسفراز و زیرواحد رابط، که نشاندهندهٔ این است که آنها برای عملکرد عادی، مهم هستند. شکل عملکردی مولکولهای تکرشتهای آراِناِی، کاملاً مانند پروتئینها، به ساختار سوّم ویژهای نیاز دارد. چارچوب (داربست) این ساختار توسط عناصر ساختاری دوّم تولید میشود که همان پیوندهای هیدروژنی درونمولکولی هستند. این ساختار دوّم به پدید آمدن چندین نمایهٔ قابل شناسایی مانند حلقههای سنجاق سری، شکمخوردگیها، و حلقههای درونی میانجامد. از آنجایی که آراِناِی باردار است، یونهای فلزی از جمله Mg2+ برای پایاسازی بسیاری از ساختارهای دوّم و سوّم مورد نیاز هستند.
گونههای آراِناِی[ویرایش]
آرانای پیامرسان[ویرایش]
آرانای پیامرسان گونهای آراِناِی است که دادهها را از دیاِناِی به ریبوزوم، جایگاه ساخت پروتئین و ترجمه در یاخته، میبرد. چیدمان آراِناِی پیامرسان، چیدمان اسید آمینهٔ پروتئینی که ساخته میشود را تعیین میکند.
بسیاری از آراِناِی ها به پروتئین فرآوری نمیشوند. بسیاری از آراِناِی ها در رمزگردانی به پروتئین فراورده نمیشوند. به این آراِناِی ها، آرانای غیر-کدکننده میگویند. برجستهترین نمونهٔ آرانای غیر-کدکننده آرانای حامل و آرانای ریبوزومی هستند که هر دوی آنها در فرایند ترجمه دارای کارکرد هستند.
آراِناِی های ویژهای میتوانند واکنشهای شیمیایی، مانند بریدن و بستن دیگر مولکولهای آراِناِی، را انجام دهند و تشکیل پیوند پپتیدی را در ریبوزوم آسان کنند، این آراِناِی ها به آرانای ریبوزومی مشهورند.
در فرایند ترجمه، آرانای پیامرسان دادههای مورد نیاز در چیدمان اسیدهای آمینهٔ یک پروتئین را به ریبوزومها؛ کارخانههای ساخت پروتئین در یاخته، میبرند. این به گونهای کد میشود که هر سه نوکلئوتید (یک رمز ژنتیکی یا کدون) مطابق با یک اسید آمینه است. در سلولهای یوکاریوتی، همین که آراِناِی پیامرسان پیشساز (pre-mRNA) از دیاِناِی رونویسی شد، به آراِناِی پیامرسان بالغ پردازش (اصلاح) میشود. این فرایند، اینترونهای (بخشهای کد نشوندهٔ pre-mRNA) آن را جدا میکند. آراِناِیهای پیامرسان سپس از هسته به سیتوپلاسم صادر میشود، جایی که آن به ریبوزوم متصل میشود و به شکل پروتئین متناظرش به کمک آرانای حامل، ترجمه میشود.
در سلولهای پروکاریوتی که هسته و اجزای سیتوپلاسمی ندارند، آرانای پیامرسان میتواند به ریبوزومها متصل شود درحالیکه آن از دیاِناِی رونوشتبرداری (رونویسی) میشود. پس از مدتی پیام به نوکلئوتیدهای مؤلفهٔ خودش با یاری ریبونوکلئازها تجزیه میشود. آرانای حامل (tRNA)، یک زنجیرهٔ آراِناِی کوچک با حدود ۸۰ نوکلئوتید است که یک اسید آمینهٔ خاص را به زنجیرهٔ پلیپپتیدی در حال رشد در محل ریبوزومی سنتز پروتئین در طول ترجمه، منتقل میکند. اینها محلهایی برای اتصال اسید آمینه و یک ناحیهٔ آنتیکدون برای تشخیص کدون دارد که به یک توالی خاص بر روی زنجیرهٔ آرانای پیامرسان از طریق پیوند هیدروژنی متصل میشود.
آراِناِی ریبوزومی[ویرایش]
آرانایهای ریبوزومی جزء کاتالتیک ریبوزومها هستند. ریبوزومهای یوکاریوتی حاوی ۴ مولکول آرانای ریبوزومی مختلف هستند: آرانای ریبوزومی ۱۸اس، آرانای ریبوزومی ۵٫۸اس، آرانای ریبوزومی ۲۸اس و آراِناِی ریبوزومی ۵اس. سه عدد از مولکولهای آرانای ریبوزومی در هسته سنتز میشوند و سایر آنها در جای دیگر سنتز میشود. در سیتوپلاسم، آراِناِی ریبوزومی و پروتئین برای تشکیل یک نوکلئوپروتئین که ریبوزوم نامیده میشود، ترکیب میشوند. ریبوزوم به آراِناِی پیامرسان متصل میشود و سنتز پروتئین را عملی (اجرا) میکند. چندین ریبوزوم ممکن است به یک آراِناِی پیامرسان منفرد در هر زمانی متصل شوند. آراِناِی ریبوزومی بسیار فراوان است و ۸۰٪ از ۱۰ میلیگرم/میلیلیتر آراِناِی یافت شده در یک سیتوپلاسم یوکاریوت نمونه را تشکیل میدهد.
آرانای پیامرسان-ناقل (tmRNA)[ویرایش]
در بسیاری از باکتریها و پلاستیدها یافت میشود. این، پروتئینهای کد شده توسط آرانای پیامرسان را نشاندار میکند که فاقد کدونهای توقف برای تجزیه هستند و ریبوزوم را از ماندن بازمیدارد.
آراِناِیهای تنظیمی[ویرایش]
چندین نوع از آراِناِی میتواند بیان ژن را توسط مکمل یکدیگر بودن (متمم بودن) برای یک بخش آرانای پیامرسان یا یک دیاِناِی ژن، فروتنظیم کند. (فروتنظیمی یا DN فرایندی است که به وسیلهٔ آن، یک سلول؛ کمیت یک جزء سلولی مانند پروتئین یا آراِناِی را در پاسخ به یک متغیر خارجی کاهش میدهد. افزایش یک جزء سلولی، فراتنظیمی نامیده میشود).
ریزآراِناِی (miRNA)[ویرایش]
ریزآرانای با ۲۱ تا ۲۲ نوکلئوتید در یوکاریوتها یافت میشود و از طریق مداخله RNA (RNAi) عمل میکنند، جاییکه یک کمپلکس مؤثر از ریزآراِناِی و آنزیمها میتوانند آرانای پیامرسان را به ریزآراِناِی که متمم است بشکند، آرانای پیامرسان را از ترجمه شدن ممانعت کند، یا تجزیهٔ آن را تسریع کند. درحالیکه آراِناِیهای مداخلهای کوچک (siRNA) با 20 تا 25 نوکلئوتید، غالباً توسط تجزیهٔ (شکستن) آراِناِی ویروسی تولید میشوند، همچنین منابع درونزادی نیز از این گونه آراِناِی وجود دارد. siRNAها از طریق مداخلهٔ آراِناِی در یک روش مشابه با miRNA عمل میکنند. بعضی از siRNAها و miRNAها میتوانند ژنهایی را که آنها نشاندار میکنند، متیله شوند که بدان وسیله، رونویسی این ژنها را کاهش یا افزایش میدهد. جانوران، آراِناِیهای برهمکنشدهنده Piwi (piRNA; 29-30 nt) دارند که در سلولهای جنینی فعال هستند و تصور میشود که دفاعی در برابر ترانسپوزونها باشند و در گامتوژنز ایفای نقش کنند. بسیاری از پروکاریوتها، آراِناِیهای CRISPR، یک سیستم تنظیمی مشابه با RNAi، دارند. آراِناِیهای آنتیسنس، بسیار گسترده و وسیع هستند، اکثراً یک ژن را فروتنظیم میکنند، اما تعدادی نیز فعالکنندهٔ رونویسی هستند. یک روش که آراِناِی آنتیسنس میتواند عمل کند، از طریق اتصال به یک آرانای پیامرسان و تشکیل یک آراِناِی دورشتهای است که بهطور آنزیمی تجزیه میشود. آراِناِیهای غیر-کدکنندهٔ طویل بسیاری وجود دارد که ژنها را در یوکاریوتها تنظیم میکنند. یکی از این آراِناِیها، xist است که یک کروموزوم ایکس را در پستانداران ماده میپوشاند و آن را غیرفعال میکند. یک آرانای پیامرسان ممکن است به خودیِ خود حاوی اجزای تنظیمی باشد، از جمله riboswitchها، در ناحیهٔ ترجمهنشوندهٔ ۵' یا ناحیهٔ ترجمهنشوندهٔ ۳'. این عناصر تنظیمی سیس، فعالیت آن آرانای پیامرسان را تنظیم میکنند. ناحیههای ترجمهنشونده همچنین ممکن است حاوی عناصری باشند که دیگر ژن را تنظیم میکنند.
آراِناِی دورشتهای[ویرایش]
آراِناِی دورشتهای (dsRNA) یک آراِناِی است با دو رشتهٔ مکمل یکدیگر که همانند دیاِناِی در همهٔ یاختهها یافت میشود. آراِناِی دورشتهای، مادهٔ ژنتیکی برخی ویروسها را میسازد. آراِناِی دورشتهای شامل آراِناِی ویروسی و آراِناِی کوچک مداخلهگر میتوانند در ترجمهٔ ژن دگرگونی پدیدآورند. این دگرگونی بیشتر از راه جفت شدن با آراِناِی پیامرسان و سرکوب کارایی آن که به کم شدن فراوردههای ژنی میانجامد، پدید میآید.
پردازش آراِناِی[ویرایش]
آراِناِی های بسیاری در اصلاح آراِناِی های دیگر درگیر هستند. اینترونها از pre-mRNA به وسیلهٔ اسپلایسوزومها پردازش میشوند که حاوی چندین آراِناِی کوچک هستهای (snRNA) هستند. یا اینترونها میتوانند ریبوزیمهایی شوند که توسط خودشان پردازش میشوند. آراِناِی میتواند همچنین توسط نگه داشتن نوکلئوتیدهای اصلاح شدهاش برای نوکلئوتیدهای به غیر از A, C, G و U، تغییر یابد. در یوکاریوتها، اصلاحات نوکلئوتیدهای آراِناِی عموماً توسط آراِناِی هستکی کوچک (snoRNA) هدایت میشود، که در هستک و جسم کاخال یافت میشوند. snoRNAها با آنزیمها همکاری میکنند و آنها را به یک موضع بر روی آراِناِی توسط جفت شدن بازی به آن آراِناِی، هدایت میکنند. این آنزیمها سپس اصلاح نوکلئوتیدی را انجام میدهند. آراِناِیهای ریبوزومی و آراِناِیهای حامل بهطور وسیعی اصلاحشده هستند، اما snRNAها و آراِناِیهای پیامرسان میتوانند همچنین هدف اصلاح شدن بازی قرار بگیرند.
ژنومهای آراِناِی[ویرایش]
مانند دیاِناِی, آراِناِی میتواند اطلاعات ژنتیکی را حمل کند. آرانای ویروسها، ژنومهایی مرکب از آراِناِی و انواعی از پروتئینهای کدشده توسط آن ژنوم را دارند. ژنوم ویروسی توسط بعضی از آن پروتئینها رونوشتبرداری میشود، درحالیکه دیگر پروتئینها ژنوم را محافظت میکنند. به محض اینکه ذرهٔ ویروسی به یک سلول میزبان وارد میشود.
ویروئیدها گروه دیگری از پاتوژنها هستند، اما آنها فقط حاوی آراِناِی هستند. هیچ پروتئینی را کد نمیکنند و توسط یک پلیمراز سلول گیاهی میزبان رونوشتبرداری میشود.
رونویسی وارونه[ویرایش]
ویروسهای رونوشتبردار معکوس، ژنومشان را بهوسیلهٔ نسخههای دیاِناِی رونوشت معکوس از آراِناِیهایشان، رونوشتبرداری میکنند. این نسخههای دیاِناِی سپس به یک آراِناِی جدید رونویسی میشوند. رتروترانسپوزونها همچنین توسط کپی شدن دیاِناِی و آراِناِی از یکدیگر گسترش مییابند و تلومراز حاوی یک آراِناِی است که بهعنوان الگو برای ساختن پایانههای کروموزومهای یوکاریوتی استفاده میشوند.
پژوهشها در زیستشناسی آراِناِی[ویرایش]
تحقیق بر روی آراِناِی منجر به کشفهای زیستشناختی مهم و جوایز نوبل متعددی شدهاست. اسیدهای نوکلئیک در سال ۱۸۶۸ توسط فردریش میشر کشف شد. بعداً کشف شد که سلولهای پروکاریوتی که هستهای ندارند، نیز همچنین در ناحیهٔ نوکلئوئیدی خود حاوی اسیدهای نوکلئیک هستند. نقش آراِناِی در سنتز پروتئین همواره در سال ۱۹۳۹ مورد توجه بود. سورو اوچوآ جایزهٔ نوبل را در سال ۱۹۵۹ (مشترکاً با آرتور کورنبرگ) برنده شد.
در سال ۱۹۶۷ کارل ووز فرضیه داد که آراِناِی ممکن است کاتالتیک باشد و پیشنهاد کرد که ابتداییترین اشکال حیات (مولکولهای خودرونوشتبردار) توانستهاند هم برای حمل اطلاعات ژنتیکیشان و هم برای کاتالیز واکنشهای بیوشیمیاییشان به آراِناِی تکیه کنند.
جستارهای وابسته[ویرایش]
- دیانای
- ریبوزوم
- پروتئین
- باز نوکلئوتیدی
- نوکلئوتید
- رونویسی (ژنتیک)
- ترجمه (زیستشناسی)
- همانندسازی دیانای
- ژنتیک
- کروموزوم
- تولیدمثل
منابع[ویرایش]
- Biologie moléculaire de la cellule, by Bruce Alberts, Flammarion, 4th edition, 2004
- a b c Berg JM, Tymoczko JL, Stryer L (2002). Biochemistry (5th ed.). WH Freeman and Company. pp. 118–19, 781–808. شابک ۰−۷۱۶۷−۴۶۸۴−۰. OCLC 48055706 59502128 179705944 48055706 59502128.
- Higgs PG (2000). "RNA secondary structure: physical and computational aspects". Quarterly Reviews of Biophysics 33: 199–253. doi:10.1017/S0033583500003620. PMID 11191843.
- a b Nissen P, Hansen J, Ban N, Moore PB, Steitz TA (2000). "The structural basis of ribosome activity in peptide bond synthesis". Science 289 (5481): 920–30. doi:10.1126/science.289.5481.920. PMID 10937990.
- a b Lee JC, Gutell RR (2004). "Diversity of base-pair conformations and their occurrence in rRNA structure and RNA structural motifs". J. Mol. Biol. 344 (5): 1225–49. doi:10.1016/j.jmb.2004.09.072. PMID 15561141.
- Barciszewski J, Frederic B, Clark C (1999). RNA biochemistry and biotechnology. Springer. pp. 73–87. ISBN 0-7923-5862-7. OCLC 52403776.
- Salazar M, Fedoroff OY, Miller JM, Ribeiro NS, Reid BR (1992). "The DNA strand in DNAoRNA hybrid duplexes is neither B-form nor A-form in solution". Biochemistry 32 (16): 4207–15. doi:10.1021/bi00067a007. PMID 7682844.
- Hermann T, Patel DJ (2000). "RNA bulges as architectural and recognition motifs". Structure 8 (3): R47–R54. doi:10.1016/S0969-2126(00)00110-6. PMID 10745015.
- Mikkola S, Nurmi K, Yousefi-Salakdeh E, Strömberg R, Lönnberg H (1999). "The mechanism of the metal ion promoted cleavage of RNA phosphodiester bonds involves a general acid catalysis by the metal aquo ion on the departure of the leaving group". Perkin transactions 2 (8): 1619–26. doi:10.1039/a903691a.
- Jankowski JAZ, Polak JM (1996). Clinical gene analysis and manipulation: Tools, techniques and troubleshooting. Cambridge University Press. pp. 14. ISBN 0-521-47896-0. OCLC 33838261.
- Yu Q, Morrow CD (2001). "Identification of critical elements in the tRNA acceptor stem and TΨC loop necessary for human immunodeficiency virus type 1 infectivity". J Virol. 75 (10): 4902–6. doi:10.1128/JVI.75.10.4902-4906.2001. PMID 11312362.
- Elliott MS, Trewyn RW (1983). "Inosine biosynthesis in transfer RNA by an enzymatic insertion of hypoxanthine". J. Biol. Chem. 259 (4): 2407–10. PMID 6365911.
- Söll D, RajBhandary U (1995). TRNA: Structure, biosynthesis, and function. ASM Press. pp. 165. ISBN 1-55581-073-X. OCLC 30663724 183036381 30663724.
- Kiss T (2001). "Small nucleolar RNA-guided post-transcriptional modification of cellular RNAs". The EMBO Journal 20: 3617–22. doi:10.1093/emboj/20.14.3617. PMC 125535. PMID 11447102.
- King TH, Liu B, McCully RR, Fournier MJ (2002). "Ribosome structure and activity are altered in cells lacking snoRNPs that form pseudouridines in the peptidyl transferase center". Molecular Cell 11 (2): 425–35. doi:10.1016/S1097-2765(03)00040-6. PMID 12620230.
- Mathews DH, Disney MD, Childs JL, Schroeder SJ, Zuker M, Turner DH (2004). "Incorporating chemical modification constraints into a dynamic programming algorithm for prediction of RNA secondary structure". Proc. Natl. Acad. Sci. USA 101 (19): 7287–92. doi:10.1073/pnas.0401799101. PMC 409911. PMID 15123812.
- Tan ZJ, Chen SJ (2008). "Salt dependence of nucleic acid hairpin stability". Biophys. J. 95 (2): 738–52. doi:10.1529/biophysj.108.131524. PMC 2440479. PMID 18424500.
- Nudler E, Gottesman ME (2002). "Transcription termination and anti-termination in E. coli". Genes to Cells 7: 755–68. doi:10.1046/j.1365-2443.2002.00563.x. PMID 12167155.
- Jeffrey L Hansen, Alexander M Long, Steve C Schultz (1997). "Structure of the RNA-dependent RNA polymerase of poliovirus". Structure 5 (8): 1109–22. doi:10.1016/S0969-2126(97)00261-X. PMID 9309225.
- Ahlquist P (2002). "RNA-Dependent RNA Polymerases, Viruses, and RNA Silencing". Science 296 (5571): 1270–73. doi:10.1126/science.1069132. PMID 12016304.
- a b c Cooper GC, Hausman RE (2004). The Cell: A Molecular Approach (3rd ed.). Sinauer. pp. 261–76, 297, 339–44. شابک ۰−۸۷۸۹۳−۲۱۴−۳. OCLC 52121379 52359301 56050609 174924833 52121379 52359301 56050609.
- Mattick JS, Gagen MJ (۱ سپتامبر ۲۰۰۱). "The evolution of controlled multitasked gene networks: the role of introns and other noncoding RNAs in the development of complex organisms". Mol. Biol. Evol. 18 (9): 1611–30. PMID 11504843. http://mbe.oxfordjournals.org/cgi/pmidlookup?view=long&pmid=11504843.
- Mattick, JS (2001). "Noncoding RNAs: the architects of eukaryotic complexity". EMBO Reports 2 (11): 986–91. doi:10.1093/embo-reports/kve230. PMC 1084129. PMID 11713189. https://web.archive.org/web/20051227234650/http://emboreports.npgjournals.com/cgi/content/full/2/11/986.
- Mattick JS (اکتبر ۲۰۰۳). "Challenging the dogma: the hidden layer of non-protein-coding RNAs in complex organisms". BioEssays: News and Reviews in Molecular, Cellular and Developmental Biology 25 (10): 930–9. doi:10.1002/bies.10332. PMID 14505360. https://web.archive.org/web/20090306105646/http://www.imb-jena.de/jcb/journal_club/mattick2003.pdf.
- Mattick JS (اکتبر ۲۰۰۴). "The hidden genetic program of complex organisms". Scientific American 291 (4): 60–7. doi:10.1038/scientificamerican1004-60. PMID 15487671. http://www.sciam.com/article.cfm?articleID=00045BB6-5D49-1150-902F83414B7F4945.
- a b c Wirta W (2006). Mining the transcriptome – methods and applications. Stockholm: School of Biotechnology, Royal Institute of Technology. ISBN 91-7178-436-5. OCLC 185406288. http://kth.diva-portal.org/smash/get/diva2:10803/FULLTEXT01.
- Rossi, JJ (2004). "Ribozyme diagnostics comes of age". Chemistry & Biology 11 (7): 894–95. doi:10.1016/j.chembiol.2004.07.002. PMID 15271347.
- Kampers T, Friedhoff P, Biernat J, Mandelkow E-M, Mandelkow E (1996). "RNA stimulates aggregation of microtubule-associated protein tau into Alzheimer-like paired helical filaments". FEBS Letters 399 (3): 104D. doi:10.1016/S0014-5793(96)01386-5. PMID 8985176.
- Gueneau de Novoa P, Williams KP (2004). "The tmRNA website: reductive evolution of tmRNA in plastids and other endosymbionts". Nucleic Acids Res. 32 (Database issue): D104–8. doi:10.1093/nar/gkh102. PMC 308836. PMID 14681369.
- Wu L, Belasco JG (ژانویه ۲۰۰۸). "Let me count the ways: mechanisms of gene regulation by miRNAs and siRNAs". Mol. Cell 29 (1): 1–7. doi:10.1016/j.molcel.2007.12.010. PMID 18206964.
- Matzke MA, Matzke AJM (2004). "Planting the seeds of a new paradigm". PLoS Biology 2 (5): e133. doi:10.1371/journal.pbio.0020133. PMC 406394. PMID 15138502.
- Vazquez F, Vaucheret H, Rajagopalan R, Lepers C, Gasciolli V, Mallory AC, Hilbert J, Bartel DP, Crété P (2004). "Endogenous trans-acting siRNAs regulate the accumulation of Arabidopsis mRNAs". Molecular Cell 16 (1): 69–79. doi:10.1016/j.molcel.2004.09.028. PMID 15469823.
- Watanabe T, Totoki Y, Toyoda A, et al. (مه ۲۰۰۸). "Endogenous siRNAs from naturally formed dsRNAs regulate transcripts in mouse oocytes". Nature 453 (7194): 539–43. doi:10.1038/nature06908. PMID 18404146.
- Sontheimer EJ, Carthew RW (ژوئیه ۲۰۰۵). "Silence from within: endogenous siRNAs and miRNAs". Cell 122 (1): 9–12. doi:10.1016/j.cell.2005.06.030. PMID 16009127.
- Doran G (2007). "RNAi – Is one suffix sufficient?". Journal of RNAi and Gene Silencing 3 (1): 217–19. https://web.archive.org/web/20070716115053/http://www.libpubmedia.co.uk/RNAiJ-Issues/Issue-5/Doran.htm.
- Pushparaj PN, Aarthi JJ, Kumar SD, Manikandan J (2008). "RNAi and RNAa - The Yin and Yang of RNAome". Bioinformation 2 (6): 235–7. PMC 2258431. PMID 18317570.
- Horwich MD, Li C Matranga C, Vagin V, Farley G, Wang P, Zamore PD (2007). "The Drosophila RNA methyltransferase, DmHen1, modifies germline piRNAs and single-stranded siRNAs in RISC". Current Biology 17: 1265–72. doi:10.1016/j.cub.2007.06.030. PMID 17604629.
- Girard A, Sachidanandam R, Hannon GJ, Carmell MA (2006). "A germline-specific class of small RNAs binds mammalian Piwi proteins". Nature 442 (7099): 199–202. doi:10.1038/nature04917. PMID 16751776.
- Horvath P, Barrangou R (2010). "CRISPR/Cas, the Immune System of Bacteria and Archaea". Science 327 (5962): 167. doi:10.1126/science.1179555. PMID 20056882. http://www.sciencemag.org/cgi/content/abstract/327/5962/167.
- Wagner EG, Altuvia S, Romby P (2002). "Antisense RNAs in bacteria and their genetic elements". Adv Genet. 46: 361–98. doi:10.1016/S0065-2660(02)46013-0. PMID 11931231.
- Gilbert SF (2003). Developmental Biology (7th ed.). Sinauer. pp. 101–3. ISBN 0-87893-258-5. OCLC 154663147 174530692 177000492 177316159 51544170 54743254 59197768 61404850 66754122 154656422 154663147 174530692 177000492 177316159 51544170 54743254 59197768 61404850 66754122.
- Amaral PP, Mattick JS (اکتبر ۲۰۰۸). "Noncoding RNA in development". Mammalian genome: official journal of the International Mammalian Genome Society 19 (7–8): 454. doi:10.1007/s00335-008-9136-7. PMID 18839252.
- Heard E, Mongelard F, Arnaud D, Chureau C, Vourc'h C, Avner P (1999). "Human XIST yeast artificial chromosome transgenes show partial X inactivation center function in mouse embryonic stem cells". Proc. Natl. Acad. Sci. USA 96 (12): 6841–46. doi:10.1073/pnas.96.12.6841. PMC 22003. PMID 10359800.
- Batey RT (2006). "Structures of regulatory elements in mRNAs". Curr. Opin. Struct. Biol. 16 (3): 299–306. doi:10.1016/j.sbi.2006.05.001. PMID 16707260.
- Scotto L, Assoian RK (ژوئن ۱۹۹۳). "A GC-rich domain with bifunctional effects on mRNA and protein levels: implications for control of transforming growth factor beta 1 expression". Mol. Cell. Biol. 13 (6): 3588–97. PMC 359828. PMID 8497272. http://mcb.asm.org/cgi/pmidlookup?view=long&pmid=8497272.
- Steitz TA, Steitz JA (1993). "A general two-metal-ion mechanism for catalytic RNA". Proc. Natl. Acad. Sci. U.S.A. 90 (14): 6498–502. doi:10.1073/pnas.90.14.6498. PMC 46959. PMID 8341661.
- Xie J, Zhang M, Zhou T, Hua X, Tang L, Wu W (2007). "Sno/scaRNAbase: a curated database for small nucleolar RNAs and cajal body-specific RNAs". Nucleic Acids Res. 35 (Database issue): D183–7. doi:10.1093/nar/gkl873. PMC 1669756. PMID 17099227.
- Omer AD, Ziesche S, Decatur WA, Fournier MJ, Dennis PP (2003). "RNA-modifying machines in archaea". Molecular Microbiology 48 (3): 617–29. doi:10.1046/j.1365-2958.2003.03483.x. PMID 12694609.
- Daròs JA, Elena SF, Flores R (2006). "Viroids: an Ariadne's thread into the RNA labyrinth". EMBO Rep. 7 (6): 593–8. doi:10.1038/sj.embor.7400706. PMC 1479586. PMID 16741503.
- Kalendar R, Vicient CM, Peleg O, Anamthawat-Jonsson K, Bolshoy A, Schulman AH (2004). "Large retrotransposon derivatives: abundant, conserved but nonautonomous retroelements of barley and related genomes". Genetics 166 (3): D339. doi:10.1534/genetics.166.3.1437. PMC 1470764. PMID 15082561.
- Podlevsky JD, Bley CJ, Omana RV, Qi X, Chen JJ (2008). "The telomerase database". Nucleic Acids Res. 36 (Database issue): D339–43. doi:10.1093/nar/gkm700. PMC 2238860. PMID 18073191.
- Blevins T et al. (2006). "Four plant Dicers mediate viral small RNA biogenesis and DNA virus induced silencing". Nucleic Acids Res 34 (21): 6233–46. doi:10.1093/nar/gkl886. PMC 1669714. PMID 17090584.
- Jana S, Chakraborty C, Nandi S, Deb JK (2004). "RNA interference: potential therapeutic targets". Appl. Microbiol. Biotechnol. 65 (6): 649–57. doi:10.1007/s00253-004-1732-1. PMID 15372214.
- Schultz U, Kaspers B, Staeheli P (2004). "The interferon system of non-mammalian vertebrates". Dev. Comp. Immunol. 28 (5): 499–508. doi:10.1016/j.dci.2003.09.009. PMID 15062646.
- Dahm R (2005). "Friedrich Miescher and the discovery of DNA". Developmental Biology 278 (2): 274–88. doi:10.1016/j.ydbio.2004.11.028. PMID 15680349.
- Caspersson T, Schultz J (1939). "Pentose nucleotides in the cytoplasm of growing tissues". Nature 143 (3623): 602–3. doi:10.1038/143602c0.
- Ochoa S (1959). "Enzymatic synthesis of ribonucleic acid". Nobel Lecture. http://nobelprize.org/nobel_prizes/medicine/laureates/1959/ochoa-lecture.pdf.
- Holley RW et al. (1965). "Structure of a ribonucleic acid". Science 147 (1664): 1462–65. doi:10.1126/science.147.3664.1462. PMID 14263761.
- Siebert S (2006). "Common sequence structure properties and stable regions in RNA secondary structures". Dissertation, Albert-Ludwigs-Universität, Freiburg im Breisgau. pp. 1. https://web.archive.org/web/20120309212648/http://deposit.ddb.de/cgi-bin/dokserv?idn=982323891&dok_var=d1&dok_ext=pdf&filename=982323891.pdf.
- Szathmáry E (1999). "The origin of the genetic code: amino acids as cofactors in an RNA world". Trends Genet. 15 (6): 223–9. doi:10.1016/S0168-9525(99)01730-8. PMID 10354582.
- Fiers W et al. (1976). "Complete nucleotide-sequence of bacteriophage MS2-RNA: primary and secondary structure of replicase gene". Nature 260 (5551): 500–7. doi:10.1038/260500a0. PMID 1264203.
- Napoli C, Lemieux C, Jorgensen R (1990). "Introduction of a chimeric chalcone synthase gene into petunia results in reversible co-suppression of homologous genes in trans". Plant Cell 2 (4): 279–89. doi:10.1105/tpc.2.4.279. PMC 159885. PMID 12354959.
- Dafny-Yelin M, Chung SM, Frankman EL, Tzfira T (دسامبر ۲۰۰۷). "pSAT RNA interference vectors: a modular series for multiple gene down-regulation in plants". Plant Physiol. 145 (4): 1272–81. doi:10.1104/pp. 107.106062. PMC 2151715. PMID 17766396.
- Ruvkun G (2001). "Glimpses of a tiny RNA world". Science 294 (5543): 797–99. doi:10.1126/science.1066315. PMID 11679654.
- Fichou Y, Férec C (2006). "The potential of oligonucleotides for therapeutic applications". Trends in Biotechnology 24 (12): 563–70. doi:10.1016/j.tibtech.2006.10.003. PMID 17045686.
پیوند به بیرون[ویرایش]
| در ویکیانبار پروندههایی دربارهٔ آرانای موجود است. |
