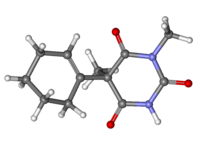
هگزوباربیتال
 | |
 | |
| دادههای بالینی | |
|---|---|
| نامهای تجاری | Hexobarbital, Hexobarbitone, Methylhexabital, Methexenyl, Evipal |
| کد ATC | |
| وضعیت قانونی | |
| وضعیت قانونی | |
| دادههای فارماکوکینتیک | |
| پیوند پروتئینی | ۲۵٪ |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| دراگبنک | |
| کماسپایدر | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.000.241 |
| دادههای فیزیکی و شیمیایی | |
| فرمول شیمیایی | C۱۲H۱۶N۲O۳ |
| جرم مولی | ۲۳۶٫۲۷۱ g·mol−1 |
| مدل سه بعدی (جیمول) | |
| دستسانی | مخلوط راسمیک |
| چگالی | ۱٫۱۶۲۳ g/cm3 |
| نقطه ذوب | ۱۴۶٫۵ درجه سلسیوس (۲۹۵٫۷ درجه فارنهایت) |
| نقطه جوش | ۳۷۸٫۷۳ درجه سلسیوس (۷۱۳٫۷۱ درجه فارنهایت) |
| حلالیت در آب | ۰٫۴۳۵میلیگرم در میلیلیتر (دمای C°۲۰) |
| |
| |
| (صحتسنجی) | |
هگزوباربیتال (انگلیسی: Hexobarbital) یا هگزوباربیتون که به هر دو شکل نمک اسیدی و سدیمی بهعنوان Citopan, Evipan و Tobinal فروخته میشود، یک مشتق باربیتورات است که دارای اثرات خوابآور و آرامبخش است. این دارو در دهههای ۱۹۴۰ و ۱۹۵۰ میلادی بهعنوان عاملی برای القای بیهوشی برای جراحی، و همچنین یک خوابآور سریع و کوتاهمدت برای استفاده عمومی مورد استفاده قرار گرفت و تأثیرات نسبتاً سریع و مدت اثر کوتاهی دارد.[۱] باربیتوراتهای مدرن (مانند تیوپنتال) تا حد زیادی جایگزین استفاده از هگزباربیتال به عنوان بیهوشی شدهاند، زیرا امکان کنترل بهتر عمق بیهوشی را فراهم میکنند. هگزوباربیتال هنوز در برخی پژوهشهای علمی به کار میرود.[۲]
تاریخچه[ویرایش]
دسته شیمیایی باربیتوراتها یکی از قدیمیترین داروهای آرامبخش-خوابآور شناخته شده هستند که قدمت آن به معرفی باربیتال در اوایل سده بیستم میلادی بازمیگردد.[۳] در اروپای شرقی، هگزوباربیتال (و سایر باربیتوراتها) بهطور منظم به عنوان دارو توسط زنان باردار که اقدام به خودکشی میکنند استفاده میشود. مدتها تصور میشد که هگزوباربیتال دارای اثرات تراتوژنیک و جنینی بالقوه است. FDA آنها را بهعنوان رده D یا C بارداری طبقهبندی کردهاست. با این حال، برخی پژوهشها نشان میدهند که مصرف هگزوباربیتال ممکن است باعث ناهنجاریهای مادرزادی شود.[۴]
واکنشپذیری[ویرایش]
یکی از ایزوآنزیمهای سیتوکروم P450 توسط ژن CYP2B1 کدگذاری شدهاست، جایی که هگزوباربیتال بستر آن است. هگزوباربیتال و ایزوآنزیم میتوانند از طریق یک واکنش هیدروکسیلاسیون، که در متابولیسم بیگانهبیوتیکها نقش دارد، یک کمپلکس آنزیم-سوبسترا تشکیل دهند. غلظت هگزوباربیتال همچنین در فعالیت اکسیژناز و اکسیداز سیتوکروم P450 میکروزومی کبدی نقش دارد.[۵] تری استیل اولاندومایسین، یک مهارکننده ایزوآنزیم CYP3A4، متابولیسم هگزوباربیتال و فعالیت بیولوژیکی را نیز مهار میکند، که نشاندهنده رابطه نزدیک میان هگزوباربیتال و سیتوکروم P450 است.[۶]
فارماکولوژی[ویرایش]
اثرات بیولوژیکی هگزوباربیتال در درجه نخست به توانایی آن در نفوذ به سیستم عصبی مرکزی بستگی دارد.[۷] هگزوباربیتال میتواند گیرندههای GABAA را مانند همه باربیتوراتها تقویت کند. طی سالها مشخص شدهاست که انانتیومر S(+) هگزوباربیتال گیرندههای GABAA را بهطور موثرتری نسبت به انانتیومر R(-) آن تقویت میکند.[۸] وقتی گابا به گیرنده GABAA متصل میشود، کانالهای یون کلرید بهگونهای باز میشوند که یونهای کلرید میتوانند به درون نورون جریان پیدا کنند.[۹] این امر باعث یک هیپرپلاریزاسیون در پتانسیل غشایی نورون میشود که باعث میشود نورون کمتر بتواند پتانسیل عمل را آغاز کند؛ بنابراین، این نوع گیرنده، گیرنده انتقال دهنده عصبی بازدارنده اصلی در سیستم عصبی مرکزی پستانداران است.[۱۰] به عنوان یک تقویت کننده گیرنده GABAA، هگزوباربیتال به محل اتصال باربیتورات که در کانال یونی کلرید قرار دارد متصل میشود، در نتیجه اتصال GABA و بنزودیازپینها به محل اتصال مربوطه خود را به صورت آلوستریک افزایش میدهد.[۱۱] افزون بر این، هگزوباربیتال باعث باز شدن کانال یونی کلرید به طولانیترین حالت باز یعنی ۹ میلیثانیه میشود و در نتیجه باعث افزایش اثر بازدارندگی پس سیناپسی میشود. بر خلاف گابا، گلوتامات مهمترین انتقالدهنده عصبی تحریککننده در مغز پستانداران است. افزون بر اثر مهاری، هگزوباربیتال، مانند همه باربیتوراتها، گیرندههای AMPA، گیرندههای کاینات، گیرندههای عصبی استیلکولین را مسدود میکند. و مهمتر از همه، باربیتوراتها با ایجاد یک بلوک کانال باز در کانالهای کلسیم فعال با ولتاژ بالا نوع P/Q، آزادسازی گلوتامات را مهار میکنند. در مجموع، هگزوباربیتال با مهار انتشار گلوتامات و تقویت اثر GABA، باعث ایجاد یک اثر مضعف CNS بر روی مغز میشود.[۱۲]
منابع[ویرایش]
- ↑ Lexikon der Neurowissenschaft: Hexobarbital (به آلمانی)
- ↑ Tseilikman VE, Kozochkin DA, Manukhina EB, Downey HF, Tseilikman OB, Misharina ME, et al. (April 2016). "Duration of hexobarbital-induced sleep and monoamine oxidase activities in rat brain: Focus on the behavioral activity and on the free-radical oxidation". General Physiology and Biophysics. 35 (2): 175–83. doi:10.4149/gpb_2015039. PMID 26689857.
- ↑ Timmermann G, Czeizel AE, Bánhidy F, Acs N (2008-02-01). "A study of the teratogenic and fetotoxic effects of large doses of barbital, hexobarbital and butobarbital used for suicide attempts by pregnant women". Toxicology and Industrial Health. 24 (1–2): 109–19. doi:10.1177/0748233708089004. PMID 18818187. S2CID 36948994.
- ↑ "FDA Pregnancy Categories - CHEMM". chemm.nlm.nih.gov. Archived from the original on 27 August 2021. Retrieved 2021-02-27.
- ↑ Heinemeyer G, Nigam S, Hildebrandt AG (November 1980). "Hexobarbital-binding, hydroxylation and hexobarbital-dependent hydrogen peroxide production in hepatic microsomes of guinea pig, rat and rabbit". Naunyn-Schmiedeberg's Archives of Pharmacology. 314 (2): 201–10. doi:10.1007/BF00504539. PMID 7453835. S2CID 37489777.
- ↑ Timbrell JA (2009). Principles of biochemical toxicology. Informa Healthcare. pp. 181. ISBN 978-0-8493-7302-2. OCLC 243818515.
- ↑ Andrews PR, Mark LC (October 1982). "Structural specificity of barbiturates and related drugs". Anesthesiology. 57 (4): 314–20. doi:10.1097/00000542-198210000-00014. PMID 6751157.
- ↑ Yamakura T, Bertaccini E, Trudell JR, Harris RA (2001-04-01). "Anesthetics and ion channels: molecular models and sites of action". Annual Review of Pharmacology and Toxicology. 41 (1): 23–51. doi:10.1146/annurev.pharmtox.41.1.23. PMID 11264449.
- ↑ Sigel E, Steinmann ME (November 2012). "Structure, function, and modulation of GABA(A) receptors". The Journal of Biological Chemistry. 287 (48): 40224–31. doi:10.1074/jbc.R112.386664. PMC 3504738. PMID 23038269.
- ↑ Olsen RW, Sapp DM, Bureau MH, Turner DM, Kokka N (1991). "Allosteric actions of central nervous system depressants including anesthetics on subtypes of the inhibitory gamma-aminobutyric acidA receptor-chloride channel complex". Annals of the New York Academy of Sciences. 625: 145–54. doi:10.1111/j.1749-6632.1991.tb33838.x. PMID 1711804. S2CID 12448489.
- ↑ Löscher W, Rogawski MA (December 2012). "How theories evolved concerning the mechanism of action of barbiturates". Epilepsia. 53 Suppl 8 (s8): 12–25. doi:10.1111/epi.12025. PMID 23205959. S2CID 4675696.
- ↑ Löscher W, Rogawski MA (December 2012). "How theories evolved concerning the mechanism of action of barbiturates". Epilepsia. 53 Suppl 8 (s8): 12–25. doi:10.1111/epi.12025. PMID 23205959. S2CID 4675696.
پیوند به بیرون[ویرایش]
| در ویکیانبار پروندههایی دربارهٔ هگزوباربیتال موجود است. |
