دیانای میتوکندریایی
دیانای میتوکندریایی (mtDNA) گونهای دیانای است که در میتوکندری (راکیزه) سلولهای یوکاریوتی یافت میشود. کار میتوکندری تبدیل انرژی شیمیایی غذا به آدنوزین تریفسفات یعنی صورتی از انرژی است که برای سلول قابل استفاده باشد.
رونویسی[ویرایش]
دیانای میتوکندریایی به وسیلهٔ پلیمراز گاما رونویسی میشود که به وسیلهٔ ژنوم هستهای کد میشود. رونویسی دیانای میتوکندریایی الزاماً با تقسیم میتوکندری همراه نیست. به همین دلیل ممکن است در یک میتوکندری چندین نسخه از ژنوم بهطور جداگانه موجود باشد که به ان کنکاتامر (concatamer) میگویند.[۲]
خاستگاه[ویرایش]
بهنظر میرسد دیانای میتوکندریایی و دیانای هستهای دارای ویژگیهای فرگشتی متفاوتی باشند. دیانایهای میتوکندریایی از ژنومهای حلقوی باکتریهایی که توسط اجداد اولیهٔ سلولهای یوکاریوتی امروزی دربر گرفته شدهاند مشتق شدهاند. این نظریه به نظریهٔ درونهمزیستی (Endosymbiotic theory) معروف است. بهطور تقریبی هر میتوکندری شامل ۲–۱۰ کپی از دیانای میتوکندریایی است.[۳]
در سلولهای جانداران موجود، اکثریت بسیار بزرگی از پروتئینهای موجود در میتوکندری به وسیلهٔ دیانای هسته کد میشوند اما تصور میشود ژنهای برخی از آنها دارای ریشهٔ باکتریایی هستند که طی فرگشت به سلولهای یوکاریوتی منتقل شدهاند.
وراثت میتوکندریایی[ویرایش]
در اغلب پرسلولیها دیانای میتوکندریایی از مادر به ارث میرسد. مکانیسمهای این توارث عبارت است از یک رقیقسازی ساده (یک سلول تخم شامل ۱۰۰ هزار تا یک میلیون مولکول دیانای میتوکندریایی است در صورتی که یک اسپرم تنها شامل ۱۰۰ تا هزار عدد از آنهاست)، کاهش دیانای میتوکندریایی اسپرمی در یک تخم بارور شده و حداقل در تعداد کمی از جانداران ناکامی دیانایهای میتوکندریایی اسپرمی در ورود به تخم، فارغ از اینکه چه مکانیسمی مؤثر واقع شود این الگوی تکوالدی بودن دیانای میتوکندریایی در اکثر جانوران، گیاهان و قارچها دیده شدهاست.
وراثت ماده[ویرایش]
در تولیدمثل جنسی میتوکندری بهطور انحصاری از مادر به ارث میرسد. میتوکندری موجود در اسپرم پستانداران معمولاً پس از لقاح توسط سلول تخم نابود میشود. علاوه بر این بیشتر میتوکندری در پایهٔ دم اسپرم حضور دارد که به منظور به پیش راندن اسپرم استفاده میشود و گاهی دُم در ضمن فرایند لقاح نابود میشود. در ۱۹۹۹ این نتیجه بهدست آمد که میتوکندری اسپرمی والدی (parental) توسط یوبیکوتین (Ubiquitin) علامتگذاری میشود تا در آینده برای انهدام درون جنینی انتخاب شود.[۴]
برخی تکنیکهای لقاح مصنوعی بهویژه تزریق یک اسپرم به درون یک تخمک ممکن است با این فرایند تداخل کند. این حقیقت که دیانای میتوکندریایی از طریق مادری به ارث میرسد محققان را قادر میسازد تا سلسلهٔ نسل مادری را طی زمان ردیابی کنند (به طریق مشابه دیاِناِی کروموزوم Y که از طریق پدری به ارث میرسد برای دنبال کردن سلسلهٔ نسل پدری بهکار میرود). این کار در انسانها به وسیلهٔ آنالیز توالی یک یا چند بخش از نواحی کنترل (HVR1 یا HVR2) بس متغیر (hypervariable)، مولکول دیانای میتوکندریایی و در قالب یک آزمایش دیانای تبارشناسی انجام میشود.HVR1 از حدود ۴۴۰ جفتباز (Base pair) تشکیل شدهاست. این ۴۴۰ جفتباز با نواحی کنترل افراد دیگر (اشخاص دیگر یا منابع موجود در دیتابیس) به منظور مشخص کردن شجرهٔ مادری مقایسه میشوند. vila et al نتایج تحقیقات تبارشناسی نوعی سگ بومی را تا درندگان منتشر کردهاست.[۵] مفهوم حوای میتوکندریایی نیز بر اساس تحلیلی مشابه بنا شد تا از طریق ردیابی نسل در طول زمان ریشهٔ اولیهٔ بشر را کشف کند.
از آنجا که دیانای میتوکندریایی بهطور کامل بکر نمانده و نرخ جهش سریعی دارد، میتواند برای بررسی روابط فرگشتی جانداران مفید واقع شود. در واقع میتوان توالی دیانایهای میتوکندریایی آرانای حامل در گونههای مختلف مشخص کرد و با مقایسهٔ آنها یک درخت فرگشتی ترسیم کرد. از آنجا که دیانای میتوکندریایی از مادر به فرزند منتقل میشود میتوان از آن بهعنوان ابزاری مفید در تحقیقات تبارشناسی برای پیدا کردن اجداد مادری فرد استفاده کرد.
وراثت نر[ویرایش]
مشاهده شدهاست که میتوکندری در بعضی از گونهها مانند صدفها میتواند از پدر به ارث برسد.[۶][۷] همچنین وراثت پدری میتوکندری در برخی حشرات چون مگس میوه،[۸] زنبور عسل[۹] و برخی جیرجیرکها[۱۰] نیز گزارش شدهاست. شواهد حاکی از این هستند که توارث پدری میتوکندری در میان پستانداران بسیار نادر است. بهطور مشخص نتایج ثبت شدهای در مورد موشها موجودند که میتوکندریهای پدری پس زده شدهاند.[۱۱][۱۲] این مسئله در میان گوسفندان[۱۳] و همچنین گاوهای شبیهسازی شده یافت شدهاست[۱۴] و همچنین در یک مورد خاص انسانی.[۱۵]
ساختار[ویرایش]
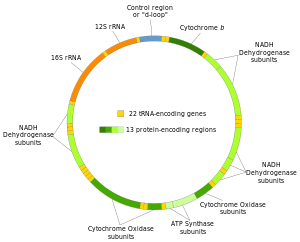
در انسانها و احتمالاً بهطور کلی در همهٔ پرسلولیها در هر سلول بین ۱۰۰ تا ۱۰۰۰۰ کپی متفاوت از دیانای میتوکندریایی موجود است (سلول تخم و اسپرم استثنا هستند). در پستانداران هر مولکول دیانای میتوکندریایی حلقوی ۲رشتهای شامل ۱۵۰۰۰–۱۷۰۰۰ جفتباز است. ۲ رشتهٔ دیانای میتوکندریایی بر اساس محتوی هستهٔ آنها با هم متفاوت میشوند بهطوریکه رشتهٔ با گوانین بیشتر رشتهٔ سنگینتر و رشتهٔ با سیتوزین بیشتر با عنوان رشتهٔ سبک یاد میشوند. در یک مجموع ۳۷ ژنی، رشتهٔ سنگین ۲۸ ژن و رشتهٔ سبک ۹ ژن را کد میکند. در این ۳۷ ژن ۱۳ تا برای پروتئینها (پلیپپتیدها)، ۲۲ تا برای آرانایهای حامل و دو تا برای زیرواحدهای کوچک و بزرگ آرانایهای ریبوزومی هستند. این الگو همچنین در میان اکثر پرسلولیها مشاهده شدهاست. با این وجود در برخی از موارد یکی یا چند مورد از ۳۷ ژن غایباند و محدودهٔ اندازهٔ دیانایهای میتوکندریایی بزرگتر است. حتی در میان گیاهان و قارچها تغییرات بزرگتری در محتوای ژنتیکی و اندازهٔ دیانایهای میتوکندریایی مشاهده شدهاست. همچنین بهنظر میرسد یک زیرمجموعه از ژنها وجود دارد که در همهٔ سلولهای یوکاریوتی حضور دارد (به استثنای بعضی موارد که بهطور کلی میتوکندری ندارند). برخی گونههای گیاهی مقادیر بسیار زیادی دیانای میتوکندریایی دارند (۲۵۰۰۰۰۰ جفتباز در مولکول دیانای میتوکندریایی) با این وجود به طرز غیرمنتظرهای حتی این دیانایهای میتوکندریایی بزرگ، تعداد و انواع برابری ژن در مقایسه با گیاهان با دیانای میتوکندریایی کوچکتر دارند.[۱۶]
ژنها[ویرایش]
زنجیرهٔ انتقال[ویرایش]
ژنوم میتوکندریایی شامل ۱۳ ژن کدکنندهٔ پروتئین است. بسیاری از این ژنها زنجیرهٔ انتقال را کد میکنند.
| دستهها | ژنها |
| NADH dehydrogenase (complex I) |
MT-ND1, MT-ND2, MT-ND3, MT-ND4, MT-ND4L, MT-ND5, MT-ND6 |
| Coenzyme Q - cytochrome c reductase/Cytochrome b (complex III) |
MT-CYB |
| سیتوکروم اکسیداز (complex IV) |
MT-CO1 , MT-CO2 , MT-CO3 |
| ایتیپی سنتاز | MT-ATP6, MT-ATP8 |
آرانای ریبوزومی (rRNA)[ویرایش]
آرانای ریبوزومی میتوکندریایی توسط MT-RNR1 (12s) و MT-RNR2 (16s) کد میشود.
آرانای حامل (tRNA)[ویرایش]
ژنهای زیر، آرانای حامل را کد میکنند:
| اسید آمینه | 3-Letter | 1-Letter | MT DNA |
|---|---|---|---|
| آلانین | Ala | A | MT-TA |
| آرژینین | Arg | R | MT-TR |
| آسپاراژین | Asn | N | MT-TN |
| اسید آسپارتیک | Asp | D | MT-TD |
| سیستئین | Cys | C | MT-TC |
| گلوتامیک اسید | Glu | E | MT-TE |
| گلوتامین | Gln | Q | MT-TQ |
| گلایسین | Gly | G | MT-TG |
| هیستیدین | His | H | MT-TH |
| ایزولوسین | Ile | I | MT-TI |
| لوسین | Leu | L | MT-TL1, MT-TL2 |
| لیزین | Lys | K | MT-TK |
| متیونین | Met | M | MT-TM |
| فنیلآلانین | Phe | F | MT-TF |
| پرولین | Pro | P | MT-TP |
| سرین | Ser | S | MT-TS1, MT-TS2 |
| ترئونین | Thr | T | MT-TT |
| تریپتوفان | Trp | W | MT-TW |
| تیروزین | Tyr | Y | MT-TY |
| والین | Val | V | MT-TV |
جهش[ویرایش]

بیماریهای ژنتیکی[ویرایش]
جهش در mtDNA میتواند منجر بهشماری از بیماریهای ژنتیکی مانند exercise intolerance و سندروم کرنز-سایر (kss) شود که میتواند سبب کاهش کارکرد قلب، چشمها و حرکات ماهیچه شود. برخی شواهد حاکی از انند که این نقصها نقش اساسی در فرایند پیری دارند.[۱۷]
کاربرد در شناسایی[ویرایش]
در انسانها دیانای میتوکندریایی، تعداد ۱۶۵۶۹ بلوک سازندهٔ دیانای (جفتهای باز) را شامل میشود[۱۸] که نمایش دهندهٔ بخشی از مجموع دیانای موجود در سلول است. برخلاف دیانای هسته که از هر دو والد به ارث میرسد و در آن ژنها طی فرایند نوترکیبی چینشی تازه مییابند در دیانای میتوکندریایی معمولاً از والد به فرزند تغییری مشاهده نمیشود. با این وجود دیانای میتوکندریایی نیز دچار نوترکیبی میشود و این کار را با کپیهایی از خودش در یک میتوکندری واحد انجام میدهد. به این دلیل و نیز بهدلیل اینکه در جانوران، دیانای میتوکندریایی نرخ جهش بالاتری نسبت به دیانای هسته دارد[۱۹] مولکول دیانای میتوکندریایی ابزاری قوی برای ردیابی نسلها از طریق مادری است و از این طریق برای جستجوی اجداد بسیاری از گونهها در طول صدها نسل بهکار میرود. دیانای میتوکندریایی انسان همچنین میتواند برای شناسایی افراد بهکار رود.[۲۰] مراکز پزشکی قانونی گاهی۰ مقایسههای دیانای میتوکندریایی را برای شناسایی بقایای انسانی و به ویژه شناسایی بقایای اسکلتهای قدیمی به کار میبرند. گرچه دیانای میتوکندریایی برخلاف دیانای هسته تنها مختص به یک شخص نیست اما میتوان با استفاده مشترک از ان و شواهد دیگر (مانند شواهد ریختشناسی، شواهد مکانی و…) عمل شناسایی را انجام داد. همچنین به عنوان گواهی سلبی نیز عمل میکند.[۲۱] بسیاری از محققان معتقدند دیانای میتوکندریایی نسبت به دیانای هستهای ابزار بهتری برای شناسایی بقایای اسکلتهای قدیمی است زیرا بهدلیل وجود کپیهای زیاد از دیانای میتوکندریایی در سلول احتمال بهدست آوردن یک نمونهٔ مفید افزایش مییابد و به این خاطر که یک همسانی با یک ارتباط زنده بسیار محتمل است حتی اگر فواصل نسلی مادری زیادی آنها را از هم جدا کند. جسد یک تبهکار معروف آمریکایی از همین طریق و به وسیلهٔ مقایسهٔ دیانای میتوکندریایی او با یکی از بستگان مسیر دختری وی مشخص شد.[۲۲] همینطور تشخیص هویت برخی از اعضای خاندان سلطنتی روسیه بهوسیلهٔ مقایسه با اقوام مادری آنها.[۲۳]
میزان کم جمعیت مؤثر و نرخ جهش سریع (در جانوران) دیانای میتوکندریایی را برای یافتن روابط ژنتیکی بین افراد و گروهها در یک گونهٔ خاص و همچنین شناسایی و دستهبندی فیلوژنی بین گونههای مختلف ابزاری مناسب ساختهاست البته مشروط به اینکه این گونهها ارتباطشان از هم خیلی دور نباشد. این کار به این شکل صورت میگیرد که ابتدا توالی دیانای میتوکندریایی افراد یا گونههای مختلف مشخص میشود و آنگاه بر حسب رابطهای که این توالیها با هم دارند شبکهای ایجاد میشود که درخت فیلوژنتیک نام دارد.
تاریخچه[ویرایش]
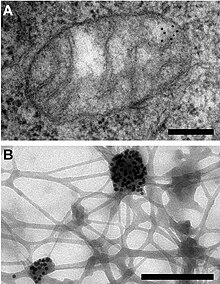
دیانای میتوکندریایی در ۱۹۶۰ توسط مارگریت ام.کی. ناس و سیلوان ام. کی ناس و به وسیلهٔ میکروسکوپ الکترونی[۲۴] و همچنین توسط الن هاسلبروز، هانس تاپی و گاتفرید شاتز بهوسیلهٔ آزمایشهای بیوشیمیایی روی بخشهای بهشدت خالص شدهٔ میتوکندری کشف گردید.[۲۵]
جستارهای وابسته[ویرایش]
منابع[ویرایش]
- ↑ Iborra, Francisco J.; Kimura, Hiroshi; Cook, Peter R. (24 مه 2004). "The functional organization of mitochondrial genomes in human cells". BMC Biology. 2 (1): 9. doi:10.1186/1741-7007-2-9. ISSN 1741-7007.
- ↑ مهدوی، موسوی، اردستانی، صادقیزاده، زیستشناسی سلولی مولکولی و مهندسی ژنتیک/ خانه زیستشناسی
- ↑ Wiesner, R. J.; Rüegg, J. C.; Morano, I. (16 مارس 1992). "Counting target molecules by exponential polymerase chain reaction: copy number of mitochondrial DNA in rat tissues". Biochemical and Biophysical Research Communications. 183 (2): 553–559. doi:10.1016/0006-291x(92)90517-o. ISSN 0006-291X. PMID 1550563.
- ↑ Sutovsky, P.; Moreno, R. D.; Ramalho-Santos, J.; Dominko, T.; Simerly, C.; Schatten, G. (25 نوامبر 1999). "Ubiquitin tag for sperm mitochondria". Nature. 402 (6760): 371–372. doi:10.1038/46466. ISSN 0028-0836. PMID 10586873.
- ↑ Vilà, C.; Savolainen, P.; Maldonado, J. E.; Amorim, I. R.; Rice, J. E.; Honeycutt, R. L.; Crandall, K. A.; Lundeberg, J.; Wayne, R. K. (13 ژوئن 1997). "Multiple and ancient origins of the domestic dog". Science (New York, N.Y.). 276 (5319): 1687–1689. doi:10.1126/science.276.5319.1687. ISSN 0036-8075. PMID 9180076.
- ↑ Hoeh, W. R.; Blakley, K. H.; Brown, W. M. (22 مارس 1991). "Heteroplasmy suggests limited biparental inheritance of Mytilus mitochondrial DNA". Science (New York, N.Y.). 251 (5000): 1488–1490. doi:10.1126/science.1672472. ISSN 0036-8075. PMID 1672472.
- ↑ Penman, Danny. «Mitochondria can be inherited from both parents». New Scientist (به انگلیسی). دریافتشده در ۲۰۲۳-۰۷-۱۹.
- ↑ Kondo, R.; Matsuura, E. T.; Chigusa, S. I. (Summer 1992). "Further observation of paternal transmission of Drosophila mitochondrial DNA by PCR selective amplification method". Genetical Research. 59 (2): 81–84. doi:10.1017/s0016672300030287. PMID 1628820.
- ↑ Meusel MS, Moritz RF (1993). «Transfer of paternal mitochondrial DNA during fertilization of honeybee (Apis mellifera L.) eggs". Curr. Genet. 24 (6): 539–43. doi:10.1007/BF00351719. PMID 8299176.
- ↑ Fontaine, KM, Cooley, JR, Simon, C (2007). «Evidence for paternal leakage in hybrid periodical cicadas (Hemiptera: Magicicada spp.)". PLoS One. 9 (9): e892. doi:10.1371/journal.pone.0000892. PMC 1963320. PMID 17849021.
- ↑ Gyllensten, U.; Wharton, D.; Josefsson, A.; Wilson, A. C. (18 ژوئیه 1991). "Paternal inheritance of mitochondrial DNA in mice". Nature. 352 (6332): 255–257. doi:10.1038/352255a0. ISSN 0028-0836. PMID 1857422.
- ↑ Shitara, H.; Hayashi, J. I.; Takahama, S.; Kaneda, H.; Yonekawa, H. (Spring 1998). "Maternal inheritance of mouse mtDNA in interspecific hybrids: segregation of the leaked paternal mtDNA followed by the prevention of subsequent paternal leakage". Genetics. 148 (2): 851–857. doi:10.1093/genetics/148.2.851. ISSN 0016-6731. PMC 1459812. PMID 9504930.
- ↑ Zhao, X.; Li, N.; Guo, W.; Hu, X.; Liu, Z.; Gong, G.; Wang, A.; Feng, J.; Wu, C. (Winter 2004). "Further evidence for paternal inheritance of mitochondrial DNA in the sheep (Ovis aries)". Heredity. 93 (4): 399–403. doi:10.1038/sj.hdy.6800516. ISSN 0018-067X. PMID 15266295.
- ↑ Steinborn R, Zakhartchenko V, Jelyazkov J, et al. (1998). «Composition of parental mitochondrial DNA in cloned bovine embryos". FEBS Lett. 426 (3): 352–6. doi:10.1016/S0014-5793(98)00350-0. PMID 9600265.
- ↑ Schwartz M, Vissing J (2002). «Paternal inheritance of mitochondrial DNA". N. Engl. J. Med. 347 (8): 576–80. doi:10.1056/NEJMoa020350. PMID 12192017.
- ↑ Ward BL, Anderson RS, Bendich AJ (September 1981). «The mitochondrial genome is large and variable in a family of plants (cucurbitaceae)". Cell 25 (3): 793–803. doi:10.1016/0092-8674(81)90187-2. PMID 6269758. Retrieved 2010-08-09.
- ↑ Alexeyev, Mikhail F. ; LeDoux, Susan P. ; Wilson, Glenn L. (July 2004). «Mitochondrial DNA and aging". Clinical Science 107 (4): 355–364. doi:10.1042/CS20040148. PMID 15279618.
- ↑ Reguly B, Jakupciak JP, Parr RL. 3.4 kb mitochondrial genome deletion serves as a surrogate predictive biomarker for prostate cancer in histopathologically benign biopsy cores. Can Urol Assoc J. 2010 Oct;4(5):E118-22. PMID PMID 20944788; PMID Central. PMID 2950771.
- ↑ Robinson K, Creed J, Reguly B, Powell C, Wittock R, Klein D, Maggrah A, Klotz L, Parr RL, Dakubo GD. Accurate prediction of repeat prostate biopsy outcomes by a mitochondrial DNA deletion assay. Prostate Cancer Prostatic Dis. 2010 Jun;13(2):126-31. Epub 2010 Jan 19. PMID. PMID 20084081.
- ↑ «نسخه آرشیو شده». بایگانیشده از اصلی در ۱۳ اوت ۲۰۱۱. دریافتشده در ۵ ژوئن ۲۰۱۱.
- ↑ Brown WM, George M Jr. , Wilson AC (1979). «Rapid evolution of mitochondrial DNA". Proc Natl Acad Sci USA 76 (4): 1967–1971. doi:10.1073/pnas.76.4.1967. PMC 383514. PMID 109836.
- ↑ Brown WM (1980). «Polymorphism in mitochondrial DNA of humans as revealed by restriction endonuclease analysis". Proc Natl Acad Sci USA 77 (6): 3605–3609. doi:10.1073/pnas.77.6.3605. PMC 349666. PMID 6251473.
- ↑ Paleo-DNA Laboratory - Forensic Services
- ↑ Gill P, Ivanov PL, Kimpton C, et al. (February 1994). «Identification of the remains of the Romanov family by DNA analysis". Nat. Genet. 6 (2): 130–5. doi:10.1038/ng0294-130. PMID 8162066.
- ↑ The details of the tests were published at Gil et al. , 'Identification of the Remains' The Duke of Fife was officially named as the source of the comparison sample of mtDNA in Ivanov, 'Mitochondrial DNA', p. 419.
