روتاویروس: تفاوت میان نسخهها
جز ابرابزار |
بدون خلاصۀ ویرایش |
||
| خط ۱۸۷: | خط ۱۸۷: | ||
== در حیوانات == |
== در حیوانات == |
||
روتاویروسها بسیاری از گونههای [[جانوران]] را در جوانیشان آلوده میکنند و عامل اصلی اسهال در حیوانات وحشی یا پرورش یافته و اهلی در سراسر جهان هستند.<ref name="ISBN 0-12-375158-62"/> روتاویروسها به عنوان یک عامل بیماریزای [[دام (جانور)|دام]]، به ویژه در [[گوساله]]ها و [[خوک|خوکچه]]های جوان، به دلیل هزینههای [[درمان]] و مرگ و میر بالا، زیان اقتصادی بسیاری به کشاورزان وارد میکنند.<ref name="pmid 197818722">{{cite journal|vauthors=Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M|year=2010|title=Zoonotic aspects of rotaviruses|url=https://hal.archives-ouvertes.fr/hal-00556058/document|journal=Veterinary Microbiology|volume=140|issue=3–4|pages=246–255|doi=10.1016/j.vetmic.2009.08.028|pmid=19781872}}</ref> روتاویروسهای حیوانی، مخزن بالقوهای برای تبادل ژنتیکی با روتاویروسهای انسانی هستند.<ref name="pmid 197818723">{{cite journal|vauthors=Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M|year=2010|title=Zoonotic aspects of rotaviruses|url=https://hal.archives-ouvertes.fr/hal-00556058/document|journal=Veterinary Microbiology|volume=140|issue=3–4|pages=246–255|doi=10.1016/j.vetmic.2009.08.028|pmid=19781872}}</ref> شواهدی وجود دارد که روتاویروسهای حیوانی میتوانند چه از طریق انتقال مستقیم<ref name="pmid 174161322">{{cite journal|vauthors=Müller H, Johne R|year=2007|title=Rotaviruses: diversity and zoonotic potential—a brief review|journal=Berliner und Munchener Tierarztliche Wochenschrift|volume=120|issue=3–4|pages=108–112|pmid=17416132}}</ref> یا با کمک ایجاد کردن ویروسهای تغییر کرده ([[جهشیافته]]) از سویههای انسانی<ref name="pmid 150663292">{{cite journal|vauthors=Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J|year=2004|title=The zoonotic potential of rotavirus|url=http://researchonline.rvc.ac.uk/id/eprint/1175/|journal=The Journal of Infection|volume=48|issue=4|pages=289–302|doi=10.1016/j.jinf.2004.01.018|pmid=15066329}}</ref> به کمک انتقال توالیهای RNA خود به آنها، انسان را آلوده کنند.<ref name="pmid 264282612">{{cite journal|vauthors=Dóró R, Farkas SL, Martella V, Bányai K|year=2015|title=Zoonotic transmission of rotavirus: surveillance and control|journal=Expert Review of Anti-infective Therapy|volume=13|issue=11|pages=1337–1350|doi=10.1586/14787210.2015.1089171|pmid=26428261|s2cid=42693014}}</ref> |
روتاویروسها بسیاری از گونههای [[جانوران]] را در جوانیشان آلوده میکنند و عامل اصلی اسهال در حیوانات وحشی یا پرورش یافته و اهلی در سراسر جهان هستند.<ref name="ISBN 0-12-375158-62"/> روتاویروسها به عنوان یک عامل بیماریزای [[دام (جانور)|دام]]، به ویژه در [[گوساله]]ها و [[خوک|خوکچه]]های جوان، به دلیل هزینههای [[درمان]] و مرگ و میر بالا، زیان اقتصادی بسیاری به کشاورزان وارد میکنند.<ref name="pmid 197818722">{{cite journal|vauthors=Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M|year=2010|title=Zoonotic aspects of rotaviruses|url=https://hal.archives-ouvertes.fr/hal-00556058/document|journal=Veterinary Microbiology|volume=140|issue=3–4|pages=246–255|doi=10.1016/j.vetmic.2009.08.028|pmid=19781872}}</ref> روتاویروسهای حیوانی، مخزن بالقوهای برای تبادل ژنتیکی با روتاویروسهای انسانی هستند.<ref name="pmid 197818723">{{cite journal|vauthors=Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M|year=2010|title=Zoonotic aspects of rotaviruses|url=https://hal.archives-ouvertes.fr/hal-00556058/document|journal=Veterinary Microbiology|volume=140|issue=3–4|pages=246–255|doi=10.1016/j.vetmic.2009.08.028|pmid=19781872}}</ref> شواهدی وجود دارد که روتاویروسهای حیوانی میتوانند چه از طریق انتقال مستقیم<ref name="pmid 174161322">{{cite journal|vauthors=Müller H, Johne R|year=2007|title=Rotaviruses: diversity and zoonotic potential—a brief review|journal=Berliner und Munchener Tierarztliche Wochenschrift|volume=120|issue=3–4|pages=108–112|pmid=17416132}}</ref> یا با کمک ایجاد کردن ویروسهای تغییر کرده ([[جهشیافته]]) از سویههای انسانی<ref name="pmid 150663292">{{cite journal|vauthors=Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J|year=2004|title=The zoonotic potential of rotavirus|url=http://researchonline.rvc.ac.uk/id/eprint/1175/|journal=The Journal of Infection|volume=48|issue=4|pages=289–302|doi=10.1016/j.jinf.2004.01.018|pmid=15066329}}</ref> به کمک انتقال توالیهای RNA خود به آنها، انسان را آلوده کنند.<ref name="pmid 264282612">{{cite journal|vauthors=Dóró R, Farkas SL, Martella V, Bányai K|year=2015|title=Zoonotic transmission of rotavirus: surveillance and control|journal=Expert Review of Anti-infective Therapy|volume=13|issue=11|pages=1337–1350|doi=10.1586/14787210.2015.1089171|pmid=26428261|s2cid=42693014}}</ref> |
||
== تاریخچه == |
|||
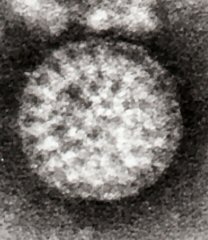
[[پرونده:Flewett_Rotavirus.jpg|بندانگشتی|یکی از میکروگرافهای الکترونی اصلی هنری فلویت که یک ذره روتاویروس را نشان میدهد. هنگامی که روتاویروسها توسط میکروسکوپ الکترونی رنگ آمیزی منفی بررسی میشوند، اغلب شبیه چرخ هستند.]] |
|||
در سال ۱۹۴۳، ژاکوب لایت و هوراس هودز ثابت کردند که یک عامل قابل پالایش در مدفوع کودکان مبتلا به اسهال عفونی باعث اسهال دامی در گاوها نیز میگردد.<ref name="pmid 18015921">{{Cite journal|vauthors=Light JS, Hodes HL|year=1943|title=Studies on Epidemic Diarrhea of the New-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves|journal=American Journal of Public Health and the Nation's Health|volume=33|issue=12|pages=1451–1454|doi=10.2105/AJPH.33.12.1451|pmc=1527675|pmid=18015921}}</ref> سه دهه بعد، بررسی نمونهها نشان داده که عامل بیماریزا روتاویروسها هستند.<ref name="pmid 184047">{{Cite journal|vauthors=Mebus CA, Wyatt RG, Sharpee RL, Sereno MM, Kalica AR, Kapikian AZ, Twiehaus MJ|year=1976|title=Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis|url=http://iai.asm.org/cgi/reprint/14/2/471|format=PDF|journal=Infection and Immunity|volume=14|issue=2|pages=471–474|doi=10.1128/IAI.14.2.471-474.1976|pmc=420908|pmid=184047}}</ref> در سالهای بعد، مشخص شد که یک ویروس در موش<ref name="pmid 4998842">{{Cite journal|vauthors=Rubenstein D, Milne RG, Buckland R, Tyrrell DA|year=1971|title=The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium|journal=British Journal of Experimental Pathology|volume=52|issue=4|pages=442–445|pmc=2072337|pmid=4998842}}</ref> با ویروس ایجاد کنندهٔ اسهال دامی مرتبط است.<ref name="pmid 965097">{{Cite journal|vauthors=Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB|year=1976|title=Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals|url=http://iai.asm.org/cgi/reprint/14/3/804|format=PDF|journal=Infection and Immunity|volume=14|issue=3|pages=804–810|doi=10.1128/IAI.14.3.804-810.1976|pmc=420956|pmid=965097}}</ref> در سال ۱۹۷۳، [[روت بیشاپ|روث بیشاپ]] و همکارانش ویروسهای مرتبطی را که در کودکان مبتلا به گاستروانتریت یافت میشود، طبقهبندی کردند.<ref name="pmid 19799704">{{Cite journal|last=Bishop R|year=2009|title=Discovery of rotavirus: Implications for child health|journal=Journal of Gastroenterology and Hepatology|volume=24|issue=Suppl 3|pages=S81–S85|doi=10.1111/j.1440-1746.2009.06076.x|pmid=19799704|doi-access=free}}</ref> |
|||
در سال ۱۹۷۴، [[توماس هنری فلویت]] پس از مشاهده این موضوع که ذرات روتاویروس در هنگام مشاهده از طریق [[میکروسکوپ الکترونی]] مانند یک چرخ (''rota'' در زبان لاتین) به نظر میرسند، نام ''روتاویروس'' را برای آنان پیشنهاد کرد.<ref name="pmid 77663">{{Cite journal|vauthors=Flewett TH, Woode GN|year=1978|title=The rotaviruses|journal=Archives of Virology|volume=57|issue=1|pages=1–23|doi=10.1007/BF01315633|pmc=7087197|pmid=77663}}</ref><ref name="pmid 4137164">{{Cite journal|vauthors=Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM|year=1974|title=Relation between viruses from acute gastroenteritis of children and newborn calves|journal=The Lancet|volume=304|issue=7872|pages=61–63|doi=10.1016/S0140-6736(74)91631-6|pmid=4137164}}</ref> چهارسال بعد، این نام بهطور رسمی توسط [[کمیته بینالمللی طبقهبندی ویروسها]] به رسمیت شناخته شد.<ref name="pmid 43850">{{Cite journal|last=Matthews RE|year=1979|title=Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses|journal=Intervirology|volume=12|issue=3–5|pages=129–296|doi=10.1159/000149081|pmid=43850|doi-access=free}}</ref> در سال ۱۹۷۶، ویروسهای مرتبط در چندین گونه دیگر از حیوانات طبقهبندی شد.<ref name="pmid 9650972">{{Cite journal|vauthors=Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB|year=1976|title=Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals|url=http://iai.asm.org/cgi/reprint/14/3/804|format=PDF|journal=Infection and Immunity|volume=14|issue=3|pages=804–810|doi=10.1128/IAI.14.3.804-810.1976|pmc=420956|pmid=965097}}</ref> این ویروسها که همگی باعث گاستروانتریت حاد میشوند، به عنوان یک عامل بیماریزای جمعی در انسان و سایر حیوانات در سراسر جهان شناخته شدند.<ref name="pmid 77663"/> سروتیپهای روتاویروس برای اولین بار در سال ۱۹۸۰ توصیف شدند<ref name="pmid 2833405">{{Cite journal|vauthors=Beards GM, Brown DW|year=1988|title=The antigenic diversity of rotaviruses: significance to epidemiology and vaccine strategies|journal=European Journal of Epidemiology|volume=4|issue=1|pages=1–11|doi=10.1007/BF00152685|pmid=2833405}}</ref> و در سال بعد، روتاویروسهای انسان برای اولین بار در [[کشت سلول|کشت سلولی]] مشتق شده از کلیه میمونها با افزودن [[تریپسین]] (آنزیم یافتشده در [[دوازدهه]] [[پستانداران]] و پروتئینی ضروری برای تکثیر روتاویروس) در محیط آزمایشگاهی کشت داده شدند.<ref name="pmid 6273696">{{Cite journal|vauthors=Urasawa T, Urasawa S, Taniguchi K|year=1981|title=Sequential passages of human rotavirus in MA-104 cells|journal=Microbiology and Immunology|volume=25|issue=10|pages=1025–1035|doi=10.1111/j.1348-0421.1981.tb00109.x|pmid=6273696|doi-access=free}}</ref> قابلیت تکثیر روتاویروسها در محیط کشت، تحقیقات را سرعت بخشید و در اواسط دهه ۱۹۸۰ اولین واکسنهای نامزدشده مورد ارزیابی قرار گرفتند.<ref name="pmid 19072246">{{Cite journal|vauthors=Ward RL, Bernstein DI|year=2009|title=Rotarix: a rotavirus vaccine for the world|journal=Clinical Infectious Diseases|volume=48|issue=2|pages=222–228|doi=10.1086/595702|pmid=19072246|doi-access=free}}</ref> |
|||
== جستارهای وابسته == |
== جستارهای وابسته == |
||
نسخهٔ ۲۷ ژانویهٔ ۲۰۲۴، ساعت ۱۷:۲۴
| روتاویروس | |
|---|---|
| |
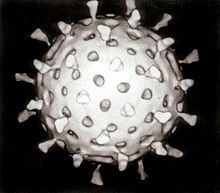
| بازسازی روتاویروس به کمک کامپیوتر بر اساس چندین میکروگراف الکترونی | |
| طبقهبندی ویروسها | |
| زیر خانواده: | سدورئوویرینه |
| سرده: | روتاویروس |
| گونهها | |
| |
روتاویروس (نام علمی: Rotavirus) شایعترین علت بیماریهای اسهالی در میان نوزادان و خردسالان است[۱] با این حال بزرگسالان را به ندرت تحت تأثیر قرار میدهد.[۲] تقریباً هر کودک در جهان حداقل یک بار قبل از پنج سالگی به روتاویروس مبتلا میشود.[۳] سرعت تغییر تکامل این ویروس پایین و ایمنی بعد از وقوع هر عفونت، فعال و ماندگار است، بنابراین ابتلاهای بعدی فرد شدت کمتری دارند.[۲] روتاویروس یک نوع از ویروسهای RNA دو رشتهای در خانواده رئوویروسها بوده و دارای ژنوم مُقطع (۱۱ قطعه) دو رشتهای و کپسید ایکوسادرال غیر لیپیدی است. نُه گونه از روتاویروسها وجود دارد که با نامهای A, B، C, D، F, G، H, I و J شناخته میشوند. ابتلا به روتاویروس A، شایعترین نوع این بیماری بوده و علت بیش از ۹۰ درصد عفونتهای روتاویروسی در انسان است.[۴]
این ویروس از طریق مسیر مدفوعی-دهانی انتقال مییابند، سلولهای روده باریک را آلوده کرده، به آنها آسیب رسانده و گاستروانتریت ایجاد میکند (علیرغم اینکه ارتباطی با آنفلوانزا ندارد، اغلب به آن «آنفلوانزای معده» شناخته میشود). با وجود اینکه روتاویروس عامل بستری شدن تقریباً یک سوم از نوزادان و کودکان به دلیل ابتلا به اسهال شدید بوده؛[۵] اهمیت پیشگیری و درمان آن در بهداشت عمومیِ جامعه به ویژه در کشورهای در حال توسعه دست کم گرفته شدهاست.[۶] این ویروس علاوه بر تأثیری بر سلامت انسان، توانایی بیماریزایی در سایر حیوانات از جمله دامها را نیز دارد.[۷] روتاویروس در سال ۱۹۷۳ توسط روت بیشاپ و همکارانش به وسیله میکروگراف الکترونی کشف شد.[۸]
اِنتریت روتاویروسی معمولاً در دوران کودکی به راحتی قابل کنترل و درمان است، اما در کودکان زیر ۵ سال میتواند وخیم و در مواردی سبب مرگ بیمار شود. این ویروس علت مرگ ۱۵۱۷۱۴ نفر بر اثر اسهال (کمآب شدن بدن) در سال ۲۰۱۹ بودهاست؛[۹] در ایالات متحده، قبل از شروع برنامه واکسیناسیون روتاویروس در دهه ۲۰۰۰، عامل حدود ۲٫۷ میلیون مورد گاستروانتریت شدید در کودکان، تقریباً ۶۰۰۰۰ مورد بستری در بیمارستان و حدود ۳۷ مرگ در هر سال میشد.[۱۰] پس از معرفی واکسن روتاویروس، نرخ بستریهای ناشی از این بیماری در بیمارستانها بهطور قابل توجهی کاهش یافتهاست.[۱۱][۱۲] کمپینهای ارتقای بهداشت عمومی برای مبارزه با روتاویروس بر ارائه درمان به کمک نمک آبرسان خوراکی (ORS) برای کودکان آلوده و واکسیناسیون برای جلوگیری از این بیماری تمرکز دارد.[۱۳] بروز و شدت عفونتهای روتاویروس در کشورهایی که واکسن روتاویروس را به سیاستهای معمول ایمنسازی کودکان اضافه کردهاند بهطور قابل توجهی کاهش یافتهاست.[۱۴][۱۵][۱۶]
ویروسشناسی
انواع
نُه گونه روتاویروس به صورت A, B، C, D، F, G، H, I و J وجود دارد.[۱۷][۱۸] انسانها عمدتاً توسط روتاویروس A آلوده میشوند و گونههای A تا I عامل بیماری و عفونت در دیگر حیوانات،[۱۹] برای مثال گونه H در خوکها،[۲۰] D, F و G در پرندگان،[۲۱] I در گربه ها[۲۲] و J در خفاشها هستند.[۲۳]
در گونه روتاویروس A سویههای مختلفی وجود دارد که سروتیپ آنها را همانند ویروس آنفلوانزا، به وسیله سیستم طبقهبندی دوگانه بر اساس دو پروتئین سطحی ویروس تعریف میکنند.[۲۴] گلیکوپروتئین VP7 بیانگر سروتیپهای G و پروتئین حساس به پروتئازِ VP4 بیانگر سروتیپهای P هستند.[۲۵] از آنجایی که دو ژن تعیینکننده نوع G و P میتوانند بهطور جداگانه به ویروسهایی که در سلول تولید میشوند منتقل گردند، ترکیبهای متفاوت ژنومی در روتاویروسها دیده میشود.[۲۶] یک سیستم ژنوتیپی کامل از ژنوم روتاویروس A ایجاد شده که برای تعیین منشأ سویههای غیر معمول به کار میرود.[۲۷] شیوع انواع G و P در بین کشورها و سالهای مختلف متفاوت بودهاست.[۲۸] حداقل ۳۶ سروتیپ نوع G و ۵۱ سروتیپ نوع P وجود دارد؛[۲۹] با این وجود، معمولاً در عفونتهای انسانی فقط چند نمونه از سروتیپهای G و P دیده میشود که شامل G1P8، G2P4، G3P8، G4P8، G9P8 و G12P8 هستند.[۳۰]
ساختار
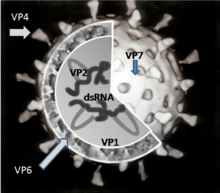
ژنوم روتاویروسها از ۱۱ مولکول مارپیچی دورشتهای منحصر به فرد (RNA دورشتهای یا dsRNA) تشکیل شدهاست که در مجموع ۱۸۵۵۵ نوکلئوتید دارند. هر مارپیچ یا بخش، یک ژن را تشکیل میدهد که بر اساس اندازه از ۱ تا ۱۱ شماره گذاری میشود (۱ بزرگترین و ۱۱ کوچکترین است).[۳۱] به جز ژن ۹ که پروتئینی همچون ژن ۲ را کد میکند هر ژن، ایجادگر یک پروتئین اختصاصی است.[۳۱] ضخامت ویریون ویروسی[توضیح ۱] تا ۷۶٫۵ نانومتر نیز میرسد.[۳۳] روتاویروس توسط یک کپسید پروتئینی ایکوسادرالِ سه لایه بدون پوشش ویروسی احاطه شدهاست.[۳۴][۳۵]
پروتئینها
شش پروتئین ویروسی (VPs) وجود دارد که بخشی از ویریون را تشکیل میدهند. این پروتئینهای ساختاری VP1، VP2، VP3، VP4، VP6 و VP7 نامیده میشوند.[۳۷] علاوه بر VPها، شش پروتئین غیر ساختاری (NSPs) نیز وجود دارد که فقط در سلولهای آلوده به روتاویروس تولید میگردند و شاملNSP1، NSP2، NSP3، NSP4، NSP5 و NSP6 میشوند.[۳۷]
حداقل شش پروتئین از دوازده پروتئینی که توسط ژنوم روتاویروس کدگذاری شدهاند بعد از بلوغ آن به RNA متصل میگردند.[۳۸] نقش این پروتئینها در تکثیر روتاویروس بهطور کامل شناخته نشدهاست؛ با این حال تصور میشود که عملکرد آنها به سنتز و بستهبندی RNA در ویریون، انتقال mRNA به محل تکثیر ژنوم و ترجمه mRNA و تنظیم بیان ژن مربوط باشد.[۳۹]
پروتئینهای ساختاری

VP1 در هسته ویویون ویروسی قرار دارد و یک آنزیم RNA پلیمراز وابسته به RNA است.[۴۰] در یک سلول آلوده، این آنزیم رونوشتهای ژنوم (mRNA) را برای سنتز پروتئینهای ویروسی تولید میکند؛ همچنین بخشهای RNA ژنومی روتاویروس را برای تولید ویریونهای ویروسی جدید همانندسازی میکند.[۴۱] VP2 لایه مرکزی ویریون را تشکیل میدهد و به ژنوم ویروسی (RNA) متصل است.[۴۲]
VP3 یک پروتئین آنزیمی به نام گوانیلیل ترانسفراز بوده که بخشی از قسمت داخلی ویریون را شامل میشود. این آنزیم نقش کاتالیز کلاهک '۵ را پس از رونویسی و در زمان اصلاح mRNA، بر عهده دارد.[۴۳] کلاهک، mRNA آن را در برابر آنزیمهای تجزیه کننده نوکلئیک اسید به نام نوکلئاز که در سلولهای جانداران آلوده شده وجود دارد حفظ میکند.[۴۴]
VP4 روی سطح ویریون قرار دارد و به صورت یک زائده بیرونی (پلپومر ویروسی) در میکروگرافی دیده میشود.[۴۵] این ماده به مولکولهای سطح سلولها (گیرنده) متصل میشود و امکان ورود ویروس به داخل سلول را فراهم میکند.[۴۶] بدن برای جلوگیری از عفونی شدن روده، باید پروتئین VP4 را توسط آنزیم تریپسین (نوعی پروتئاز)، که پیشساز آن در لوزالمعده تولید و به روده ترشح میشود، به VP5* و VP8* تغییر دهد.[۴۷] VP4 مشخص کننده میزان گسترش و ویرولانس روتاویروس است و نوع P سروتیپِ ویروس را ایجاد میکند.[۴۸] در انسان بین گروه خونی (سیستم آنتیژن لوئیس، سیستم گروه خونی ABO و وضعیت ترشح کنندگی آنتیژن[توضیح ۲]) و امکان عفونی شدن بیماری ارتباط وجود دارد.[۵۱] به نظر میرسد که غیر ترشح کنندهها در برابر عفونت سروتیپهای P4 و P8 مقاوم هستند، این مسئله نشان میدهد آنتیژنهای گروه خونی، گیرنده پروتئینهای ویروسی هستند و مقاومت بدن در برابر بیماری به ژنوتیپ روتاویروس و گروه خونی فرد بستگی دارد.[۵۲]
VP6 بخش عمده کپسید را تشکیل میدهد. نقش این پروتئین به عنوان یک آنتیژن بهطور کامل شناخته شدهاست و میتواند برای شناسایی گونه روتاویروس مورد استفاده قرار گیرد.[۵۳] VP6 همچنین برای بررسیهای و تحقیقات آزمایشگاهی در رابطه با عفونت روتاویروس بسیار پر استفاده است.[۵۴] VP7 یک گلیکوپروتئین بوده که سطح خارجی ویریون را تشکیل میدهد. جدا از عملکردهای ساختاری، سروتیپ G سویه را تعیین میکند و همراه با VP4 در مصونیت نسبت به سیستم ایمنی نقش دارد.[۳۳]
پروتئینهای غیر ساختاری
NSP1، محصول تولیدی ژن ۵ بوده و یک پروتئین غیر ساختاری متصل به RNA بهشمار میرود. NSP1 همچنین کارآمدی اینترفرون که بخشی از سیستم ایمنی ذاتی سلولها در برابر عفونت ویروسی است، را از بین میبرد.[۵۵] این پروتئین، وظیفه تجزیه پروتئازوم (یکی از اجزای کلیدی سیگنال دهی برای تحریک تولید اینترفرون در سلول آلوده و پاسخ دهندهٔ ایمنی به اینترفرون ترشح شده توسط سلولهای مجاور) را بر عهده دارد.[۵۵] NSP1 همچنین برای جلوگیری از تولید این سیتوکین در سلول میزبان، چندین فاکتور رونویسی IRF مورد نیاز برای رونویسی ژن اینترفرون را تخریب میکند.[۵۶] NSP2 یک RNAپلیمراز وابسته به RNA است که در انکلوزیونهای سیتوپلاسمی (ویروپلاسم) تجمع مییابد و برای همانندسازی ژنوم مورد نیاز است.[۴۲][۵۷]
NSP3 به mRNAهای ویروسی در سلولهای آلوده متصل میشود و مسئول خاموش کردن سنتز پروتئین سلول میزبان است.[۵۸] NSP3 دو فاکتور ضروری برای شروع ترجمه و سنتز پروتئینها را که بر روی mRNA سلول قرار دارد، غیرفعال میکند؛[۵۸] در ابتدا، «پروتئین متصلشونده به پلیآدنین» (PABP) را که برای ترجمهٔ کارآمد رونوشتهای ژنی با انتهای پلی آدنین '۳ مورد نیاز است (در اکثر رونوشتهای سلول میزبان یافت میشود)، از فاکتورِ شروع ترجمهٔ eIF4F خارج و در ادامه، فاکتور eIF2 را نیز با تحریک آغاز فسفریلاسیون آن غیرفعال میکند.[۵۹] از آنجایی که mRNA روتاویروس فاقد انتهای پلی آدنین '۳ است، برای ترجمه شدن در سلول میزبان، هیچ نیازی به این فاکتورهای آغازی ندارد.[۶۰]
NSP4 اولین انتروتوکسین ویروسی بود که توسط محققین کشف شد.[۶۱] NSP4 همچنین یک ویروپورین بهشمار میرود که Ca+2 سیتوزولی را در سلولهای پستانداران افزایش میدهد.[۶۲] NSP5 توسط ترجمه بخشی از ژن ۱۱ روتاویروسِ A ایجاد میشود و در سلولهای آلوده به ویروس در ویروپلاسم تجمع مییابد.[۶۳] NSP6 نیز یک پروتئین اتصالدهنده بوده و رونوشتِ ژنوم ویروس که یک RNA تک رشتهای (ssRNA) است را به محتوای ژنی سلول پیوند میدهد.[۶۴] این پروتئین توسط ژن ۱۱ تحت یک چارچوب خوانش بازِ خارج از فاز کدگذاری میشود.[۶۵][توضیح ۳]
| شماره RNA (ژنوم) | اندازه (جفتباز) | پروتئین | یونیپروت | وزن مولکولی کیلودالتون | موقعیت | تعداد در هر ویریون | عملکرد |
|---|---|---|---|---|---|---|---|
| ۱ | ۳۳۰۲ | VP1 | P22678 | ۱۲۵ | در بالای بخش مرکزی | ۱۲ | RNA پلیمراز وابسته به RNA |
| ۲ | ۲۶۹۰ | VP2 | A2T3R5 | ۱۰۲ | پوسته داخلی بخش مرکزی را تشکیل میدهد | ۱۲۰ | بخشی از ساختار ژنوم |
| ۳ | ۲۵۹۱ | VP3 | A2T3S5 | ۸۸ | در بالای بخش مرکزی | ۱۲ | آنزیم پوشاننده mRNA (متیل ترانسفراز) |
| ۴ | ۲۳۶۲ | VP4 | A2T3T2 | ۸۷ | پلپومر ویروسی | ۱۸۰ | اتصال به سلول میزبان، بیماریزایی |
| ۵ | ۱۶۱۱ | NSP1 | Q99FX5 | ۵۹ | غیر ساختاری | ۰ | کلاهکگذاری '۵، آنتاگونیست اینترفرون |
| ۶ | ۱۳۵۶ | VP6 | Q6LE89 | ۴۵ | کپسید داخلی | ۷۸۰ | آنتیژن ساختاری گونههای خاص |
| ۷ | ۱۱۰۴ | NSP3 | P03536 | ۳۷ | غیر ساختاری | ۰ | فعالیت mRNA ویروسی را افزایش میدهد و سنتز پروتئین سلولی را متوقف میکند |
| ۸ | ۱۰۵۹ | NSP2 | A2T3P0 | ۳۵ | غیر ساختاری | ۰ | در همانندسازی و بستهبندی RNA نقش دارد |
| ۹ | ۱۰۶۲ | VP71 VP72 | P03533 | ۳۸ و ۳۴ | سطح | ۷۸۰ | آنتیژن ساختاری و مصونیت ایمنی ویروس |
| ۱۰ | ۷۵۱ | NSP4 | P04512 | ۲۰ | غیر ساختاری | ۰ | ویروپورین (انتروتوکسین) |
| ۱۱ | ۶۶۷ | NSP5 NSP6 | A2T3Q9 P11203 | ۲۲ | غیر ساختاری | ۰ | تعدیل کننده اتصال ssRNA و dsRNA، فسفوپروتئینی برای NSP2 |
این جدول بر اساس سویه SA11 روتاویروس میمونسانیان است. تخصیص کدگذاری RNA پروتئین در برخی از سویهها متفاوت است.[نیازمند منبع]
تکثیر

- اتصال ویروس به سلولهای میزبان که با واسطه VP4 و VP7 انجام میشود
- نفوذ کپسید ویروسی به پوشش سلولی
- ایجاد رشته ssRNA سنس مثبت که به عنوان mRNA عمل میکند و عاملی برای سنتز پروتئینهای VP1، VP3 و VP2 است.
- تشکیل ویروپلاسم، بستهبندی RNA ویروسی و سنتز RNA تک رشتهای سنس منفی و تشکیل ویریونهای دو لایه
- تکامل ویریونها و آزادسازی به صورت ویروسهای بالغ
اتصال ویروس به سلول میزبان به کمک VP4 و در نتیجه اتصال به مولکولهایی به نام گلیکان در سطح سلول انجام میگیرد.[۳۵] ویروس با اتصال به این گیرندههای سلولی، اندوسیتوز کرده و وارد سلول میزبان میشود و یک وزیکول به نام اندوزوم را تشکیل میدهد. پس از ورود به درون سلول، پروتئینهای لایه سوم، VP7 و VP4، غشای اندوزوم را شکافته و سبب تغییر غلظت یون کلسیم (Ca+2) در محیط سیتوپلاسمی میشود.[۶۹] این افزایش، باعث تجزیه تریمرهای VP7 به زیر واحدهای پروتئینی منفرد میگردد اما پوشش پروتئینی ایجاد شده توسط VP2 و VP6 همچنان در اطراف dsRNA ویروسی باقی مانده و یک ویریون دو لایه (DLP) را تشکیل میدهد.[۶۹]
یازده رشته dsRNA تحت حفاظتِ دو پوسته پروتئینی به کار خود ادامه میدهند و RNA پلیمراز، رونوشتهای mRNA ویروسی را از روی آنها و به عنوان رابطی برای پروتئین سازی ایجاد میکند.[۷۰] باقی ماندن ژنوم ویروسی در پوشش دو لایه سبب مخفی ماندن آن از سیستم ایمنی سلول، از جمله تداخل RNA در اثر حضور RNA دو رشتهای در سلول میزبان (RNAهای سلولهای انسانی تک رشتهای هستند)، میشود.[۷۰] در طول عفونت، روتاویروس mRNAها را برای بیوسنتز پروتئین و تکثیر ژنوم خود تولید میکنند (روش رونویسی معکوس؛ استفاده از یک واسطه به جای ماده وراثتی اصلی).[۷۱] بیشتر پروتئینهای روتاویروس در ویروپلاسم، جایی که RNA تکثیر و ویریونهای دو لایه ایجاد میشوند، تجمع مییابند.[۷۲]
ویروپلاسم به RNAهای ویروسی کمک میکند بدون هیچ مشکی به عنوان الگوهایی برای سنتز ssRNA ژنومی ویروس استفاده شوند و از تخریب به وسیله ریبونوکلئاز، که پس از اتصال RNAهای کوچک مداخلهگر (siRNA) به مادههای وراثتی ناشناس به کار گرفته میشود، در امان بمانند.[۷۲] ویروپلاسم بهطور معمول دو ساعت پس از عفونت ویروسی در اطراف هسته سلول به وجود میآید و در درون آن کارخانههای ویروسی، احتمالاً، توسط دو پروتئین غیرساختاری ویروسی، NSP5 و NSP2 ساخته میشود.[توضیح ۴][۷۳] سپس ویریونهای دو لایه به شبکه آندوپلاسمی میزبان مهاجرت میکنند و در آنجا سومین لایه بیرونی خود را به کمک پروتئینهای VP7 و VP4 تشکیل میدهند. پس از تکامل ویریونها به ویروس، این میکروبها تحت فرآیندی به نام لیز از سلول میزبان خارج میشوند.[۴۷][۷۴]
انتقال

اسهالِ ویروسی بسیار مسری است.[۷۵] روتاویروسها از طریق مسیر مدفوعی-دهانی و به کمک تماس دستها با سطوح و اشیاء آلوده و احتمالاً از مجرای تنفسی منتقل میشوند.[۷۶] مدفوع یک فرد مبتلا میتواند حاوی بیش از ۱۰ تریلیون ذره عفونی در هر گرم باشد[۵۳] که کمتر از ۱۰۰ مورد از این ذرهها، برای انتقال عفونت به فرد دیگر کافی است.[۲]
روتاویروسها در محیطهای غیر زنده پایدار هستند و میتوانند بین ۹ تا ۱۹ روز این این مکانها زنده بمانند.[۷۷] طی بررسیهای انجام شده در مَصَبها، در هر ۳/۷۹ لیتر آب، مقدار ۱ تا ۵ ذره عفونی از این ویروس وجود دارد.[۷۸] از آنجا که شیوع عفونت روتاویروس در کشورهای دارای استانداردهای بهداشتی بالا و پایین به یک میزان دیده میشود؛[۷۵] احتمال میرود اقدامات بهداشتی که برای از بین بردن باکتریها و انگلها کافی است در کنترل روتاویروس بی اثر باشد.[۷۹]
علائم و نشانهها
انتریت روتاویروس یک بیماری خفیف تا شدید است که با تهوع، استفراغ، اسهال آبکی و تب خفیف مشخص میشود. هنگامی که کودک به ویروس آلوده میگردد، یک دورهٔ کمون حدود دو روز قبل از ظاهر شدن علائم را تجربه میکند.[۸۰] دوره بیماری، طولانی بوده و علائم اغلب با استفراغ شروع میشود و سپس چهار تا هشت روز با اسهال شدید ادامه مییابد. کمآبی در عفونت با روتاویروس نسبت به اکثر موارد ناشی از پاتوژنهای باکتریایی شایع تر بوده و اصلیترین علت مرگ ناشی از عفونت روتاویروس است.[۸۱]
عفونتهای روتاویروسی میتوانند در هر سنی در طول زندگی رخ دهند؛[۵۳][۸۲] اولین مورد ابتلا معمولاً علائمی شدید را به همراه دارد، اما عفونتهای بعدی به دلیل شکلگیری ایمنی فعال معمولاً خفیف یا بدون علامت هستند.[۸۳] میزان عفونتهای علامت دار و شدید در کودکان زیر دو سال بالاتر است و به تدریج تا سن ۴۵ سالگی کاهش مییابد.[۸۴] شدیدترین علائم معمولاً در کودکان ششماهه تا دو ساله، افراد مسن و مبتلایان به نقص ایمنی رخ میدهد. به دلیل ایمنی به دست آمده در دوران کودکی، بیشتر بزرگسالان مستعد ابتلا به روتاویروس نیستند. گاستروانتریت در بزرگسالان معمولاً علتی غیر از روتاویروس دارد، اما شیوع عفونتهای بدون علامت در بزرگسالان میتوانند به انتقال این ویروس به افراد آسیبپذیر کمک کند.[۸۵] شواهدی وجود دارد که نشان میدهد گروه خونی میتواند بر استعداد ابتلا به عفونت توسط روتاویروسها مؤثر باشد.[۸۶]
تشخیص
تشخیص عفونت با روتاویروس معمولاً به دنبال تشخیص گاستروانتریت و در نتیجه اسهال شدید صورت میگیرد.[۸۷] اکثر کودکانی که با گاستروانتریت در بیمارستان بستری میشوند، ابتلایشان به روتاویروس نیز مورد بررسی قرار میگیرد.[۸۸] تشخیص اختصاصی و قطعی عفونت روتاویروسی با یافتن ویروس در مدفوع کودک با روش ایمونواسی آنزیمی انجام میشود. چندین تست مجاز وجود دارد که حساس و اختصاصی هستند و میتوانند تمام سروتیپهای روتاویروس را شناسایی کنند.[۸۹] روشهای دیگری مانند میکروسکوپ الکترونی و PCR (واکنش زنجیرهای پلیمراز)، در آزمایشگاههای تحقیقاتی مورد استفاده قرار میگیرند.[۹۰] واکنش زنجیره ای پلیمراز رونویسی معکوس (RT-PCR) میتواند تمام گونهها و سروتیپهای روتاویروسهای انسانی را شناسایی کند.[۹۱]
در حیوانات
روتاویروسها بسیاری از گونههای جانوران را در جوانیشان آلوده میکنند و عامل اصلی اسهال در حیوانات وحشی یا پرورش یافته و اهلی در سراسر جهان هستند.[۷] روتاویروسها به عنوان یک عامل بیماریزای دام، به ویژه در گوسالهها و خوکچههای جوان، به دلیل هزینههای درمان و مرگ و میر بالا، زیان اقتصادی بسیاری به کشاورزان وارد میکنند.[۹۲] روتاویروسهای حیوانی، مخزن بالقوهای برای تبادل ژنتیکی با روتاویروسهای انسانی هستند.[۹۳] شواهدی وجود دارد که روتاویروسهای حیوانی میتوانند چه از طریق انتقال مستقیم[۹۴] یا با کمک ایجاد کردن ویروسهای تغییر کرده (جهشیافته) از سویههای انسانی[۹۵] به کمک انتقال توالیهای RNA خود به آنها، انسان را آلوده کنند.[۹۶]
تاریخچه
در سال ۱۹۴۳، ژاکوب لایت و هوراس هودز ثابت کردند که یک عامل قابل پالایش در مدفوع کودکان مبتلا به اسهال عفونی باعث اسهال دامی در گاوها نیز میگردد.[۹۷] سه دهه بعد، بررسی نمونهها نشان داده که عامل بیماریزا روتاویروسها هستند.[۹۸] در سالهای بعد، مشخص شد که یک ویروس در موش[۹۹] با ویروس ایجاد کنندهٔ اسهال دامی مرتبط است.[۱۰۰] در سال ۱۹۷۳، روث بیشاپ و همکارانش ویروسهای مرتبطی را که در کودکان مبتلا به گاستروانتریت یافت میشود، طبقهبندی کردند.[۱۰۱]
در سال ۱۹۷۴، توماس هنری فلویت پس از مشاهده این موضوع که ذرات روتاویروس در هنگام مشاهده از طریق میکروسکوپ الکترونی مانند یک چرخ (rota در زبان لاتین) به نظر میرسند، نام روتاویروس را برای آنان پیشنهاد کرد.[۱۰۲][۱۰۳] چهارسال بعد، این نام بهطور رسمی توسط کمیته بینالمللی طبقهبندی ویروسها به رسمیت شناخته شد.[۱۰۴] در سال ۱۹۷۶، ویروسهای مرتبط در چندین گونه دیگر از حیوانات طبقهبندی شد.[۱۰۵] این ویروسها که همگی باعث گاستروانتریت حاد میشوند، به عنوان یک عامل بیماریزای جمعی در انسان و سایر حیوانات در سراسر جهان شناخته شدند.[۱۰۲] سروتیپهای روتاویروس برای اولین بار در سال ۱۹۸۰ توصیف شدند[۱۰۶] و در سال بعد، روتاویروسهای انسان برای اولین بار در کشت سلولی مشتق شده از کلیه میمونها با افزودن تریپسین (آنزیم یافتشده در دوازدهه پستانداران و پروتئینی ضروری برای تکثیر روتاویروس) در محیط آزمایشگاهی کشت داده شدند.[۱۰۷] قابلیت تکثیر روتاویروسها در محیط کشت، تحقیقات را سرعت بخشید و در اواسط دهه ۱۹۸۰ اولین واکسنهای نامزدشده مورد ارزیابی قرار گرفتند.[۱۰۸]
جستارهای وابسته
یادداشتها
- ↑ هنگامی که ویروسها در داخل یا در حال آلوده کردن یک سلول نیستند، به شکل ذرات ویروسی یا ویریونهای مستقل وجود دارند که تنها از پوشش و ماده ژنتیکی تشکیل شدهاند (بدون پروتئین عملکردی). این مادههای ژنتیکی به صورت مولکولهای طولانی DNA یا RNA که ساختار ویروس و پروتئینهای عملکردی آن را در آینده ایجاد میکند، وجود دارند. ویریونها از کپسید که مواد ژنتیکی را احاطه کرده، پوشش پروتئینی که از آن محافظت میکند و در برخی موارد یک پوشش خارجی از لیپیدها، تشکیل شدهاند[۳۲]
- ↑ ترشح کنندگی آنتیژن یک صفت ژنتیکی است[۴۹] که به وجود یا عدم وجود آنتیژنهای گروه خونی ABO محلول در مایعات بدن فرد مانند بزاق، اشک، شیر مادر، ادرار و مایع منی اشاره دارد. افرادی که این آنتیژنها را در مایعات بدن خود ترشح میکنند، ترشح کننده آنتیژن نامیده میشوند.[۵۰]
- ↑ چارچوب خوانش بازِ خارج از فاز زمانی اتفاق میافتد که توالیهای همپوش (توالیهایی شبیه از چند ژن همسایه) حین ترجمه توسط چارچوبهای خواندن مختلف ترجمه میشوند[۶۶] و بسته به اینکه این توالیهای همپوش، ۱ یا ۲ نوکلئوتید باشد، پروتئینهای متفاوتی توسط یک ژن را کد میکند (هر کدون شامل ۳ نوکلئوتید است).[۶۷]
- ↑ به صورت کامل تأثیرات این پروتئینها بر روی ساخت محلهای سوخت و ساز ویروسی شناخته نشدهاست؛ از آنجا که در شرایط آزمایشگاهی، مهار پروتئین NSP5 به کمک تخریب ژن آن در RNA ویروسی، منجر به کاهش شدید تکثیر روتاویروس میشود، وجود نقش این پروتئین در ساخت این محلها محتمل است.[۷۳]
منابع
- ↑ Dennehy PH (September 2015). "Rotavirus Infection: A Disease of the Past?". Infectious Disease Clinics of North America. 29 (4): 617–635. doi:10.1016/j.idc.2015.07.002. PMID 26337738.
- ↑ ۲٫۰ ۲٫۱ ۲٫۲ Grimwood K, Lambert SB (2009). "Rotavirus vaccines: opportunities and challenges". Human Vaccines. 5 (2): 57–69. doi:10.4161/hv.5.2.6924. PMID 18838873. S2CID 31164630.
- ↑ Bernstein DI (2009). "Rotavirus overview". The Pediatric Infectious Disease Journal. 28 (Suppl 3): S50–S53. doi:10.1097/INF.0b013e3181967bee. PMID 19252423. S2CID 30544613.
- ↑ Leung AK, Kellner JD, Davies HD (2005). "Rotavirus gastroenteritis". Advances in Therapy. 22 (5): 476–487. doi:10.1007/BF02849868. PMID 16418157. S2CID 39847059.
- ↑ Hallowell BD, Chavers T, Parashar U, Tate JE (April 2022). "Global Estimates of Rotavirus Hospitalizations Among Children Below 5 Years in 2019 and Current and Projected Impacts of Rotavirus Vaccination". Journal of the Pediatric Infectious Diseases Society. 11 (4): 149–158. doi:10.1093/jpids/piab114. PMID 34904636.
- ↑ Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL (2007). "Use of formative research in developing a knowledge translation approach to rotavirus vaccine introduction in developing countries". BMC Public Health. 7: 281. doi:10.1186/1471-2458-7-281. PMC 2173895. PMID 17919334. S2CID 424503.
- ↑ ۷٫۰ ۷٫۱ Dubovi EJ, MacLachlan NJ (2010). Fenner's Veterinary Virology (4th ed.). Boston: Academic Press. p. 288. ISBN 978-0-12-375158-4.
- ↑ Bishop R (2009). "Discovery of rotavirus: Implications for child health". Journal of Gastroenterology and Hepatology. 24 (Suppl 3): S81–S85. doi:10.1111/j.1440-1746.2009.06076.x. PMID 19799704.
- ↑ Janko MM, Joffe J, Michael D, Earl L, Rosettie KL, Sparks GW, Albertson SB, Compton K, Pedroza Velandia P, Stafford L, Zheng P, Aravkin A, Kyu HH, Murray CJ, Weaver MR (June 2022). "Cost-effectiveness of rotavirus vaccination in children under five years of age in 195 countries: A meta-regression analysis". Vaccine. 40 (28): 3903–3917. doi:10.1016/j.vaccine.2022.05.042. PMC 9208428. PMID 35643565. S2CID 249072461.
- ↑ Fischer TK, Viboud C, Parashar U, Malek M, Steiner C, Glass R, Simonsen L (April 2007). "Hospitalizations and deaths from diarrhea and rotavirus among children <5 years of age in the United States, 1993–2003". The Journal of Infectious Diseases. 195 (8): 1117–1125. doi:10.1086/512863. PMID 17357047.
- ↑ Leshem E, Moritz RE, Curns AT, Zhou F, Tate JE, Lopman BA, Parashar UD (July 2014). "Rotavirus vaccines and health care utilization for diarrhea in the United States (2007–2011)". Pediatrics. 134 (1): 15–23. doi:10.1542/peds.2013-3849. PMC 7975848. PMID 24913793.
- ↑ Tate JE, Cortese MM, Payne DC, Curns AT, Yen C, Esposito DH, et al. (January 2011). "Uptake, impact, and effectiveness of rotavirus vaccination in the United States: review of the first 3 years of postlicensure data". The Pediatric Infectious Disease Journal. 30 (1 Suppl): S56–60. doi:10.1097/INF.0b013e3181fefdc0. PMID 21183842. S2CID 20940659.
- ↑ Diggle L (2007). "Rotavirus diarrhea and future prospects for prevention". British Journal of Nursing. 16 (16): 970–974. doi:10.12968/bjon.2007.16.16.27074. PMID 18026034.
- ↑ Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (2011). "Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries". Human Vaccines. 7 (7): 734–748. doi:10.4161/hv.7.7.15511. PMID 21734466. S2CID 23996836.
- ↑ Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (2011). "Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries". Human Vaccines. 7 (7): 734–748. doi:10.4161/hv.7.7.15511. PMID 21734466. S2CID 23996836.
- ↑ Parashar UD, Johnson H, Steele AD, Tate JE (May 2016). Parashar UD, Tate JE (eds.). "Health Impact of Rotavirus Vaccination in Developing Countries: Progress and Way Forward". Clinical Infectious Diseases. 62 (Suppl 2): S91–95. doi:10.1093/cid/civ1015. PMID 27059361.
- ↑ "Virus Taxonomy: 2021 Release". International Committee on Taxonomy of Viruses (ICTV). Retrieved May 19, 2022.
- ↑ Suzuki H (August 2019). "Rotavirus Replication: Gaps of Knowledge on Virus Entry and Morphogenesis". The Tohoku Journal of Experimental Medicine. 248 (4): 285–296. doi:10.1620/tjem.248.285. PMID 31447474.
- ↑ Kirkwood CD (September 2010). "Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs". The Journal of Infectious Diseases. 202 Suppl (Suppl 1): S43–48. doi:10.1086/653548. PMID 20684716.
- ↑ Marthaler D, Rossow K, Culhane M, Goyal S, Collins J, Matthijnssens J, Nelson M, Ciarlet M (July 2014). "Widespread rotavirus H in commercially raised pigs, United States". Emerging Infectious Diseases. 20 (7): 1195–1198. doi:10.3201/eid2007.140034. PMC 4073875. PMID 24960190.
- ↑ Wakuda M, Ide T, Sasaki J, Komoto S, Ishii J, Sanekata T, Taniguchi K (August 2011). "Porcine rotavirus closely related to novel group of human rotaviruses". Emerging Infectious Diseases. 17 (8): 1491–1493. doi:10.3201/eid1708.101466. PMC 3381553. PMID 21801631.
- ↑ Phan TG, Leutenegger CM, Chan R, Delwart E (June 2017). "Rotavirus I in feces of a cat with diarrhea". Virus Genes. 53 (3): 487–490. doi:10.1007/s11262-017-1440-4. PMC 7089198. PMID 28255929.
- ↑ Bányai K, Kemenesi G, Budinski I, Földes F, Zana B, Marton S, Varga-Kugler R, Oldal M, Kurucz K, Jakab F (March 2017). "Candidate new rotavirus species in Schreiber's bats, Serbia". Infection, Genetics and Evolution. 48: 19–26. doi:10.1016/j.meegid.2016.12.002. PMC 7106153. PMID 27932285.
- ↑ O'Ryan M (March 2009). "The ever-changing landscape of rotavirus serotypes". The Pediatric Infectious Disease Journal. 28 (3 Suppl): S60–62. doi:10.1097/INF.0b013e3181967c29. PMID 19252426. S2CID 22421988.
- ↑ Patton JT (January 2012). "Rotavirus diversity and evolution in the post-vaccine world". Discovery Medicine. 13 (68): 85–97. PMC 3738915. PMID 22284787.
- ↑ Patton JT (January 2012). "Rotavirus diversity and evolution in the post-vaccine world". Discovery Medicine. 13 (68): 85–97. PMC 3738915. PMID 22284787.
- ↑ Phan MV, Anh PH, Cuong NV, Munnink BB, van der Hoek L, My PT, Tri TN, Bryant JE, Baker S, Thwaites G, Woolhouse M, Kellam P, Rabaa MA, Cotten M (July 2016). "Unbiased whole-genome deep sequencing of human and porcine stool samples reveals circulation of multiple groups of rotaviruses and a putative zoonotic infection". Virus Evolution. 2 (2): vew027. doi:10.1093/ve/vew027. PMC 5522372. PMID 28748110.
- ↑ Beards GM, Desselberger U, Flewett TH (December 1989). "Temporal and geographical distributions of human rotavirus serotypes, 1983 to 1988". Journal of Clinical Microbiology. 27 (12): 2827–2833. doi:10.1128/JCM.27.12.2827-2833.1989. PMC 267135. PMID 2556435.
- ↑ Rakau KG, Nyaga MM, Gededzha MP, Mwenda JM, Mphahlele MJ, Seheri LM, Steele AD (January 2021). "Genetic characterization of G12P[6] and G12P[8] rotavirus strains collected in six African countries between 2010 and 2014". BMC Infectious Diseases. 21 (1): 107. doi:10.1186/s12879-020-05745-6. PMC 7821174. PMID 33482744.
- ↑ Antoni S, Nakamura T, Cohen AL, Mwenda JM, Weldegebriel G, Biey JN, Shaba K, Rey-Benito G, de Oliveira LH, Oliveira MT, Ortiz C, Ghoniem A, Fahmy K, Ashmony HA, Videbaek D, Daniels D, Pastore R, Singh S, Tondo E, Liyanage JB, Sharifuzzaman M, Grabovac V, Batmunkh N, Logronio J, Armah G, Dennis FE, Seheri M, Magagula N, Mphahlele J, Leite JP, Araujo IT, Fumian TM, El Mohammady H, Semeiko G, Samoilovich E, Giri S, Kang G, Thomas S, Bines J, Kirkwood CD, Liu N, Lee DY, Iturriza-Gomara M, Page NA, Esona MD, Ward ML, Wright CN, Mijatovic-Rustempasic S, Tate JE, Parashar UD, Gentsch J, Bowen MD, Serhan F (2023). "Rotavirus genotypes in children under five years hospitalized with diarrhea in low and middle-income countries: Results from the WHO-coordinated Global Rotavirus Surveillance Network". PLOS Global Public Health. 3 (11): e0001358. doi:10.1371/journal.pgph.0001358. PMC 10683987. PMID 38015834.
- ↑ ۳۱٫۰ ۳۱٫۱ ۳۱٫۲ Estes MK, Cohen J (1989). "Rotavirus gene structure and function". Microbiological Reviews. 53 (4): 410–449. doi:10.1128/MMBR.53.4.410-449.1989. PMC 372748. PMID 2556635.
- ↑ Kiselev, N. A.; Sherman, M. B.; Tsuprun, V. L. (1990-01-01). "Negative staining of proteins". Electron Microscopy Reviews. 3 (1): 43–72. doi:10.1016/0892-0354(90)90013-I. ISSN 0892-0354.
- ↑ ۳۳٫۰ ۳۳٫۱ Pesavento JB, Crawford SE, Estes MK, Prasad BV (2006). "Rotavirus proteins: structure and assembly". In Roy P (ed.). Reoviruses: Entry, Assembly and Morphogenesis. Current Topics in Microbiology and Immunology. Vol. 309. New York: Springer. pp. 189–219. doi:10.1007/3-540-30773-7_7. ISBN 978-3-540-30772-3. PMID 16913048. S2CID 11290382.
- ↑ Prasad BV, Chiu W (1994). "Structure of Rotavirus". In Ramig RF (ed.). Rotaviruses. Current Topics in Microbiology and Immunology. Vol. 185. New York: Springer. pp. 9–29. doi:10.1007/978-3-642-78256-5_2. ISBN 978-3-540-56761-5. PMID 8050286.
- ↑ ۳۵٫۰ ۳۵٫۱ Rodríguez JM, Luque D (2019). "Structural Insights into Rotavirus Entry". Physical Virology. Advances in Experimental Medicine and Biology. Vol. 1215. pp. 45–68. doi:10.1007/978-3-030-14741-9_3. hdl:20.500.12105/10344. ISBN 978-3-030-14740-2. PMID 31317495. S2CID 197541267.
- ↑ Gray, James; Desselberger, U. (2000). Rotaviruses: methods and protocols. Totowa, N.J.: Humana Press. p. 15. ISBN 978-1-59259-078-0. OCLC 55684328.
- ↑ ۳۷٫۰ ۳۷٫۱ ۳۷٫۲ Kirkwood CD (September 2010). "Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs". The Journal of Infectious Diseases. 202 Suppl (Suppl 1): S43–48. doi:10.1086/653548. PMID 20684716.
- ↑ Patton JT (1995). "Structure and function of the rotavirus RNA-binding proteins". The Journal of General Virology. 76 (11): 2633–2644. doi:10.1099/0022-1317-76-11-2633. PMID 7595370.
- ↑ Patton JT (2001). "Rotavirus RNA Replication and Gene Expression". Gastroenteritis Viruses. Novartis Foundation Symposia. Vol. 238. pp. 64–77, discussion 77–81. doi:10.1002/0470846534.ch5. ISBN 978-0-470-84653-7. PMID 11444036.
- ↑ Vásquez-del Carpió R, Morales JL, Barro M, Ricardo A, Spencer E (2006). "Bioinformatic prediction of polymerase elements in the rotavirus VP1 protein". Biological Research. 39 (4): 649–659. doi:10.4067/S0716-97602006000500008. PMID 17657346.
- ↑ Trask SD, Ogden KM, Patton JT (2012). "Interactions among capsid proteins orchestrate rotavirus particle functions". Current Opinion in Virology. 2 (4): 373–379. doi:10.1016/j.coviro.2012.04.005. PMC 3422376. PMID 22595300.
- ↑ ۴۲٫۰ ۴۲٫۱ Taraporewala ZF, Patton JT (2004). "Nonstructural proteins involved in genome packaging and replication of rotaviruses and other members of the Reoviridae". Virus Research. 101 (1): 57–66. doi:10.1016/j.virusres.2003.12.006. PMID 15010217.
- ↑ Angel J, Franco MA, Greenberg HB (2009). Mahy BW, Van Regenmortel MH (eds.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p. 277. ISBN 978-0-12-375147-8.
- ↑ Cowling VH (2009). "Regulation of mRNA cap methylation". The Biochemical Journal. 425 (2): 295–302. doi:10.1042/BJ20091352. PMC 2825737. PMID 20025612.
- ↑ Gardet A, Breton M, Fontanges P, Trugnan G, Chwetzoff S (2006). "Rotavirus spike protein VP4 binds to and remodels actin bundles of the epithelial brush border into actin bodies". Journal of Virology. 80 (8): 3947–3456. doi:10.1128/JVI.80.8.3947-3956.2006. PMC 1440440. PMID 16571811.
- ↑ Arias CF, Isa P, Guerrero CA, Méndez E, Zárate S, López T, Espinosa R, Romero P, López S (2002). "Molecular biology of rotavirus cell entry". Archives of Medical Research. 33 (4): 356–361. doi:10.1016/S0188-4409(02)00374-0. PMID 12234525.
- ↑ ۴۷٫۰ ۴۷٫۱ Jayaram H, Estes MK, Prasad BV (2004). "Emerging themes in rotavirus cell entry, genome organization, transcription and replication". Virus Research. 101 (1): 67–81. doi:10.1016/j.virusres.2003.12.007. PMID 15010218.
- ↑ Hoshino Y, Jones RW, Kapikian AZ (2002). "Characterization of neutralization specificities of outer capsid spike protein VP4 of selected murine, lapine, and human rotavirus strains". Virology. 299 (1): 64–71. doi:10.1006/viro.2002.1474. PMID 12167342.
- ↑ Rydell, Gustaf E.; Kindberg, Elin; Larson, Göran; Svensson, Lennart (February 2011). "Susceptibility to winter vomiting disease: a sweet matter". Reviews in Medical Virology. 21 (6): 370–382. doi:10.1002/rmv.704. ISSN 1099-1654. PMID 22025362.
- ↑ Denise M Harmening (30 November 2018). Modern Blood Banking & Transfusion Practices. F.A. Davis. ISBN 978-0-8036-9462-0.
- ↑ Van Trang N, Vu HT, Le NT, Huang P, Jiang X, Anh DD (2014). "Association between norovirus and rotavirus infection and histo-blood group antigen types in Vietnamese children". Journal of Clinical Microbiology. 52 (5): 1366–1374. doi:10.1128/JCM.02927-13. PMC 3993640. PMID 24523471.
- ↑ Sharma S, Hagbom M, Svensson L, Nordgren J (March 2020). "The Impact of Human Genetic Polymorphisms on Rotavirus Susceptibility, Epidemiology, and Vaccine Take". Viruses. 12 (3): 324. doi:10.3390/v12030324. PMC 7150750. PMID 32192193.
- ↑ ۵۳٫۰ ۵۳٫۱ ۵۳٫۲ Bishop RF (1996). "Natural history of human rotavirus infection". Archives of Virology. Supplementum. 12: 119–28. doi:10.1007/978-3-7091-6553-9_14. PMID 9015109.
- ↑ Beards GM, Campbell AD, Cottrell NR, Peiris JS, Rees N, Sanders RC, Shirley JA, Wood HC, Flewett TH (1984). "Enzyme-linked immunosorbent assays based on polyclonal and monoclonal antibodies for rotavirus detection" (PDF). Journal of Clinical Microbiology. 19 (2): 248–54. doi:10.1128/JCM.19.2.248-254.1984. PMC 271031. PMID 6321549.
- ↑ ۵۵٫۰ ۵۵٫۱ Hua J, Mansell EA, Patton JT (1993). "Comparative analysis of the rotavirus NS53 gene: conservation of basic and cysteine-rich regions in the protein and possible stem-loop structures in the RNA". Virology. 196 (1): 372–378. doi:10.1006/viro.1993.1492. PMID 8395125.
- ↑ Arnold MM (2016). "The Rotavirus Interferon Antagonist NSP1: Many Targets, Many Questions". Journal of Virology. 90 (11): 5212–5215. doi:10.1128/JVI.03068-15. PMC 4934742. PMID 27009959.
- ↑ Kattoura MD, Chen X, Patton JT (1994). "The rotavirus RNA-binding protein NS35 (NSP2) forms 10S multimers and interacts with the viral RNA polymerase". Virology. 202 (2): 803–13. doi:10.1006/viro.1994.1402. PMID 8030243.
- ↑ ۵۸٫۰ ۵۸٫۱ Poncet D, Aponte C, Cohen J (1993). "Rotavirus protein NSP3 (NS34) is bound to the 3' end consensus sequence of viral mRNAs in infected cells" (PDF). Journal of Virology. 67 (6): 3159–3165. doi:10.1128/JVI.67.6.3159-3165.1993. PMC 237654. PMID 8388495.
- ↑ Gratia M, Vende P, Charpilienne A, Baron HC, Laroche C, Sarot E, Pyronnet S, Duarte M, Poncet D (2016). "Challenging the Roles of NSP3 and Untranslated Regions in Rotavirus mRNA Translation". PLOS ONE. 11 (1): e0145998. Bibcode:2016PLoSO..1145998G. doi:10.1371/journal.pone.0145998. PMC 4699793. PMID 26727111.
- ↑ López S, Arias CF (2012). "Rotavirus-host cell interactions: an arms race". Current Opinion in Virology. 2 (4): 389–398. doi:10.1016/j.coviro.2012.05.001. PMID 22658208.
- ↑ Hyser JM, Estes MK (2009). "Rotavirus vaccines and pathogenesis: 2008". Current Opinion in Gastroenterology. 25 (1): 36–43. doi:10.1097/MOG.0b013e328317c897. PMC 2673536. PMID 19114772.
- ↑ Pham T, Perry JL, Dosey TL, Delcour AH, Hyser JM (March 2017). "The Rotavirus NSP4 Viroporin Domain is a Calcium-conducting Ion Channel". Scientific Reports. 7: 43487. Bibcode:2017NatSR...743487P. doi:10.1038/srep43487. PMC 5335360. PMID 28256607.
- ↑ Afrikanova I, Miozzo MC, Giambiagi S, Burrone O (1996). "Phosphorylation generates different forms of rotavirus NSP5". Journal of General Virology. 77 (9): 2059–2065. doi:10.1099/0022-1317-77-9-2059. PMID 8811003.
- ↑ Rainsford EW, McCrae MA (2007). "Characterization of the NSP6 protein product of rotavirus gene 11". Virus Research. 130 (1–2): 193–201. doi:10.1016/j.virusres.2007.06.011. PMID 17658646.
- ↑ Mohan KV, Atreya CD (2001). "Nucleotide sequence analysis of rotavirus gene 11 from two tissue culture-adapted ATCC strains, RRV and Wa". Virus Genes. 23 (3): 321–329. doi:10.1023/A:1012577407824. PMID 11778700. S2CID 21538632.
- ↑ Fukuda, Yoko; Nakayama, Yoichi; Tomita, Masaru (December 2003). "On dynamics of overlapping genes in bacterial genomes". Gene. 323: 181–187. doi:10.1016/j.gene.2003.09.021. PMID 14659892.
- ↑ Johnson Z, Chisholm S (2004). "Properties of overlapping genes are conserved across microbial genomes". Genome Res. 14 (11): 2268–72. doi:10.1101/gr.2433104. PMC 525685. PMID 15520290.
- ↑ Gray, James; Desselberger, U. (2000). Rotaviruses: methods and protocols. Totowa, N.J.: Humana Press. p. 5. ISBN 978-1-59259-078-0. OCLC 55684328.
- ↑ ۶۹٫۰ ۶۹٫۱ Baker M, Prasad BV (2010). "Rotavirus cell entry". In Johnson J (ed.). Cell Entry by Non-Enveloped Viruses. Current Topics in Microbiology and Immunology. Vol. 343. pp. 121–148. doi:10.1007/82_2010_34. ISBN 978-3-642-13331-2. PMID 20397068.
- ↑ ۷۰٫۰ ۷۰٫۱ Arnold MM (2016). "The Rotavirus Interferon Antagonist NSP1: Many Targets, Many Questions". Journal of Virology. 90 (11): 5212–5215. doi:10.1128/JVI.03068-15. PMC 4934742. PMID 27009959.
- ↑ Staginnus, Christina; Richert-Pöggeler, Katja R. (October 2006). "Endogenous pararetroviruses: two-faced travelers in the plant genome". Trends in Plant Science. 11 (10): 485–491. doi:10.1016/j.tplants.2006.08.008. ISSN 1360-1385. PMID 16949329.
- ↑ ۷۲٫۰ ۷۲٫۱ Silvestri LS, Taraporewala ZF, Patton JT (2004). "Rotavirus replication: plus-sense templates for double-stranded RNA synthesis are made in viroplasms". Journal of Virology. 78 (14): 7763–7774. doi:10.1128/JVI.78.14.7763-7774.2004. PMC 434085. PMID 15220450.
- ↑ ۷۳٫۰ ۷۳٫۱ Patton JT, Vasquez-Del Carpio R, Spencer E (2004). "Replication and transcription of the rotavirus genome". Current Pharmaceutical Design. 10 (30): 3769–3777. doi:10.2174/1381612043382620. PMID 15579070.
- ↑ Ruiz MC, Leon T, Diaz Y, Michelangeli F (2009). "Molecular biology of rotavirus entry and replication". The Scientific World Journal. 9: 1476–1497. doi:10.1100/tsw.2009.158. PMC 5823125. PMID 20024520.
- ↑ ۷۵٫۰ ۷۵٫۱ Dennehy PH (2000). "Transmission of rotavirus and other enteric pathogens in the home". Pediatric Infectious Disease Journal. 19 (Suppl 10): S103–105. doi:10.1097/00006454-200010001-00003. PMID 11052397. S2CID 28625697.
- ↑ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R (1993). "Prevalence of rotavirus on high-risk fomites in day-care facilities". Pediatrics. 92 (2): 202–205. doi:10.1542/peds.92.2.202. PMID 8393172. S2CID 20327842.
- ↑ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1984). "Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments" (PDF). Applied and Environmental Microbiology. 48 (2): 404–409. Bibcode:1984ApEnM..48..404R. doi:10.1128/AEM.48.2.404-409.1984. PMC 241526. PMID 6091548.
- ↑ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1984). "Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments" (PDF). Applied and Environmental Microbiology. 48 (2): 404–409. Bibcode:1984ApEnM..48..404R. doi:10.1128/AEM.48.2.404-409.1984. PMC 241526. PMID 6091548.
- ↑ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1984). "Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments" (PDF). Applied and Environmental Microbiology. 48 (2): 404–409. Bibcode:1984ApEnM..48..404R. doi:10.1128/AEM.48.2.404-409.1984. PMC 241526. PMID 6091548.
- ↑ Hochwald C, Kivela L (1999). "Rotavirus vaccine, live, oral, tetravalent (RotaShield)". Pediatric Nursing. 25 (2): 203–204, 207. PMID 10532018.
- ↑ Maldonado YA, Yolken RH (1990). "Rotavirus". Baillière's Clinical Gastroenterology. 4 (3): 609–625. doi:10.1016/0950-3528(90)90052-I. PMID 1962726.
- ↑ Glass RI, Parashar UD, Bresee JS, Turcios R, Fischer TK, Widdowson MA, Jiang B, Gentsch JR (2006). "Rotavirus vaccines: current prospects and future challenges". The Lancet. 368 (9532): 323–332. doi:10.1016/S0140-6736(06)68815-6. PMID 16860702. S2CID 34569166.
- ↑ Offit PA (2001). Gastroenteritis viruses. New York: Wiley. pp. 106–124. ISBN 978-0-471-49663-2.
- ↑ Ramsay M, Brown D (2000). "Epidemiology of Group A Rotaviruses: Surveillance and Burden of Disease Studies". In Desselberger U, Gray J (eds.). Rotaviruses: Methods and Protocols. Methods in Molecular Medicine. Vol. 34. Totowa, NJ: Humana Press. pp. 217–238. doi:10.1385/1-59259-078-0:217. ISBN 978-0-89603-736-6. PMID 21318862.
- ↑ Anderson EJ, Weber SG (2004). "Rotavirus infection in adults". The Lancet Infectious Diseases. 4 (2): 91–99. doi:10.1016/S1473-3099(04)00928-4. PMC 7106507. PMID 14871633.
- ↑ Elhabyan A, Elyaacoub S, Sanad E, Abukhadra A, Elhabyan A, Dinu V (November 2020). "The role of host genetics in susceptibility to severe viral infections in humans and insights into host genetics of severe COVID-19: A systematic review". Virus Research. 289: 198163. doi:10.1016/j.virusres.2020.198163. PMC 7480444. PMID 32918943.
- ↑ Patel MM, Tate JE, Selvarangan R, Daskalaki I, Jackson MA, Curns AT, Coffin S, Watson B, Hodinka R, Glass RI, Parashar UD (2007). "Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination". The Pediatric Infectious Disease Journal. 26 (10): 914–919. doi:10.1097/INF.0b013e31812e52fd. PMID 17901797. S2CID 10992309.
- ↑ The Pediatric ROTavirus European CommitTee (PROTECT) (2006). "The paediatric burden of rotavirus disease in Europe". Epidemiology and Infection. 134 (5): 908–916. doi:10.1017/S0950268806006091. PMC 2870494. PMID 16650331.
- ↑ Angel J, Franco MA, Greenberg HB (2009). Mahy WJ, Van Regenmortel MH (eds.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p. 278. ISBN 978-0-12-375147-8.
- ↑ Goode J, Chadwick D (2001). Gastroenteritis viruses. New York: Wiley. p. 14. ISBN 978-0-471-49663-2.
- ↑ Fischer TK, Gentsch JR (2004). "Rotavirus typing methods and algorithms". Reviews in Medical Virology. 14 (2): 71–82. doi:10.1002/rmv.411. PMC 7169166. PMID 15027000.
- ↑ Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (2010). "Zoonotic aspects of rotaviruses". Veterinary Microbiology. 140 (3–4): 246–255. doi:10.1016/j.vetmic.2009.08.028. PMID 19781872.
- ↑ Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (2010). "Zoonotic aspects of rotaviruses". Veterinary Microbiology. 140 (3–4): 246–255. doi:10.1016/j.vetmic.2009.08.028. PMID 19781872.
- ↑ Müller H, Johne R (2007). "Rotaviruses: diversity and zoonotic potential—a brief review". Berliner und Munchener Tierarztliche Wochenschrift. 120 (3–4): 108–112. PMID 17416132.
- ↑ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J (2004). "The zoonotic potential of rotavirus". The Journal of Infection. 48 (4): 289–302. doi:10.1016/j.jinf.2004.01.018. PMID 15066329.
- ↑ Dóró R, Farkas SL, Martella V, Bányai K (2015). "Zoonotic transmission of rotavirus: surveillance and control". Expert Review of Anti-infective Therapy. 13 (11): 1337–1350. doi:10.1586/14787210.2015.1089171. PMID 26428261. S2CID 42693014.
- ↑ Light JS, Hodes HL (1943). "Studies on Epidemic Diarrhea of the New-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves". American Journal of Public Health and the Nation's Health. 33 (12): 1451–1454. doi:10.2105/AJPH.33.12.1451. PMC 1527675. PMID 18015921.
- ↑ Mebus CA, Wyatt RG, Sharpee RL, Sereno MM, Kalica AR, Kapikian AZ, Twiehaus MJ (1976). "Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis" (PDF). Infection and Immunity. 14 (2): 471–474. doi:10.1128/IAI.14.2.471-474.1976. PMC 420908. PMID 184047.
- ↑ Rubenstein D, Milne RG, Buckland R, Tyrrell DA (1971). "The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium". British Journal of Experimental Pathology. 52 (4): 442–445. PMC 2072337. PMID 4998842.
- ↑ Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1976). "Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals" (PDF). Infection and Immunity. 14 (3): 804–810. doi:10.1128/IAI.14.3.804-810.1976. PMC 420956. PMID 965097.
- ↑ Bishop R (2009). "Discovery of rotavirus: Implications for child health". Journal of Gastroenterology and Hepatology. 24 (Suppl 3): S81–S85. doi:10.1111/j.1440-1746.2009.06076.x. PMID 19799704.
- ↑ ۱۰۲٫۰ ۱۰۲٫۱ Flewett TH, Woode GN (1978). "The rotaviruses". Archives of Virology. 57 (1): 1–23. doi:10.1007/BF01315633. PMC 7087197. PMID 77663.
- ↑ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM (1974). "Relation between viruses from acute gastroenteritis of children and newborn calves". The Lancet. 304 (7872): 61–63. doi:10.1016/S0140-6736(74)91631-6. PMID 4137164.
- ↑ Matthews RE (1979). "Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses". Intervirology. 12 (3–5): 129–296. doi:10.1159/000149081. PMID 43850.
- ↑ Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1976). "Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals" (PDF). Infection and Immunity. 14 (3): 804–810. doi:10.1128/IAI.14.3.804-810.1976. PMC 420956. PMID 965097.
- ↑ Beards GM, Brown DW (1988). "The antigenic diversity of rotaviruses: significance to epidemiology and vaccine strategies". European Journal of Epidemiology. 4 (1): 1–11. doi:10.1007/BF00152685. PMID 2833405.
- ↑ Urasawa T, Urasawa S, Taniguchi K (1981). "Sequential passages of human rotavirus in MA-104 cells". Microbiology and Immunology. 25 (10): 1025–1035. doi:10.1111/j.1348-0421.1981.tb00109.x. PMID 6273696.
- ↑ Ward RL, Bernstein DI (2009). "Rotarix: a rotavirus vaccine for the world". Clinical Infectious Diseases. 48 (2): 222–228. doi:10.1086/595702. PMID 19072246.
پیوند به بیرون
| در ویکیانبار پروندههایی دربارهٔ روتاویروس موجود است. |
