مقدمهای بر ویروس: تفاوت میان نسخهها
| [نسخهٔ بررسینشده] | [نسخهٔ بررسینشده] |
Hosseiniran (بحث | مشارکتها) ←ویروسها و بیماریها: ابرابزار |
Hosseiniran (بحث | مشارکتها) ←جستارهای وابسته: ابرابزار |
||
| خط ۹۴: | خط ۹۴: | ||
[[File:Guanosine-acyclovir-comparison.png|thumb|upright|ساختار [[گوانین]] برپایه DNA و داروی ضد ویروس [[آسیکلوویر]]]] |
[[File:Guanosine-acyclovir-comparison.png|thumb|upright|ساختار [[گوانین]] برپایه DNA و داروی ضد ویروس [[آسیکلوویر]]]] |
||
از اواسط دهه ۱۹۸۰، توسعه داروهای ضد ویروسی به سرعت افزایش یافتهاست که دلیل عمده این تلاشها، [[همهگیری]] بیماری ایدز میباشد. داروهای ضد ویروسی اغلب [[آنالوگ نوکلئوزید]] هستند که مولکولهای بسیار مشابهی دارند اما با بلوکهای ساختمانی DNA یکسان نیستند. هنگامی که تکثیر DNA ویروس شروع میشود، برخی از این بلوکهای ساختگی جعلی در ژنوم ویروس گنجانیده میشوند. به محض این اتفاق میافتد، تکثیر متوقف میشود. بلوکهای ساختگی جعلی فاقد ویژگیهای اساسی هستند که امکان افزودن بلوکهای بیشتر را فراهم میکند؛ بنابراین، تولید DNA متوقف شده و ویروس دیگر نمیتواند تولید مثل کند.<ref>Shors p. 514−515</ref> نمونههایی از آنالوگهای نوکلئوزید عبارتند از: [[آسیکلوویر]] برای عفونت ویروس هرپس و [[لامیوودین]] برای عفونت ویروس ایدز و هپاتیت بی. آسیکلوویر یکی از قدیمیترین و رایجترین داروهای ضد ویروسی است.<ref>Shors p. 514</ref>{{سخ}}سایر داروهای ضد ویروسی مراحل مختلف چرخه زندگی ویروسی را هدف قرار میدهند. HIV برای عفونی بودن به آنزیمی بنام [[پروتئاز اچآیوی]] وابسته است. طبقه ای از داروها به نام [[بازدارندههای پروتئاز]] وجود دارد که به این آنزیم متصل میشوند و عملکرد آن را متوقف میکنند.<ref name="Shors p. 463">Shors p. 568</ref>{{سخ}}هپاتیت C در اثر ویروسی RNA دار ایجاد میشود. در ۸۰٪ از افراد آلوده، این بیماری مزمن میشود و تا آخر عمر میماند مگر اینکه درمان شود. برای درمان آن، یک روش مؤثر وجود دارد که از داروی آنالوگ نوکلئوزید [[ریباویرین]] به همراه [[اینترفرون]] استفاده میکند.<ref name="pmid 17927615">{{cite journal | vauthors = Witthöft T, Möller B, Wiedmann KH, Mauss S, Link R, Lohmeyer J, Lafrenz M, Gelbmann CM, Hüppe D, Niederau C, Alshuth U|display-authors = 6 | title = Safety, tolerability and efficacy of peginterferon alpha-2a and ribavirin in chronic hepatitis C in clinical practice: The German Open Safety Trial | journal = J. Viral Hepat. | volume = 14 | issue = 11 | pages = 788–96 | date = November 2007 | pmid = 17927615 | pmc = 2156112 | doi = 10.1111/j.1365-2893.2007.00871.x}}</ref> درمان برای حاملان مزمن ویروس هپاتیت B با استفاده از یک استراتژی مشابه با استفاده از [[لامیوودین]] و سایر داروهای ضد ویروس انجام شدهاست.<ref name="pmid 21654909">{{cite journal | vauthors = Paul N, Han SH | title = Combination Therapy for Chronic Hepatitis B: Current Indications | journal = Curr Hepat Rep | volume = 10 | issue = 2 | pages = 98–105 | date = June 2011 | pmid = 21654909 | pmc = 3085106 | doi = 10.1007/s11901-011-0095-1}}</ref> در هر دو بیماری، داروها تولید مثل ویروس را متوقف میکنند و اینترفرون سلولهای آلوده باقی مانده را از بین میبرد.{{سخ}}عفونت HIV معمولاً با ترکیبی از داروهای ضد ویروسی درمان میشود که هریک مرحله مختلفی از چرخه زندگی ویروس را هدف قرار میدهد. داروهایی وجود دارد که مانع از اتصال ویروس به سلولها میشود، برخی دیگر که آنالوگ نوکلئوزید هستند و برخی از آنزیمهای ویروس را که برای تکثیر موردنیاز هستند را از خنثی میکنند.<ref name="Shors p. 463"/> موفقیت این داروها، اثبات اهمیت آشنایی با نحوه تولید مثل ویروسها است. |
از اواسط دهه ۱۹۸۰، توسعه داروهای ضد ویروسی به سرعت افزایش یافتهاست که دلیل عمده این تلاشها، [[همهگیری]] بیماری ایدز میباشد. داروهای ضد ویروسی اغلب [[آنالوگ نوکلئوزید]] هستند که مولکولهای بسیار مشابهی دارند اما با بلوکهای ساختمانی DNA یکسان نیستند. هنگامی که تکثیر DNA ویروس شروع میشود، برخی از این بلوکهای ساختگی جعلی در ژنوم ویروس گنجانیده میشوند. به محض این اتفاق میافتد، تکثیر متوقف میشود. بلوکهای ساختگی جعلی فاقد ویژگیهای اساسی هستند که امکان افزودن بلوکهای بیشتر را فراهم میکند؛ بنابراین، تولید DNA متوقف شده و ویروس دیگر نمیتواند تولید مثل کند.<ref>Shors p. 514−515</ref> نمونههایی از آنالوگهای نوکلئوزید عبارتند از: [[آسیکلوویر]] برای عفونت ویروس هرپس و [[لامیوودین]] برای عفونت ویروس ایدز و هپاتیت بی. آسیکلوویر یکی از قدیمیترین و رایجترین داروهای ضد ویروسی است.<ref>Shors p. 514</ref>{{سخ}}سایر داروهای ضد ویروسی مراحل مختلف چرخه زندگی ویروسی را هدف قرار میدهند. HIV برای عفونی بودن به آنزیمی بنام [[پروتئاز اچآیوی]] وابسته است. طبقه ای از داروها به نام [[بازدارندههای پروتئاز]] وجود دارد که به این آنزیم متصل میشوند و عملکرد آن را متوقف میکنند.<ref name="Shors p. 463">Shors p. 568</ref>{{سخ}}هپاتیت C در اثر ویروسی RNA دار ایجاد میشود. در ۸۰٪ از افراد آلوده، این بیماری مزمن میشود و تا آخر عمر میماند مگر اینکه درمان شود. برای درمان آن، یک روش مؤثر وجود دارد که از داروی آنالوگ نوکلئوزید [[ریباویرین]] به همراه [[اینترفرون]] استفاده میکند.<ref name="pmid 17927615">{{cite journal | vauthors = Witthöft T, Möller B, Wiedmann KH, Mauss S, Link R, Lohmeyer J, Lafrenz M, Gelbmann CM, Hüppe D, Niederau C, Alshuth U|display-authors = 6 | title = Safety, tolerability and efficacy of peginterferon alpha-2a and ribavirin in chronic hepatitis C in clinical practice: The German Open Safety Trial | journal = J. Viral Hepat. | volume = 14 | issue = 11 | pages = 788–96 | date = November 2007 | pmid = 17927615 | pmc = 2156112 | doi = 10.1111/j.1365-2893.2007.00871.x}}</ref> درمان برای حاملان مزمن ویروس هپاتیت B با استفاده از یک استراتژی مشابه با استفاده از [[لامیوودین]] و سایر داروهای ضد ویروس انجام شدهاست.<ref name="pmid 21654909">{{cite journal | vauthors = Paul N, Han SH | title = Combination Therapy for Chronic Hepatitis B: Current Indications | journal = Curr Hepat Rep | volume = 10 | issue = 2 | pages = 98–105 | date = June 2011 | pmid = 21654909 | pmc = 3085106 | doi = 10.1007/s11901-011-0095-1}}</ref> در هر دو بیماری، داروها تولید مثل ویروس را متوقف میکنند و اینترفرون سلولهای آلوده باقی مانده را از بین میبرد.{{سخ}}عفونت HIV معمولاً با ترکیبی از داروهای ضد ویروسی درمان میشود که هریک مرحله مختلفی از چرخه زندگی ویروس را هدف قرار میدهد. داروهایی وجود دارد که مانع از اتصال ویروس به سلولها میشود، برخی دیگر که آنالوگ نوکلئوزید هستند و برخی از آنزیمهای ویروس را که برای تکثیر موردنیاز هستند را از خنثی میکنند.<ref name="Shors p. 463"/> موفقیت این داروها، اثبات اهمیت آشنایی با نحوه تولید مثل ویروسها است. |
||
== نقش در بومشناسی == |
|||
ویروسها فراوانترین موجود زیستی در محیطهای آبی هستند.<ref name="pmid 16984643">{{cite journal | vauthors = Koonin EV, Senkevich TG, Dolja VV | title = The ancient Virus World and evolution of cells | journal = Biol. Direct | volume = 1 | issue = | pages = 29 | date = September 2006 | pmid = 16984643 | pmc = 1594570 | doi = 10.1186/1745-6150-1-29}}</ref> (حدود یک میلیون ویروس در یک قاشق چایخوری از آب دریا وجود دارد)<ref>Shors p. 25</ref>و آنها برای تنظیم اکوسیستمهای آب شور و آب شیرین ضروری هستند.<ref>Shors p. 5</ref> بیشتر این ویروسها باکتریوفاژها هستند که برای گیاهان و حیوانات بیضرر هستند. آنها باکتریها را در جوامع میکروبی آبزی آلوده کرده و از بین میبرند و این مهمترین مکانیسم بازیافت کربن در محیط دریایی است. مولکولهای آلی که توسط ویروسها از سلولهای باکتریایی آزاد میشوند رشد باکتریها و جلبکهای تازه را تحریک میکنند.<ref>Shors p. 25−26</ref>{{سخ}}میکروارگانیسمها بیش از ۹۰٪ زیست توده دریا را تشکیل میدهند. تخمین زده میشود که ویروسها تقریباً ۲۰٪ از این زیست توده را هر روز از بین میبرند و تعداد ویروسها در اقیانوسها ۱۵ برابر باکتریها و باستانیان است. ویروسها عمدتاً مسئول نابودی سریع [[شکوفایی جلبکی|شکوفاییهای جلبکی]] زیانبار<ref name="pmid 16163346">{{cite journal | vauthors = Suttle CA | title = Viruses in the sea | journal = Nature | volume = 437 | issue = 7057 | pages = 356–61 | date = September 2005 | pmid = 16163346 | doi = 10.1038/nature04160 |bibcode = 2005Natur.437..356S}}</ref> که اغلب زیستبومهای دیگر را نبود میکنند، هستند.<ref>{{cite web|url=https://www.cdc.gov/hab/redtide/|title=Harmful Algal Blooms: Red Tide: Home | CDC HSB|publisher=www.cdc.gov|accessdate=23 August 2009}}</ref>تعداد ویروسهای موجود در اقیانوسها بیشتر در تعداد ویروسهای خارج از آب ساحل است و تعدادشان با عمیقتر شدن آب کاهش مییابد. زیرا در آن جا میزبانان کمتری دارند.<ref name="pmid 17853907">{{cite journal | vauthors = Suttle CA | title = Marine viruses--major players in the global ecosystem | journal = Nat. Rev. Microbiol. | volume = 5 | issue = 10 | pages = 801–12 | date = October 2007 | pmid = 17853907 | doi = 10.1038/nrmicro1750}}</ref>{{سخ}} |
|||
تأثیرات آنها بسیار وسیع است. با افزایش مقدار تنفس در اقیانوسها، ویروسها بهطور غیرمستقیم مسئول کاهش میزان دیاکسید کربن در جو به میزان تقریباً ۳ [[تن (یکا)|گیگاتن]] کربن در سال هستند.<ref name="pmid 17853907"/>{{سخ}} |
|||
پستانداران دریایی نیز مستعد ابتلا به عفونتهای ویروسی هستند. در سالهای ۱۹۸۸ و ۲۰۰۲، هزاران [[فک بندرگاه]] در اروپا توسط [[ویروس دیستمپر فک]] کشته شدند.<ref>{{cite journal | last1= Hall | first1= A | last2= Jepson | first2= P | last3= Goodman | first3= S | last4= Harkonen | first4= T | title= Phocine distemper virus in the North and European Seas – Data and models, nature and nurture | journal= Biological Conservation | volume= 131 | issue= 2 | pages= 221–229 | year= 2006 |doi = 10.1016/j.biocon.2006.04.008}}</ref> بسیاری از ویروسهای دیگر، از جمله [[ویروس کالیسی]]، [[هرپسویروسان|هرپسویروس]]، [[آدنوویروس]] و [[پاروویروس]] در جمعیت پستانداران دریایی گردش میکنند.<ref name="pmid 17853907"/> |
|||
== جستارهای وابسته == |
== جستارهای وابسته == |
||
نسخهٔ ۲۲ سپتامبر ۲۰۱۹، ساعت ۱۸:۴۷
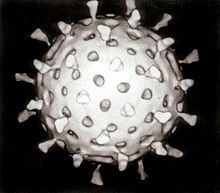
ویروس یک عامل بیولوژیکی است که در سلولهای میزبانهای زنده تولید مثل میکند. هنگامی آلودگی با ویروس، سلول میزبان مجبور میشود هزاران نسخه مشابه از ویروس اصلی را با سرعت زیاد تولید کند. برخلاف اکثر موجودات زنده، ویروسها توانایی تقسیم شدن ندارند. ویروسهای جدید در سلول میزبان آلوده جمع میشوند اما برخلاف عوامل عفونی سادهتر، ویروسها دارای ژنهایی هستند که به آنها توانایی جهش و تکامل را میدهد. بیش از ۵۰۰۰ گونه ویروس کشف شدهاست.[۱]
منشأ ویروسها مشخص نیست: بعضی از آنها ممکن است از پلاسمیدها (قطعات DNA که میتوانند بین جابجا شوند) تکامل یافته باشند، در حالی که برخی دیگر ممکن است از باکتریها تکامل یافته باشند. ویروس از دو یا سه بخش تشکیل شدهاست: بخش اول ژن است که از DNA یا RNA ساخته شدهاست که این دو مولکولهای طولانی و دارای اطلاعات ژنتیکی هستند. بخش دوم یک لایه پروتئینی است که از ژنها محافظت میکند. برخی از ویروسها لایه ای از جنس لیپید دارند که پوشش پروتئینی را احاطه کرده و در ترکیب با گیرندههای خاص، برای ورود به سلول میزبان جدید استفاده میشود. اشکال ویروسها از سادهٔ مارپیچی و بیست وجهی تا ساختارهای پیچیدهتر متفاوت هستند. اندازهٔ ویروسها از ۲۰ تا ۳۰۰ نانومتر است و ۳۳٬۰۰۰ تا ۵۰۰٬۰۰۰ عدد ویروس در کنار هم یک سانتیمتر (۰٫۳۹ اینچ) طول دارند.
ویروسها از راههای مختلفی گسترش مییابند. بسیاری از ویروسها برای گونه میزبان یا بافتی که به آن حمله میکنند اختصاص یافتهاند. هر گونه ویروس برای تکثیر به یک روش خاص متکی است. ویروسهای گیاهی اغلب توسط حشرات و ارگانیسمهای دیگر، که به عنوان ناقل شناخته میشوند، از گیاهی به گیاهی دیگر پخش میشوند. برخی از ویروسهای حیوانی از جمله ویروسهای انسانی با قرار گرفتن میزبان در معرض مایعات آلوده بدن گسترش مییابند. ویروسهایی مانند آنفولانزا هنگام سرفه یا عطسه، توسط قطرات رطوبت از طریق هوا پخش میشوند. ویروسهایی مانند نورو ویروس از طریق چرخهٔ مدفوعی دهانی که شامل آلودگی دست، غذا و آب است، منتقل میشوند. روتاویروس اغلب از طریق تماس مستقیم با کودکان آلوده منتقل میشود. ویروس نقص ایمنی انسانی (HIV) توسط مایعات بدن منتقل شده در طول رابطه جنسی منتقل میشود. برخی دیگر، مانند ویروس تب دنگی، توسط حشرات خونخوار پخش میشوند.
عفونتهای ویروسی میتوانند باعث ایجاد بیماری در انسانها، حیوانات و حتی گیاهان شوند. با این حال، آنها معمولاً توسط سیستم ایمنی بدن از بین میروند و ایمنی مادام العمر علیه آنها در بدن میزبان ایجاد میشود. آنتیبیوتیکها هیچ تأثیری روی ویروسها ندارند، اما داروهای ضد ویروسی برای درمان عفونتهای ویروسی تهدید کننده زندگی تولید اند. واکسنهایی که ایمنی مادام العمر ایجاد میکنند میتوانند از برخی عفونتهای ویروسی جلوگیری کنند.
کشف

در سال ۱۸۸۴ میکروبیولوژیست فرانسوی چارلز چمبرلند فیلتری را اختراع کرد که امروزه به عنوان فیلتر چمبرلند یا فیلتر چمبرلند-پاستور شناخته میشود که دارای منافذی کوچکتر از باکتریها میباشد؛ بنابراین او میتوانست یک محلول حاوی باکتری را از فیلتر عبور داده و باکتریها را بهطور کامل از محلول جدا کند.[۲] در اوایل دهه ۱۸۹۰، زیستشناس روسی دیمیتری ایوانفسکی از این فیلتر برای بررسی آنچه به ویروس موزائیک تنباکو معروف شد استفاده کرد. آزمایشهای او نشان داد که عصارههای برگهای خرد شده گیاهان تنباکوییان آلوده پس از فیلتراسیون، همچنان عفونی کننده باقی میمانند.
در همین زمان چند دانشمند دیگر ثابت کردند که اگرچه این عوامل (که بعدها ویروس خوانده شدند) با باکتریها متفاوت هستند، اما هنوز هم میتوانند باعث بیماری شوند و تقریباً یک صدم اندازه باکتری بودند. در سال ۱۸۹۹، میکروبیولوژیست هلندی مارتینوس بایرینک، مشاهده کرد که این عامل فقط در سلولهای درحال تقسیم تکثیر میشود. وی که نتوانست ماهیت ذرات آن را نشان دهد، آن را «جرم زنده محلول» نامید.[۳] در اوایل قرن بیستم، فردریک توورت، باکتریشناس انگلیسی، ویروسهایی را کشف کرد که باکتریها را آلوده میکردند[۴] و میکروبیولوژیست فرانسوی-کانادایی فلیکس درل، ویروسهایی را توصیف کرد که با افزودن باکتریهای رشد یافته بر روی آگار، منجر به کشته شدن آن باکتریها میشد. شمارش این مناطق باکتریهای کشته شده، به وی اجازه میداد تا تعداد ویروسهای موجود در سوسپانسیون را محاسبه کند.[۵]
با اختراع میکروسکوپ الکترونی در سال ۱۹۳۱ توسط مهندسان آلمانی ارنست روسکا و مکس نول اولین تصاویر از ویروسها به دست آمد.[۶] در سال ۱۹۳۵ وندل مردیت استنلی، زیست شیمیدان و ویروسشناس آمریکایی ویروس موزائیک تنباکو را بررسی کرد و دریافت که بیشتر آن از پروتئین ساخته شدهاست.[۷] اندکی بعد، قسمتهای پروتئین و RNA این ویروس جدا شد.[۸] یک مشکل برای دانشمندان آن زمان این بود که آنها نمیدانند چگونه ویروسها را بدون استفاده از حیوانات زنده پرورش دهند. این موفقیت در سال ۱۹۳۱ هنگامی که پاتولوژیست آمریکایی ارنست ویلیام گودپاسچر و آلیس مایلز وودروف، آنفولانزا و چندین ویروس دیگر را در تخم مرغهای بارور شده رشد دادند.[۹] برخی ویروسها را نمیتوان در تخم مرغ پرورش داد، اما این مشکل در سال ۱۹۴۹ حل شد هنگامی که جان اندرز، تامس هاکل ولر و فردریک چپمن رابینز ویروس فلج اطفال را در کشت سلولهای زنده حیوانات رشد دادند.[۱۰] تاکنون بیش از ۵۰۰۰ گونه ویروس کشف شدهاست.
خاستگاه
در هر کجا که حیات وجود دارند، ویروسها هم هستند. آنها احتمالاً از زمان تکامل سلولهای زنده وجود داشتهاند. منشأ ویروسها ناشناخته ماندهاست زیرا آنها فسیلی تشکیل نمیدهند، بنابراین تکنیکهای مولکولی مفیدترین وسیله برای بررسی فرضیه نحوه ظهور آنها بودهاند. با این حال، این تکنیکها به در دسترس بودن DNA یا RNA ویروسی باستانی یا متکی هستند، اما بیشتر ویروسهایی که در آزمایشگاهها نگهداری و ذخیره شدهاند، کمتر از ۹۰ سال عمر دارند.[۱۱][۱۲] روشهای مولکولی تنها در ردیابی اصل و نسب ویروسهایی که در قرن بیستم تکامل یافتهاند موفق بودهاند.[۱۳] گروههای جدید ویروس ممکن است بارها و بارها در تمام مراحل تکاملی پدید آمده باشند.[۱۴] سه نظریه اصلی دربارهٔ منشأ ویروسها وجود دارد:[۱۴][۱۵]
- نظریه پسرفت
- ممکن است ویروسها قبلاً سلولهای کوچکی بودهاند که انگل سلولهای بزرگتر بودهاند. با گذشت زمان، ژنهایی که برای زندگی انگلی مورد نیاز نبودند، خود از بین رفتند. باکتریهای ریکتزیا و کلامیدیا سلولهای زنده ای هستند که مانند ویروسها میتوانند تنها در سلولهای میزبان تولید مثل کنند. آنها به این نظریه اعتبار میدهند، زیرا احتمالاً وابستگی آنها به زندگی انگلی باعث از بین رفتن ژنهایی شدهاست که آنها را قادر میسازد تا در خارج از سلول زنده بمانند.[۱۶]
- نظریه خاستگاه سلولی
- برخی از ویروسها ممکن است از ذرات DNA یا RNA که از ژنهای یک ارگانیسم بزرگتر «فرار» کردهاند، تکامل یافته باشند. DNA فرار کرده میتواند از پلاسمیدها باشد (قطعات DNA که میتواند بین سلولها جابجا شود) در حالی که دیگران ممکن است از باکتریها تکامل یافته باشند
- نظریه تکاملی
- همزمان با ظهور اولین سلول بر روی زمین، ویروسها از مولکولهای پیچیده پروتئین و DNA تکامل یافتهاند و ممکن است که از میلیونها سال پیش به زندگی سلولی وابسته شده باشند.[۱۷]
با وجود همه این نظریهها، مشکلاتی وجود دارند: نظریه پسرفت توضیح نمیدهد که چرا حتی کوچکترین انگلهای سلولی به هیچ وجه شبیه ویروسها نیستند. نظریه خاستگاه سلولی ساختار ذرات ویروس را توضیح نمیدهد. نظریه تکاملی مغایر با تعریف ویروسها است، زیرا ویروس وابسته به سلولهای میزبان است.[۱۷] در کل ویروسها به عنوان موجودات باستانی شناخته میشوند و منشأ آنها به پیش از تقسیم حیات به ۳ حوزه بر میگردد.[۱۸] این اکتشافات باعث شدهاست که ویروس شناسان مدرن این سه فرضیه کلاسیک را مجدداً مورد بررسی و ارزیابی مجدد قرار دهند.[۱۸][۱۴]
ساختار

یک ذره ویروس که به عنوان ویریون هم شناخته میشود، از ژنهای ساخته شده از DNA یا RNA تشکیل شدهاست که توسط یک لایه محافظ پروتئینی به نام کپسید احاطه شدهاست.[۱۹]این کپسید از تعداد زیادی از مولکولهای یکسان پروتئینی کوچکتر ساخته شدهاست که به آنها کپسومر گفته میشود. چیدمان کپسومرها میتوانند به صورت ۲۰ وجهی، مارپیچی یا پیچیدهتر باشد. یک پوسته داخلی در اطراف DNA یا RNA به نام نوکلئوکپسید وجود دارد که توسط پروتئینها تشکیل میشود. بعضی از ویروسها توسط لایه ای از چربی به نام انولوپ احاطه شدهاند.
اندازه
ویروسها از کوچکترین عوامل عفونی هستند و بیشتر آنها فقط با میکروسکوپ الکترونی قابل مشاهده هستند. بیشتر ویروسها با میکروسکوپ نوری قابل مشاهده نیستند. اندازه آنها بین ۲۰ تا ۳۰۰ نانومتر است. آنها به قدری کوچک هستند که ۳۳٬۰۰۰ تا ۵۰۰٬۰۰۰ عدد ویروس در کنار هم یک سانتیمتر (۰٫۳۹ اینچ) طول دارند.[۱۹] در مقابل، اندازه باکتریها بهطور معمول حدود ۱ میکرومتر (۱۰۰۰ نانومتر) است و سلولهای موجودات پیشرفته تر چند ده میکرومتر دارند. برخی از ویروسها مانند مگاویروس و پاندوراویروس نسبتاً بزرگ (در حدود ۱ میکرومتر) هستند. این ویروسها که آمیبها را آلوده میکنند، در سال ۲۰۰۳ و ۲۰۱۳ کشف شدند. آنها تقریباً هزار برابر بزرگتر از ویروسهای آنفولانزا هستند و کشف این ویروسهای «غول پیکر» دانشمندان را شگفت زده کردهاست.
ژنها
ژنها از DNA و در بسیاری از ویروسها RNA ساخته میشوند. اطلاعات زیستی موجود در ارگانیسم در DNA یا RNA آن رمزگذاری میشود. بیشتر ارگانیسمها از DNA استفاده میکنند، اما بسیاری از ویروسها از RNA به عنوان ماده ژنتیکی خود استفاده میکنند. DNA یا RNA ویروسها شامل یک رشته یا مارپیچ دوگانه است.[۲۰]
ویروسها به سرعت تکثیر میشوند، زیرا آنها در مقایسه با انسان که ۲۰٬۰۰۰–۲۵٬۰۰۰ ژن دارد، تعداد بسیار کمتری ژن دارند.[۲۱] به عنوان مثال، ویروس آنفلوانزا تنها هشت ژن دارد و روتاویروس یازده عدد ژن دارد. این ژنها پروتئینهای ساختاری را تشکیل میدهند که در ذره ویروس موجود هستند یا پروتئینهای غیر ساختاری را تشکیل میدهند که فقط در سلولهای آلوده به ویروس یافت میشوند.[۲۲]
تمام سلولها و بسیاری از ویروسها، پروتئینهای آنزیمی به نام DNA پلیمراز و RNA پلیمراز تولید میکنند که نسخههای جدیدی از DNA و RNA را تشکیل میدهند. آنزیمهای پلیمراز ویروسی اغلب در ساخت DNA و RNA نسبت به آنزیمهای سلول میزبان بسیار مؤثر تر هستند.[۲۳]با این حال، آنزیمهای RNA پلیمراز اغلب دچار اشتباه میشوند و این یکی از دلایلی است که ویروسهای RNA اغلب برای تشکیل سویههای جدید جهش مییابند.[۲۴] در برخی از گونههای ویروس RNAدار، ژنها روی یک مولکول مداوم RNA نیستند بلکه جدا هستند. به عنوان مثال، ویروس آنفلوانزا دارای هشت ژن جدا و ساخته شده از RNA است. هنگامی که دو سویه مختلف ویروس آنفلوانزا یک سلول را آلوده میکنند، این ژنها میتوانند در فرآیندی به نام بازآرایی، گونههای جدید ویروس را مخلوط کرده و تولید کنند.[۲۵]
ساخت پروتئین

پروتئینها برای زندگی ضروری هستند. سلولها بر اساس اطلاعات کدنویسی شده در DNA، مولکولهای جدید پروتئین را از بلوکهای ساخت اسید آمینه تولید میکنند. هر نوع پروتئین یک مولکول اختصاصی است که معمولاً فقط یک عملکرد را انجام میدهد، بنابراین اگر یک سلول نیاز به انجام کار جدید دارد باید یک پروتئین جدید بسازد. ویروسها سلول را مجبور به ساختن پروتئینهای جدیدی میکند که سلول به آن نیاز ندارد، اما برای تولید مثل ویروس مورد نیاز است. ساخت پروتئین از دو مرحله اصلی تشکیل شدهاست: رونویسی و ترجمه.
رونویسی فرایندی است که در آن اطلاعات در DNA به نام کد ژنتیکی برای تولید نسخههای RNA به نام RNA پیامرسان (mRNA) استفاده میشود. این مواد از طریق سلول مهاجرت میکنند و رمز ژنتیکی را به ریبوزوم منتقل میکنند و در آن برای ساخت پروتئینها استفاده میگردند. این فرایند ترجمه نام دارد زیرا در آن ساختار اسید آمینه ای پروتئین توسط رمزهای روی RNA پیامرسان تعیین میشود. از این رو اطلاعات از زبان اسیدهای نوکلئیک به زبان اسیدهای آمینه ترجمه میشوند.
اسیدهای نوکلئیک بعضی از ویروسهای RNA مستقیماً به عنوان mRNA عمل میکنند. به همین دلیل به این ویروسها ویروس RNAدار با قطبیت مثبت گفته میشود.[۲۶] در سایر ویروسهای RNAدار، RNA رشته مکمل mRNA است و این ویروسها برای ساخت mRNA به آنزیمهای سلول یا خودشان متکی هستند. به این ویروسها ویروس RNAدار با قطبیت منفی گفته میشود. در ویروسهای دارای DNA، روش ساخت mRNA مشابه سلول است. ویروسهای گونه رتروویروس کاملاً متفاوت رفتار میکنند: آنها دارای RNA هستند، اما در داخل سلول میزبان یک نسخه DNA از RNA آنها با کمک آنزیم رونوشت بردار معکوس ساخته میشود. سپس این DNA در DNA خود میزبان گنجانیده میشود و توسط مسیرهای طبیعی سلول در mRNA تکثیر میشود.[۲۷]
چرخه زندگی
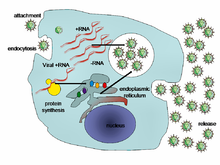
هنگامی که ویروس سلولی را آلوده میکند، ویروس آن سلول را مجبور میکند تا هزاران ویروس بیشتر ایجاد کند. ویروس این کار را با مجبور ساختن سلول برای تولید DNA یا RNA ویروسی و پروتئینهای ویروسی انجام میدهد که این ذرات برای تشکیل ویروس جدید سرهم میشوند.[۲۸]
شش چرخه پایه و همپوشان در چرخه زندگی ویروسها در سلولهای زنده وجود دارد:[۲۹]
- اتصال فرایند اتصال ویروس به مولکولهای خاص روی سطح سلول است. این ویژگی ویروس را به یک نوع سلول بسیار محدود محدود میکند. به عنوان مثال، ویروس نقص ایمنی بدن (HIV) فقط سلولهای T انسان را آلوده میکند، زیرا پروتئین سطح آن، gp120، تنها با CD4 و سایر مولکولهای موجود در سطح سلول T میتواند واکنش نشان دهد. ویروسهای گیاهی فقط میتوانند به سلولهای گیاهی متصل شوند و نمیتوانند حیوانات را آلوده کنند. این مکانیسم به نفع آن ویروسهایی که فقط سلولهایی را آلوده میکنند که در آنها قادر به تکثیر هستند، میباشد.
- نفوذ پس از اتصال اتفاق میافتد. ویروسها توسط اندوسیتوز یا با ادغام با سلول هدف به آن نفوذ میکنند.
- پوشش برداری هنگامی اتفاق میافتد که کپسید ویروسی توسط آنزیمهای ویروسی یا میزبان برداشته میشود، در نتیجه اسید نوکلئیک ویروسی برهنه میشود.
- تکثیر مرحله ای است که سلول از آر ان آ پیام رسان ویروسی در سیستمهای سنتز پروتئین خود برای تولید پروتئینهای ویروسی استفاده میکند. توانایی سنتز RNA یا DNA سلول باعث ایجاد DNA یا RNA ویروس میشود.
- سرهمبندی در سلول هنگامی اتفاق میافتد که پروتئینهای ویروسی و اسید نوکلئیک تازه ایجاد شده با یکدیگر ترکیب شوند تا صدها ذره ویروس جدید تشکیل شود.
- آزاد شدن هنگامی رخ میدهد که ویروسهای جدید فرار کرده یا از سلول آزاد میشوند. بیشتر ویروسها این کار را با تخریب سلولها در فرایندی به نام لیز انجام میدهند. ویروسهای دیگر مانند HIV یک فرآیندی به نام جوانه زدن به آرامی آزاد میشوند.
اثرات روی سلول میزبان
دامنه اثرات ساختاری و بیوشیمیایی ویروسها روی سلول میزبان گستردهاست.[۳۰] به این اثرات، اثرات سیتوپاتیک گفته میشود.[۳۱] بیشتر عفونتهای ویروسی سرانجام منجر به مرگ سلول میزبان میشوند. علل مرگ شامل لیز سلولی (ترکیدن)، تغییر در غشای سطح سلول و آپوپتوز (خودکشی سلول) است.[۳۲]غالباً مرگ سلول به دلیل قطع فعالیت طبیعی آن به علت پروتئینهای تولید شده توسط ویروس است که لزوماً این پروتئینها همگی از اجزای ویروس نیستند.[۳۳]
برخی از ویروسها باعث ایجاد تغییرات ظاهری در سلول آلوده نمیشوند. سلولهایی که ویروس در آنها نهفته و غیرفعال است، علائم کمی از عفونت را نشان میدهد و معمولاً بهطور طبیعی کار میکنند.[۳۴] این امر باعث عفونت پایدار میشود و ویروس اغلب برای ماهها یا سالها خنثی باقی میماند. این نوع عفونت اغلب در مورد ویروسهای هرپس اتفاق میافتد.[۳۵][۳۶]
بعضی از ویروسها، مانند ویروس اپشتین بار، اغلب باعث تکثیر سلولها بدون ایجاد بدخیمی میشوند،[۳۷] اما برخی دیگر از ویروسها مانند پاپیلوما ویروس از علل اصلی ایجاد سرطان هستند.[۳۸] هنگامی که DNA سلول توسط یک ویروس آسیب ببیند و سلول نتواند خود را ترمیم کند، اغلب منجر به آپوپتوز میشود. یکی از نتایج آپوپتوز تخریب DNA آسیب دیده توسط خود سلول است. بعضی از ویروسها مکانیسمهایی برای محدود کردن آپوپتوز دارند به طوری که سلول میزبان قبل از تولید ویروسهای جدید از بین نرود. به عنوان مثال HIV این کار را میکند.[۳۲]
ویروسها و بیماریها

بیماریهای شایع انسانی ناشی از ویروسها شامل سرماخوردگی، آنفولانزا، آبله مرغان و تبخال است. بیماریهای جدی مانند ابولا و ایدز نیز در اثر ویروسها ایجاد میشود. بسیاری از ویروسها بیماریزا نیستند یا باعث بیماریهای خفیف میشوند و گفته میشود که «خوشخیم» هستند. ویروسهای مضرتر به عنوان بیماریزا توصیف میشوند. بسته به نوع سلول آلوده شده، ویروسها باعث ایجاد بیماریهای مختلف میشوند. بعضی از ویروسها میتوانند باعث عفونتهای مادام العمر یا مزمن شوند که در این بیماریها، ویروس با وجود مکانیسمهای دفاعی میزبان همچنان در بدن تکثیر میشود.[۳۹]این اتفاق در ویروس هپاتیت ب و عفونتهای ویروس هپاتیت سی شایع است. افراد مزمن مبتلا به ویروس به عنوان ناقل شناخته میشوند. آنها به عنوان مخزن مهم ویروس عمل میکنند. اگر تعداد بالایی از ناقلین در یک جمعیت معین وجود داشته باشد، به این حالت، بیماری بومی گفته میشود.[۴۰]
روشهای زیادی وجود دارد که ویروسها از میزبانی به میزبان دیگر گسترش پیدا میکنند اما هر ویروس فقط از یک یا دو روش استفاده میکند. ویروسهای زیادی که باعث آلوده شدن گیاهان میشوند توسط ارگانیسمها منتقل میشوند. این ارگانیسمها ناقل نامیده میشوند. برخی از ویروسهایی که حیوانات از جمله انسانها را آلوده میکنند نیز توسط ناقلین و معمولاً حشرات خونخوار گسترش مییابند. با این حال ، انتقال مستقیم شایع تر است. برخی از عفونتهای ویروسی، مانند نورو ویروس و روتاویروس، توسط مواد غذایی آلوده و آب، دستها و اشیاء عمومی و با تماس نزدیک با فرد آلوده دیگر پخش میشوند، در حالی که برخی دیگر از راه هوایی (ویروس آنفولانزا) منتقل میشوند. ویروسهایی مانند HIV، هپاتیت ب و هپاتیت سی اغلب توسط رابطه جنسی محافظت نشده یا فرورفت سوزن آلوده به زیرجلد منتقل میشوند. برای جلوگیری از عفونتها و همهگیریها، مهم است که راههای انتقال ویروس شناخته شوند.[۴۱]
بیماریهای گیاهان

انواع مختلفی از ویروسهای گیاهی وجود دارد، اما اغلب آنها فقط باعث کاهش بازدهی میشوند و تلاش برای کنترل آنها از نظر اقتصادی مناسب نیست. ویروسهای گیاهی اغلب توسط ارگانیسمها (ناقلها) از گیاهی به گیاه دیگر پخش میشوند. اینها ناقلها معمولاً حشرات هستند، اما برخی قارچها، کرمهای نماتود و ارگانیسمهای تک سلولی هم ناقل هستند. هنگامی که کنترل عفونتهای ویروسی گیاه مقرون به صرفه تلقی میشود (مثلاً میوههای چند ساله) در کشتن ناقلها و از بین بردن میزبانهای جایگزین مانند علفهای هرز تلاش میشود.[۴۲] ویروسهای گیاهی برای انسان و سایر حیوانات بیضرر هستند زیرا تنها میتوانند در سلولهای زنده گیاه تولید مثل کنند.[۴۳]
باکتریوفاژها
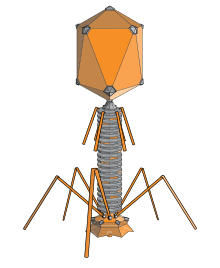
باکتریوفاژها ویروسهایی هستند که باکتریها و باستانیان را آلوده میکنند. کمیته بینالمللی طبقهبندی ویروسها بهطور رسمی ۲۸ جنس باکتریوفاژ را که متعلق به ۱۱ خانواده است، به رسمیت میشناسد.[۴۴] باکتریوفاژها در محیط زیست دریایی مهم هستند: با تخریب باکتریهای آلوده، ترکیبات کربن دوباره به داخل محیط آزاد میشوند و این امر باعث رشد اقتصادی ارگانیک میشود. باکتریوفاژها در تحقیقات علمی مفید هستند زیرا برای انسان بیضرر هستند و به راحتی قابل مطالعه هستند. این ویروسها میتوانند در صنایعی که از طریق تخمیر مواد غذایی و دارویی تولید میکنند و به باکتریهای سالم وابسته هستند، مشکل ایجاد کنند. کنترل برخی از عفونتهای باکتریایی با کنترل آنتیبیوتیکها رو به سختی میرود، بنابراین علاقه زیادی به استفاده از باکتریوفاژها برای درمان این عفونتها در انسان وجود دارد.[۴۵]
مقاومت میزبان
ایمنی ذاتی حیوانات
حیوانات، از جمله انسانها، در برابر ویروسها مکانیسمهای طبیعی دفاعی زیادی دارند. برخی از آنها غیر اختصاصی هستند و در برابر بسیاری از ویروسها صرف نظر از نوع، محافظت میکنند. این مصونیت ذاتی با قرار گرفتن مکرر در برابر ویروسها بهبود نمییابد و «خاطره» عفونت را حفظ نمیکند. پوست حیوانات، به ویژه سطح آن، که از سلولهای مرده ساخته شدهاست، مانع از آلوده شدن بسیاری از ویروسها به میزبان میشود. اسیدیته محتویات معده ویروسهای زیادی را که بلعیده شدهاند از بین میبرد. هنگامی که ویروس بر این موانع غلبه کرده و وارد میزبان میشود، سایر مکانیسمهای ایمنی ذاتی مانع از انتشار عفونت در بدن میشوند. در صورت وجود ویروس، هورمون ویژه ای به نام اینترفرون توسط بدن تولید میشود و این امر با از بین بردن ویروسها به وسیله کشتن سلول آلوده و همسایگان نزدیک آن متوقف میشود. در داخل سلولها آنزیمهایی وجود دارد که RNA ویروسها را از بین میبرد. به این حالت آرانای مداخلهگر گفته میشود. برخی از سلولهای خونی سلولهای آلوده به ویروس را درگیر و نابود میکنند.[۴۶]
ایمنی اکتسابی در حیوانات
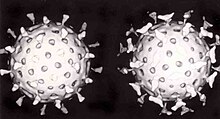
ایمنی اختصاصی به ویروسها به مرور زمان ایجاد میشود و گلبولهای سفید به نام لنفوسیتها نقش اصلی را در این ایمنی ایفا میکنند. لنفوسیتها «خاطره ای» از عفونتهای ویروسی حفظ میکنند و مولکولهای خاصی به نام آنتیبادی تولید میکنند. این آنتیبادیها به ویروس متصل شده و ویروس را از آلوده سازی سلولهای دیگر بازمیدارند. آنتیبادیها به شدت انتخابی هستند و فقط به یک نوع ویروس حمله میکنند. بدن آنتیبادیهای مختلفی ایجاد میکند، به خصوص در هنگام عفونت اولیه. با این حال، پس از فروکش عفونت، برخی از آنتیبادیها باقی مانده و تولید میشوند که اغلب به میزبان ایمنی مادام العمر علیه آن ویروس میدهد.[۴۷]
مقاومت گیاهیان
گیاهان دارای مکانیسمهای دفاعی مفصل و مؤثری در برابر ویروسها هستند. یکی از مؤثرترین آنها وجود ژنهای مقاومت است. هر ژن مقاومت، مقاومت در برابر یک ویروس خاص را القا میکند و این کار را از طریق تحریک مناطق موضعی اطراف سلول آلوده، که اغلب با چشم غیرمستقیم به صورت نقاط بزرگی قابل مشاهده است، انجام میدهد. این امر مانع از انتشار عفونت میشود.[۴۸] آرانای مداخلهگر در گیاهان نیز به عنوان یک دفاع مؤثر عمل میکند.[۴۹] اغلب گیاهان هنگامی که آلوده میشوند، ضد عفونی کنندههای طبیعی تولید میکنند که ویروسها را از بین میبرد، مانند اسید سالیسیلیک، نیتریک اکسید و مولکولهای اکسیژن واکنش پذیر.[۵۰]
مقاومت به باکتریوفاژ
راه اصلی دفاع از باکتریها در برابر باکتریوفاژها، تولید آنزیمهایی است که DNA خارجی را از بین میبرد. این آنزیمها که اندونوکلئازهای محدودکننده نام دارند، DNA ویروسی را که باکتریوفاژها به سلولهای باکتریایی تزریق میکنند، قطع میکنند.
پیشگیری و درمان بیماری ویروسی در انسان و حیوانات دیگر
واکسنها

واکسیناسیون روشی برای جلوگیری از بیماریهای ناشی از ویروسها است. واکسنها یک عفونت طبیعی و پاسخ ایمنی مرتبط با آن را شبیهسازی میکنند، اما باعث بیماری نمیشوند. استفاده از آنها منجر به ریشه کنی آبله مرغان و کاهش چشمگیر بیماری و مرگ ناشی از عفونتهایی مانند فلج اطفال، سرخک، اوریون و سرخچه شدهاست.[۵۱] Vaccines are available to prevent over fourteen viral infections of humans[۵۲] واکسنها برای جلوگیری از بیش از چهارده عفونت ویروسی انسانی موجود هستند[۵۲] و تعدادی بیشتری نیز برای عفونتهای حیوانی ساخته شدهاند.[۵۳] واکسنها ممکن است شامل ویروس زنده یا کشته شده باشند.[۵۴]واکسنهای زنده حاوی اشکال تضعیف شده از ویروس هستند، اما این واکسنها در صورت استفاده شدن برای افرادی که ایمنی ضعیفی دارند میتوانند خطرناک باشند. در این افراد، ویروس تضعیف شده میتواند باعث بیماری اصلی شود.[۵۵] تکنیکهای بیوتکنولوژی و مهندسی ژنتیک برای تولید واکسنهای «نوترکیب» که فقط پروتئینهای کپسید ویروسی را دارند، استفاده میشود. واکسن هپاتیت بی نمونه ای از این نوع واکسنهاست.[۵۶] این واکسنها ایمن تر هستند زیرا هرگز نمیتوانند باعث ایجاد بیماری شوند.[۵۴]
داروی ضد ویروس

از اواسط دهه ۱۹۸۰، توسعه داروهای ضد ویروسی به سرعت افزایش یافتهاست که دلیل عمده این تلاشها، همهگیری بیماری ایدز میباشد. داروهای ضد ویروسی اغلب آنالوگ نوکلئوزید هستند که مولکولهای بسیار مشابهی دارند اما با بلوکهای ساختمانی DNA یکسان نیستند. هنگامی که تکثیر DNA ویروس شروع میشود، برخی از این بلوکهای ساختگی جعلی در ژنوم ویروس گنجانیده میشوند. به محض این اتفاق میافتد، تکثیر متوقف میشود. بلوکهای ساختگی جعلی فاقد ویژگیهای اساسی هستند که امکان افزودن بلوکهای بیشتر را فراهم میکند؛ بنابراین، تولید DNA متوقف شده و ویروس دیگر نمیتواند تولید مثل کند.[۵۷] نمونههایی از آنالوگهای نوکلئوزید عبارتند از: آسیکلوویر برای عفونت ویروس هرپس و لامیوودین برای عفونت ویروس ایدز و هپاتیت بی. آسیکلوویر یکی از قدیمیترین و رایجترین داروهای ضد ویروسی است.[۵۸]
سایر داروهای ضد ویروسی مراحل مختلف چرخه زندگی ویروسی را هدف قرار میدهند. HIV برای عفونی بودن به آنزیمی بنام پروتئاز اچآیوی وابسته است. طبقه ای از داروها به نام بازدارندههای پروتئاز وجود دارد که به این آنزیم متصل میشوند و عملکرد آن را متوقف میکنند.[۵۹]
هپاتیت C در اثر ویروسی RNA دار ایجاد میشود. در ۸۰٪ از افراد آلوده، این بیماری مزمن میشود و تا آخر عمر میماند مگر اینکه درمان شود. برای درمان آن، یک روش مؤثر وجود دارد که از داروی آنالوگ نوکلئوزید ریباویرین به همراه اینترفرون استفاده میکند.[۶۰] درمان برای حاملان مزمن ویروس هپاتیت B با استفاده از یک استراتژی مشابه با استفاده از لامیوودین و سایر داروهای ضد ویروس انجام شدهاست.[۶۱] در هر دو بیماری، داروها تولید مثل ویروس را متوقف میکنند و اینترفرون سلولهای آلوده باقی مانده را از بین میبرد.
عفونت HIV معمولاً با ترکیبی از داروهای ضد ویروسی درمان میشود که هریک مرحله مختلفی از چرخه زندگی ویروس را هدف قرار میدهد. داروهایی وجود دارد که مانع از اتصال ویروس به سلولها میشود، برخی دیگر که آنالوگ نوکلئوزید هستند و برخی از آنزیمهای ویروس را که برای تکثیر موردنیاز هستند را از خنثی میکنند.[۵۹] موفقیت این داروها، اثبات اهمیت آشنایی با نحوه تولید مثل ویروسها است.
نقش در بومشناسی
ویروسها فراوانترین موجود زیستی در محیطهای آبی هستند.[۶۲] (حدود یک میلیون ویروس در یک قاشق چایخوری از آب دریا وجود دارد)[۶۳]و آنها برای تنظیم اکوسیستمهای آب شور و آب شیرین ضروری هستند.[۶۴] بیشتر این ویروسها باکتریوفاژها هستند که برای گیاهان و حیوانات بیضرر هستند. آنها باکتریها را در جوامع میکروبی آبزی آلوده کرده و از بین میبرند و این مهمترین مکانیسم بازیافت کربن در محیط دریایی است. مولکولهای آلی که توسط ویروسها از سلولهای باکتریایی آزاد میشوند رشد باکتریها و جلبکهای تازه را تحریک میکنند.[۶۵]
میکروارگانیسمها بیش از ۹۰٪ زیست توده دریا را تشکیل میدهند. تخمین زده میشود که ویروسها تقریباً ۲۰٪ از این زیست توده را هر روز از بین میبرند و تعداد ویروسها در اقیانوسها ۱۵ برابر باکتریها و باستانیان است. ویروسها عمدتاً مسئول نابودی سریع شکوفاییهای جلبکی زیانبار[۶۶] که اغلب زیستبومهای دیگر را نبود میکنند، هستند.[۶۷]تعداد ویروسهای موجود در اقیانوسها بیشتر در تعداد ویروسهای خارج از آب ساحل است و تعدادشان با عمیقتر شدن آب کاهش مییابد. زیرا در آن جا میزبانان کمتری دارند.[۶۸]
تأثیرات آنها بسیار وسیع است. با افزایش مقدار تنفس در اقیانوسها، ویروسها بهطور غیرمستقیم مسئول کاهش میزان دیاکسید کربن در جو به میزان تقریباً ۳ گیگاتن کربن در سال هستند.[۶۸]
پستانداران دریایی نیز مستعد ابتلا به عفونتهای ویروسی هستند. در سالهای ۱۹۸۸ و ۲۰۰۲، هزاران فک بندرگاه در اروپا توسط ویروس دیستمپر فک کشته شدند.[۶۹] بسیاری از ویروسهای دیگر، از جمله ویروس کالیسی، هرپسویروس، آدنوویروس و پاروویروس در جمعیت پستانداران دریایی گردش میکنند.[۶۸]
جستارهای وابسته
پانویس
- ↑ Leppard, Keith; Nigel Dimmock; Easton, Andrew (2007). Introduction to Modern Virology. Blackwell Publishing Limited. p. 4. ISBN 978-1-4051-3645-7.
- ↑ Shors p. 6
- ↑ Topley and Wilson p. 3
- ↑ Shors p. 827
- ↑ D'herelle, F (2007). "On an invisible microbe antagonistic toward dysenteric bacilli: brief note by Mr. F. D'Herelle, presented by Mr. Roux. 1917". Research in Microbiology. 158 (7): 553–4. doi:10.1016/j.resmic.2007.07.005. PMID 17855060.
- ↑ From Nobel Lectures, Physics 1981–1990, (1993) Editor-in-Charge Tore Frängsmyr, Editor Gösta Ekspång, World Scientific Publishing Co. , Singapore
- ↑ Stanley, W.M.; Loring, H.S. (1936). "The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants". Science. 83 (2143): 85. Bibcode:1936Sci....83...85S. doi:10.1126/science.83.2143.85. PMID 17756690.
- ↑ Stanley, W.M.; Lauffer, M.A. (1939). "Disintegration of tobacco mosaic virus in urea solutions". Science. 89 (2311): 345–347. Bibcode:1939Sci....89..345S. doi:10.1126/science.89.2311.345. PMID 17788438.
- ↑ Goodpasture EW, Woodruff AM, Buddingh GJ (October 1931). "The Cultivation Of Vaccine and other Viruses In The Chorioallantoic Membrane of Chick Embryos". Science. 74 (1919): 371–2. Bibcode:1931Sci....74..371G. doi:10.1126/science.74.1919.371. PMID 17810781.
- ↑ Rosen FS (October 2004). "Isolation of poliovirus--John Enders and the Nobel Prize". N. Engl. J. Med. 351 (15): 1481–3. doi:10.1056/NEJMp048202. PMID 15470207.
- ↑ Shors. p. 16
- ↑ Topley and Wilson pp. 18–19
- ↑ Liu Y, Nickle DC, Shriner D, Jensen MA, Learn GH, Mittler JE, Mullins JI (November 2004). "Molecular clock-like evolution of human immunodeficiency virus type 1". Virology. 329 (1): 101–8. doi:10.1016/j.virol.2004.08.014. PMID 15476878.
- ↑ ۱۴٫۰ ۱۴٫۱ ۱۴٫۲ Krupovic, M; Dolja, VV; Koonin, EV (2019). "Origin of viruses: primordial replicators recruiting capsids from hosts". Nature Reviews Microbiology. doi:10.1038/s41579-019-0205-6. PMID 31142823.
- ↑ Topley and Wilson pp.11–21
- ↑ Topley and Wilson p. 11
- ↑ ۱۷٫۰ ۱۷٫۱ Wessner D. R. (2010). "The Origins of Viruses". Nature Education. 3 (9): 37.
- ↑ ۱۸٫۰ ۱۸٫۱ Mahy WJ & Van Regenmortel MHV (eds). Desk Encyclopedia of General Virology. Oxford: Academic Press; 2009. ISBN 0-12-375146-2. p. 28.
- ↑ ۱۹٫۰ ۱۹٫۱ Topley and Wilson pp. 33–55
- ↑ Shors p. 81
- ↑ International Human, Genome Sequencing Consortium (2004). "Finishing the euchromatic sequence of the human genome". Nature. 431 (7011): 931–945. Bibcode:2004Natur.431..931H. doi:10.1038/nature03001. PMID 15496913.
- ↑ Shors p. 129
- ↑ Shors pp. 129–131
- ↑ Shors p. 652
- ↑ Shors p. 654
- ↑ Topley and Wilson pp. 75–82
- ↑ Shors p. 698
- ↑ Shors pp. 6–13
- ↑ Shors pp. 121–123
- ↑ Collier pp. 115–146
- ↑ Collier p. 115
- ↑ ۳۲٫۰ ۳۲٫۱ Roulston A, Marcellus RC, Branton PE (1999). "Viruses and apoptosis". Annu. Rev. Microbiol. 53: 577–628. doi:10.1146/annurev.micro.53.1.577. PMID 10547702.
- ↑ Alwine JC (2008). Modulation of host cell stress responses by human cytomegalovirus. Curr. Top. Microbiol. Immunol. Current Topics in Microbiology and Immunology. Vol. 325. pp. 263–79. doi:10.1007/978-3-540-77349-8_15. ISBN 978-3-540-77348-1. PMID 18637511.
- ↑ Sinclair J (March 2008). "Human cytomegalovirus: Latency and reactivation in the myeloid lineage". J. Clin. Virol. 41 (3): 180–5. doi:10.1016/j.jcv.2007.11.014. PMID 18164651.
- ↑ Jordan MC, Jordan GW, Stevens JG, Miller G (June 1984). "Latent herpesviruses of humans". Ann. Intern. Med. 100 (6): 866–80. doi:10.7326/0003-4819-100-6-866. PMID 6326635.
- ↑ Sissons JG, Bain M, Wills MR (February 2002). "Latency and reactivation of human cytomegalovirus". J. Infect. 44 (2): 73–7. doi:10.1053/jinf.2001.0948. PMID 12076064.
- ↑ Barozzi P, Potenza L, Riva G, Vallerini D, Quadrelli C, Bosco R, Forghieri F, Torelli G, Luppi M (December 2007). "B cells and herpesviruses: a model of lymphoproliferation". Autoimmun Rev. 7 (2): 132–6. doi:10.1016/j.autrev.2007.02.018. PMID 18035323.
- ↑ Subramanya D, Grivas PD (November 2008). "HPV and cervical cancer: updates on an established relationship". Postgrad Med. 120 (4): 7–13. doi:10.3810/pgm.2008.11.1928. PMID 19020360.
- ↑ Shors p. 4643
- ↑ Topley and Wilson p. 766
- ↑ Shors p. 32
- ↑ Shors p. 822
- ↑ Shors pp. 802–803
- ↑ Fauquet, CM (2009). Desk Encyclopedia of General Virology. Boston: Academic Press. p. 82. ISBN 978-0-12-375146-1.
- ↑ Shors p. 803
- ↑ Shors pp. 116–117
- ↑ Shors pp.225–233
- ↑ Dinesh-Kumar, S.P.; Tham, Hong; -1#Wai-, Baker (2000). "Structure—function analysis of the tobacco mosaic virus resistance gene N". PNAS. 97 (26): 14789–94. Bibcode:2000PNAS...9714789D. doi:10.1073/pnas.97.26.14789. PMC 18997. PMID 11121079.
- ↑ Shors p. 812
- ↑ Soosaar, J.L.; Burch-Smith, T.M.; Dinesh-Kumar, S.P. (2005). "Mechanisms of plant resistance to viruses". Nature Reviews Microbiology. 3 (10): 789–98. doi:10.1038/nrmicro1239. PMID 16132037.
- ↑ Shors pp. 237–255
- ↑ ۵۲٫۰ ۵۲٫۱ Small JC, Ertl HC (2011). "Viruses - from pathogens to vaccine carriers". Current Opinion in Virology. 1 (4): 241–5. doi:10.1016/j.coviro.2011.07.009. PMC 3190199. PMID 22003377.
- ↑ Pastoret, P.P.; Schudel, A.A.; Lombard, M. (2007). "Conclusions—future trends in veterinary vaccinology". Rev. Off. Int. Epizoot. 26 (2): 489–94, 495–501, 503–9. doi:10.20506/rst.26.2.1759. PMID 17892169.
- ↑ ۵۴٫۰ ۵۴٫۱ Shors p. 237
- ↑ Thomssen, R. (1975). "Live attenuated versus killed virus vaccines". Monographs in Allergy. 9: 155–76. PMID 1090805.
- ↑ Shors p. 238
- ↑ Shors p. 514−515
- ↑ Shors p. 514
- ↑ ۵۹٫۰ ۵۹٫۱ Shors p. 568
- ↑ Witthöft T, Möller B, Wiedmann KH, Mauss S, Link R, Lohmeyer J, et al. (November 2007). "Safety, tolerability and efficacy of peginterferon alpha-2a and ribavirin in chronic hepatitis C in clinical practice: The German Open Safety Trial". J. Viral Hepat. 14 (11): 788–96. doi:10.1111/j.1365-2893.2007.00871.x. PMC 2156112. PMID 17927615.
- ↑ Paul N, Han SH (June 2011). "Combination Therapy for Chronic Hepatitis B: Current Indications". Curr Hepat Rep. 10 (2): 98–105. doi:10.1007/s11901-011-0095-1. PMC 3085106. PMID 21654909.
- ↑ Koonin EV, Senkevich TG, Dolja VV (September 2006). "The ancient Virus World and evolution of cells". Biol. Direct. 1: 29. doi:10.1186/1745-6150-1-29. PMC 1594570. PMID 16984643.
- ↑ Shors p. 25
- ↑ Shors p. 5
- ↑ Shors p. 25−26
- ↑ Suttle CA (September 2005). "Viruses in the sea". Nature. 437 (7057): 356–61. Bibcode:2005Natur.437..356S. doi:10.1038/nature04160. PMID 16163346.
- ↑ "Harmful Algal Blooms: Red Tide: Home | CDC HSB". www.cdc.gov. Retrieved 23 August 2009.
- ↑ ۶۸٫۰ ۶۸٫۱ ۶۸٫۲ Suttle CA (October 2007). "Marine viruses--major players in the global ecosystem". Nat. Rev. Microbiol. 5 (10): 801–12. doi:10.1038/nrmicro1750. PMID 17853907.
- ↑ Hall, A; Jepson, P; Goodman, S; Harkonen, T (2006). "Phocine distemper virus in the North and European Seas – Data and models, nature and nurture". Biological Conservation. 131 (2): 221–229. doi:10.1016/j.biocon.2006.04.008.
| منابع کتابخانهای دربارۀ Virus |
