سیال فوق بحرانی
سیال فوق بحرانی (انگلیسی:supercritical fluid) به هر مادهای که بالاتر از فشار و دمای آن در نقطه بحرانی باشد گفته میشود. جائی که فازهای گاز و مایع از یکدیگر متمایز نیستند. اینگونه از سیالات میتوانند همچون گازها بینابین جامدات پراکنده شوند یا به مانند مایعات، مواد را در خود حل کنند. در نزدیکی نقطه بحرانی هر گونه تغییر اندک در فشار یا دما باعث یک تغییر عظیم در چگالی میشود. سیالات فوق بحرانی بسیار مناسب جهت جایگزینی برای حلالهای ارگانیگ در فرایندهای صنعتی و آزمایشگاهی هستند. از پرکاربردترین سیالات فوق بحرانی میتوان به کربن دیاکسید و آب اشاره کرد که در کافئین زدایی و تولید قدرت (نیروگاهها) استفاده میشوند.
ویژگیها[ویرایش]
در ویژگیهای عمومی، سیالات فوق بحرانی ویژگیهای تلفیقی از گاز و مایع را دارا میباشند. در جدول ۱، ویژگیهای بحرانی چند ماده فوق بحرانی آورده شدهاست.
| محلول | جرم مولی
گرم بر مول |
دمای بحرانی
بر حسب کلوین |
دمای بحرانی
بر حسب مگا پاسکال (اتمسفر) |
چگالی بحرانی |
|---|---|---|---|---|
| کربن دیاکسید (CO2) | ۴۴٫۰۱ | ۳۰۴٫۱ | ۷٫۳8(72.8) | ۰٫۴۶۹ |
| آب(H2O) | ۱۸٫۰۱۵ | ۶۴۷٫۰۹۶ | ۲۲٫۰۶4(217.755) | ۰٫۳۲۲ |
| متان(CH4) | ۱۶٫۰۴ | ۱۹۰٫۴ | ۴٫۶0(45.4) | ۰٫۱۶۲ |
| اتان(C2H6) | ۳۰٫۰۷ | ۳۰۵٫۳ | ۴٫۸7(48.1) | ۰٫۲۰۳ |
| پروپان(C3H8) | ۴۴٫۰۹ | ۳۶۹٫۸ | ۴٫۲5(41.9) | ۰٫۲۱۷ |
| اتیلن (C2H4) | ۲۸٫۰۵ | ۲۸۲٫۴ | ۵٫۰4(49.7) | ۰٫۲۱۵ |
| پروپیلن(C3H6) | ۴۲٫۰۸ | ۳۶۴٫۹ | ۴٫۶0(45.2) | ۰٫۲۳۲ |
| متانول(CH3OH) | ۳۲٫۰۴ | ۵۱۲٫۶ | ۸٫۰9(79.8) | ۰٫۲۷۲ |
| اتانول (C2H5OH) | ۴۶٫۰۷ | ۵۱۳٫۹ | ۶٫۱4(60.6) | ۰٫۲۷۶ |
| استون(C3H6O) | ۵۸٫۰۸ | ۵۰۸٫۱ | ۴٫۷0(46.4) | ۰٫۲۷۸ |
| دی نیتروژن مونوکسید (N2O) | ۴۴٫۰۱۳ | ۳۰۶٫۵۷ | ۷٫۳5(72.5) | ۰٫۴۵۲ |
| چگالی (kg/m3) | ویسکوزیته(µPa·s) | انتشار(mm2/s) | |
|---|---|---|---|
| گازها | ۱ | ۱۰ | ۱–۱۰ |
| سیالات فوق بحرانی | ۱۰۰–۱۰۰۰ | ۵۰–۱۰۰ | ۰٫۰۱–۰٫۱ |
| مایعات | ۱۰۰۰ | ۵۰۰–۱۰۰۰ | ۰٫۰۰۱ |
در سیالهای فوق بحرانی، هیچ گونه کشش سطحی وجود ندارد. این بدین دلیل است که در آن دما و فشار، هیچ گونه مرزی بین فازهای گاز و مایع وجود ندارد. با ایجاد تغییر در دما یا گاز سیال، میتوان ویژگیهای سیال را به گونهای تنظیم کرد که سیال ما رفتاری همانند گاز یا مایع بگیرد. یکی از مهمترین ویژگیهای سیال فوق بحرانی، انحلال پذیری آن است. در دمای ثابت، انحلالپذیری در سیال فوق بحرانی با چگالی آن رابطه مستقیم دارد. از طرفی تغیرات در فشار باعث تا ایجاد تغییرات در چگالی میشود. پس میتوان گفت با افزایش فشار، انحلالپذیری سیال افزایش مییابد. رابطه انحلالپذیری با دما کمی پیچیدهتر هست. در چگالی ثابت، انحلالپذیری با افزایش دما، افزایش مییابد. اما در نزدیکی نقطه بحرانی چگالی دچار یک افت شدید میشود که با افزایش دمای اندکی همراه است. در هر حال در نزدیکی دمای بحرانی، در اکثر مواقع، انحلالپذیری با افزایش دما، کاهش مییابد و پس از مدتی، دوباره افزایش مییابد.[۲]
همه سیالات فوق بحرانی نسبت به یک دیگر قابلیت امتزاج دارند. پس میتوان یک محلول دو فازی را با رسیدن به دمای فوق بحرانی به یک محلول تک فازی تبدیل کرد. دمای بحرانی محلول جدید را نیز میتوان را با میانگین حسابی گرفتن از دما و فشار بحرانی دو جز تخمین زد.
- Tc(mix) = (mole fraction A) × TcA + (mole fraction B) × TcB
با استفاده از معادلات حالت، چون پنگ رابینسون (Peng Robinson) یا روش مشارکت گروهی (group contribution) میتوان دمای بحرانی یا دیگر ویژگیها همچون چگالی را با دقت بالا به دست آورد.[۳]
دیاگرام فاز[ویرایش]
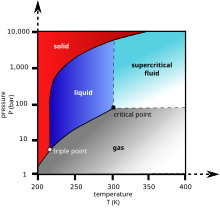

شکلهای ۱ و ۲ نمایانگر نمودار فازی هستند. در نموداری فازی فشار بر حسب دما (شکل ۱) دمای جوش، مرزی بین گاز و مایع ایجاد کرده که در نقطه بحرانی پایان میگیرد. جاییکه فازهای مایع و گاز ناپدید میشوند تا یک فاز فوق بحرانی را تشکیل بدهند. این موضوع را میتوان در نمودار فازی چگالی بر حسب فشار گاز کربن دیاکسید (شکل ۲) نیز مشاهده کرد. در دماهایی پایینتر از دما بحرانی، (۲۸۰ کلوین) فشار افزایش مییابد و گاز فشرده میشود (بیشتر از ۴۰ بار) و به مایع چگالتر منبفض میشود که به صورت خطهای نقطه چین بر روی نمودار قابل مشاهده است.
سیستم در تعادل دارای دو فاز است. مایعی با چگالی بالا و گاز با چگالی پایین. با افزایش دمای بحرانی (تا ۳۰۰ کلوین) بر چگالی گاز افزوده و از چگالی مایع کاسته میشود. در وضعیت بحرانی (۳۰۴٫۱ کلوین و ۷٫۳۸ مگا پاسکال) هیچ تفاوتی در چگالی وجود ندارد و دو فاز مایع و گاز به یک فاز بدل گشتهاند. از این رو، در دمای بالاتر از دمای بحرانی، گاز نمیتواند تحت تأثیر فشار مایع گردد. کمی بالاتر از دمای بحرانی (۳۱۰ کلوین)، در همسایگی فشار بحرانی، خط تقریباً افقی است. افزایش اندک در فشار باعث افزایش عظیمی در چگالی فاز فوق بحرانی ما دارد. در دماهای بالاتر، سیال شروع به رفتار به مانند گازها میکند. همانگونه که در شکل ۲ نمایان است، برای کربن دیاکسید در دمای ۴۰۰ کلوین، چگالی تقریباً به صورت خطی با فشار تغییر میکند.
بسیاری دیگر از ویژگیهای فیزیک ماده از جمله ویسکوزیته و گذردهی نسبی و مقاومت محلول در نزدیکی نقطه بحرانی، با شیب تندی تغییر میکنند.
تاریخچه[ویرایش]
در سالهای اخیر، تلاشهای برجستهای برای جستجو و کشف خاصیتهای گوناگون سیالات فوق بحرانی صورت گرفتهاست. سابقهٔ این کوششها به سال ۱۸۲۲ بر میگردد. چارلز کانیار د لا تور (Baron Charles Cagniard de la Tour)، دانشمند فرانسوی، هنگامیکه در حال آزمایش بر روی اختلالات صوت درون یک لوله توپ جنگی مملوء از سیالات مختلف در دمایهای بالا بود، برای اولین بار با سیال فوق بحرانی روبه رو شد.
ترمودینامیک[ویرایش]

کمی بعد، تحقیقات در حوزه سیالات فوق بحرانی توسعه بیشتری یافت و کاربردهای گستردهتری به خود گرفت. کاربردهایی از استخراج عطر گلها تا استخراج کافئین از قهوه. عناصر غذاهای فراسودمند، داروها، لوازم آرایشی، پلیمرها، پودرها، مواد فرا بیولوژیکی، نانو سیستمها، تولیدات طبیعی، بیوتکنولوژیها، سوختهای فسیلی، سوختهای بیوفسیلی؛ میکلروالکترونیکها، انرژی و محیط زیست. یخش اعظمی از تحقیقات و تلاشهای دهههای اخیر در جهت افزایش پیشرفت و توسعه در ابزآلات آزمایشگاه صورت گرفتهاست.
دیما بولماتوف، براژکین و تراچنکو کشف کردهاند که ظرفیت گرمایی در واقع تقاطعی است بین دو سازمان دینامیکی متفاوتی که ما در یک مایع سخت در دمای پایین و یک گاز غیر صلب با دمای بالا (مانند سیالات) شاهد هستیم. مایعات سخت در با مقیاس کوتاه مدت، درست به مانند جامدات عمل میکنند ولی در مقیاس زمانی بلند مدت به مانند دیگر مایعات جاری میشوند.[۴]
گاز بحرانی همانند سیالات، حرکت دینامیکی مشابه گازها دارند، اما از طرف دیگر به مانند مایعات توانایی حل کردن دیگر مواد را در خود دارا میباشند. این روزها این باور که بین گاز و مایع در دماهای بالاتر از نقطه بحرانی هیچ تفاوتی نمیتوان قائل شد توسط دانشمندان روسی به چالش کشیده شدهاست. بالماتوف و همکارانش ترمودینامیک سیستم و ظرفیت گرمایی را بالاتر از تقاطع فرمول بندی کردند. آنها پیشبینی کردند که ارتباط بین ظرفیت گرمایی اجزا فوق بحرانی و ویسکوزیته نشات گرفته از قاونو توان در شرایط فوق بحرانی است.[۵] محدوده (مرز) مایع – گاز بحرانی به ما این اجازه را میدهد تا بین حالتها شبه مایع و شبه گاز در سیال فوق بحرانی، تمایز قائل شویم.
سیال فوق بحرانی در طبیعت[ویرایش]
گردش آب گرم[ویرایش]

گردش آب گرم در پوسته زمین هر گاه که سیال گرم بشود و شروع به تغییر حالت بکند، رخ میدهد. اینطور که پیداست، سیالها به دلایل مختلفی به شرایط بحرانی در آن وضعیت میرسند.
در پشته میانی اقیانوس، این جریان به وسیله یک چاه گرمایی که به " دود سیاه " معروف است، نمایان میشود. اینها چاههای بزگ دود سولفید و سولفات هستند که سیال را به دمای ۴۰۰ درجه سانتی گراد رساندهاند. سیال به شکل یک دود و ابری سیاه ظاهر میشود که این به سبب تهنشین شدن فلزات در سیال هست. اینطور که به نظر میآید در عمقهای بیشتر، بسیاری از این چاهها به شرایط فوق بحرانی میرسند. اما عمده آنها وقتی به سطح دریا میرسند به اندازه کافی سرد میشوند.[۶]
کاربردها[ویرایش]
استخراج[ویرایش]
نظر به ویسکوزیته پایین و قدرت نفوذ بالای سیالات فوق بحرانی در مقایسه با دیگر مایعات، استخراج به کمک آنها با سرعت بیشتری صورت میگیرد. ماده استخراج شده میتواند به راحتی با کم کردن فشار بازیافت شود، که به سیال فوق بحرانی این اجازه را میدهد تا به فاز گاز بازگردد و تبخیر شود که در اینصورت حجم حلال بسیار کم (حتی صفر) میشود. کربن دیاکسید یکی از پرکاربردترین حلالهای فوق بحرانی است که در مقیاس بالا برای جداسازی کافئین (کافئین زدایی) از دانههای کافه سبز[۷] و تولید اسانسها و تولیدات دارویی از گیاهان استفاده میشود.
تجزیه به کمک سیال فوق بحرانی[ویرایش]
از آب فوق بحرانی میتوان برای تجزیه زیست تودهها از طریق گازی سازی میتوان استفاده نمود.[۸]
این نوع از گازیسازی بیومس میتوانند در تولید سوختهای هیدروکربنی برای استفاده در دستگاههای احتراق یا تولید هیدروژن برای سلولهای سوختی نقش مهمی ایفا کنند.
خشکشویی[ویرایش]
کربن دیاکسید فوق بحرانی میتواند به جای پرکلرواتیلن یا هر حلال دیگهای که در خشکشویی استفاده میشود به کار برود. باید توجه داشت گاهی مواقع کربن دیاکسید فوق بحرانی با دکمهها درگیر میشود و وقتی که افت فشار پیدا میکند، باعث کنده شدن یا شکسته شدن دکمهها میشود. پاککنندههایی که توانایی حل شدن در کربن دیاکسید را دارند خود گواهی بر قدرت این محلول هستند.[۹]
اشباع و رنگرزی[ویرایش]
اشباع در اصل، عملیاتی است برعکس استخراج. اشباع بدین صورت است که یک ماده در سیال فوق بحرانی حل میشود، محلول از روی لایه جامد میگذرد و در نتیجه این لایه را حل میکند یا روی آن تهنشین میشود، اینطوری است که رنگرزی به راحتی روی فیبرهای پلیمر، همچون پلی استر که از رنگهای پراکنده (غیر یونیک) تشکیل شدهاست، صورت میپذیرد. ما در اینجا به نمونهای خاص از آن اشاره کردیم. دیاکسید کربن نیز در بسیار از پلیمرها حل میشود و آنها را به طرز قابل توجهی حجم میدهد (باعث ورم کردن آنها میشود) و آنها را پلاسیتکی میکند و از این رو باعث سرعت بخشیدن به فرایند انتشار میشود.
شکلگیری ذرات نانو و میکرو ذرات[ویرایش]
شکلگیری ذرات یک ماده با توزیع باریک و اندک یک فرایند در صنایع داروسازی و نیز سایر صنایع زیاد دیده میشود. وقتی سیالهای فوق بحرانی را بررسی میکنیم میبینیم که این سیالها به ما این امکان را میدهند تا از روشهای متعددی برای بالاتر رفتن از نقطه اشباع یک محلول از طریق رقیق کردن استفاده کنیم. البته این کار با کاهش فشارنیز انجام پذیر است و همچنین میتوان ترکیبی از روشها استفاده نماییم. این فرایند در سیالهای فوق بحرانی نسبت به سایر مایعات سریعتر رخ میدهند. این مسئله باعث میشود تا تجزیه اسپینودال یا هستهای رخ دهد. این مسئله در خلال فرایند رشد کریستالی رخ میدهد و همین باعث شود تا ذرات بسیار ریز بهطور منظم و یک اندازه شکل گیرند. سیالهای فوق بحرانی جدید نشان دادهاند که این توانایی را دارند تا ذرات را به به گستره ۵ الی ۲۰۰۰ نانومتر برسانند.[۱۰]
تولید کوکریستالهای دارویی[ویرایش]
سیالهای بحرانی، به عنوان وسیلهای جدید برای تولید فرمهای کریستالی بدیع استفاده میشود. این فرمها API(Active Pharmaceutical Ingredients) کوکریستالهای دارویی نام دارند. فناوری سیالهای بحرانی به ما این فرصت را میدهد تا به تولید موادی بپردازیم که از نسل تک مرحلهای (single-step generation) میباشند. این موارد با فناوریهای سنتی بعید است یا حتی امکانناپذیر است که بتوانند ساخته شوند. تولید کریستالهای جدید خالص و خشک شده (کمپلکسهای مولکولی کریستالی که شامل API و یک یا تعدادی بیشتر از خانواده همسایه میباشند که در شبکه کریستال میباشند) میتواند بر مبنای ویژگیهای خاص SCFs صورت پذیرد به این صورت که از دیگر ویژگیهای سیال فوق بحرانی استفاده شود. مثلاً در این میان باید قدرت حلالیت دیاکسید کربن فوق بحرانی هم چنین اثر ضد حلالیت و بهبود اتمیزه آن را در نظر آورد.[۱۱][۱۲]
خشک کردن فوق بحرانی[ویرایش]
خشک کردن فوق بحرانی، روشی برای جدا کردن حلال بدون اثرات تنش سطحی میباشد. هنگامی که یک مایع خشک میشود، تنش سطح به ساختارهای کوچک کشیده میشود این کار در قالب اعوجاج و انقباض رخ میدهد. در شرایط فوق بحرانی، تنش سطحی وجود ندارد و سیال فوق بحرانی میتواند بدون اعوجاج جدا شود. رنگآمیزی فوق بحرانی برای ساختن هواژل و خشک کردن مواد ظریف استفاده میشود. مانند نمونههای باستان شناختی یا نمونههای زیست شناختی برای میکروسکوپ الکترونی. این جاست که دیاکسید کربن به عنوان حلال فوق بحرانی در بعضی از فرایندهای تمیز کاری خشک مورد استفاده قرار میگیرد.
هیدرولیزهای آب فوق بحرانی[ویرایش]
هیدرولیزهای فوق بحرانی، روشی برای تبدیل همه زیست تودههای چند قندی و هم چنین لیگنین همراه آن ترکیبها مولکولی از طریق تماس برقرار کردن با آب به تنهایی در شرایط فوق بحرانی میباشد. آب فوق بحرانی به عنوان یک حلال عمل میکند، در واقع آب بحرانی یک تأمینکننده برای انرژی گرمایی مورد نیاز برای شکستن پیوندها، میباشد. همچنین عاملی است برای انتقال گرما و نیز منبعی برای اتمهای هیدروژن میباشد. اینگونه است که همه پلی ساکاریدها (چند قندها) به به قند ساده - در عرض یک لحظه یا کمتر - تبدیل میشوند.
سیال فوق بحرانی در تولید قدرت[ویرایش]
بهطور کلی اثربخشی یک موتور گرمایی به اختلاف دما موجود بین منبع و چگالنده ربط دارد (چرخه کارنو). برای بهبود اثربخشی ایستگاههای قدرت، دمای عملیات باید افزایش یابد. استفاده از آب به عنوان یک سیال در کار این امر را محقق میکند. این باعث میشود تا شرایط فوق بحرانی رخ دهد.[۱۳] اثربخشی میتواند از ۳۹ درصد به حدود ۴۵ درصد برسد برای عملیات فوق بحرانی برسد که البته میتوان با فناوریهای موجود آن را انجام داد.[۱۴] رآکتورهای آب فوق بحرانی(SCWRs) در سرتاسر جهان عملیاتی شدند و این نوید ارتقا کیفیت در سیستمها تولید قدرت سنتی را به ما میدهند.[۱۵]
تولید زیست دیزلها[ویرایش]
تغییر روغن سبزیجات زیست دیزل یک واکنش ترانس استریفیکاسیون میباشد. جاییکه تری گلیسیرید به متیل استر و گلیسیرین تبدیل میشود. این کار معمولاً با استفاده از متانول، مواد خورنده یا کاتالیزورهای اسید صورت می یپذیرد ولی میتواند از طریق متانول فوق بحرانی بدون استفاده از کاتالیزور هم صورت پذیرد. روش استفاده از متانول فوق بحرانی برای تولید زیست دیزل اولین بار بار توسط ساکا(Saka) و همکارانش مورد مطالعه قرار گرفت. این مسئله باعث میشود تا از آب داخل مواد غذایی استفاده کنیم و از روغن آن بهرهمند شود. نیازی نیست محصول نهایی برای خارج کردن کاتالیستها شسته شود.[۱۶]
افزایش بهرهوری در بازیافت نفت و جداسازی کربن دیاکسید و ذخیره آن[ویرایش]
دیاکسید کربن فوق بحرانی برای بازیابی نفت در حوزههای نفتی قدیمی (آخرین استخراجها از آنها صورت میگیرد) به کار میرود. دیاکسید کربن از سایر گازهای دودکش متمایز میباشد. فشرده میشود تا به وضعیت فوق بحرانی برسد و در ذخایر زمین شناختی تزریق میشود. برای مثال به میتوان برای افزایش استحکام آنها را به میدان نفتی تزیق کرد.
تبرید[ویرایش]
دیاکسید کربن فوق بحرانی همچون یک یخ ساز (سردکننده) مهم میباشد. اخیراً هم در پمپهای گرمایی مصرفی از محلولهای با کربن پایین استفاده میشود.[۱۷] این سیستم هادر حال توسعه میباشد و در آنها از پمپهای دیاکسید کربن فوق بحرانی استفاده شدهاست که در آسیا به خوبی برای آنها بازاریابی شدهاست. مثلاً میتوان به سیستمهای اکوکیوت(Eco cute) ژاپن که توسط ائتلاف تجاری تعدای از شرکتها، از جمله میتسوبیشی؛ ساخته شدهاست، اشاره کرد. در این سیستمها، آب مصرفی فشار بالا را توسط گرمای انتقال یافته از محیط به وسیله قدرت الکتریکی تقویت میکنند.[۱۸]
منابع[ویرایش]
- ↑ «What is a supercritical fluid?». Budapest University of Technology and Economics. بایگانیشده از اصلی در ۸ ژانویه ۲۰۱۶. دریافتشده در ۸ دسامبر ۲۰۱۷.
- ↑ «Supercritical Fluid Extraction, Density Considerations». ۲۰۰۷-۱۱-۲۰.
- ↑ Critical Processes Ltd (۲۰۰۷-۱۱-۲۰). «Calculation of Thermodynamic Properties of CO2 using Peng–Robinson equation of state». بایگانیشده از اصلی در ۳۱ مارس ۲۰۱۲. دریافتشده در ۸ دسامبر ۲۰۱۷.
- ↑ Trachenko؛ Brazhkin (۲۰۱۳). «Thermodynamic behaviour of supercritical matter». Nature Communications: ۲۳۳۱. doi:10.1038/ncomms3331. PMID 23949085. بیش از یک پارامتر
|نویسنده=و|نام خانوادگی=دادهشده است (کمک) - ↑ Brazhkin؛ Trachenko (۲۰۱۲). «The phonon theory of liquid thermodynamics». Scientific Reports. doi:10.1038/srep00421.
- ↑ Webber؛ Murton (۲۹ ژوئیه ۲۰۱۴). «Supercritical Venting and VMS Formation at the Beebe Hydrothermal Field, Cayman Spreading Centre». Goldschmidt Conference Abstracts 2014. Geochemical Society. بایگانیشده از اصلی در ۲۹ ژوئیه ۲۰۱۴. دریافتشده در ۸ دسامبر ۲۰۱۷.
- ↑ «The Naked Scientist Interviews». ۲۰۰۷-۱۱-۲۰.
- ↑ «Supercritical water gasification of biomas». 201-11-17. بایگانیشده از اصلی در ۲۳ مارس ۲۰۰۹. دریافتشده در ۸ دسامبر ۲۰۱۷. تاریخ وارد شده در
|تاریخ=را بررسی کنید (کمک) - ↑ «Science News Online». ۲۰۰۷-۱۱-۲۰. بایگانیشده از اصلی در ۹ مه ۲۰۱۳. دریافتشده در ۸ دسامبر ۲۰۱۷.
- ↑ «Formation of polymer particles with supercritical fluids: A review». The Journal of Supercritical Fluids. ۲۰۰۵. doi:j.supflu.2004.10.006/10.1016 مقدار
|doi=را بررسی کنید (کمک). - ↑ Rodrigues، M.A.؛ Velaga، S.P. «Formation of indomethacin–saccharin cocrystals using supercritical fluid technology». European Journal of Pharmaceutical Sciences: ۹–۱۷. doi:10.1016/j.ejps.2009.05.010.
- ↑ L. Padrela, M.A. Rodrigues, S.P. Velaga, H.A. Matos and E.G. Azevedo (2009). "Screening for pharmaceutical cocrystals using the supercritical fluid enhanced atomization process". Journal of Supercritical Fluids. article in press, corrected proof. doi:10.1016/j.supflu.2010.01.010
- ↑ Malhotra, Ashok and Satyakam,R, 2000,Influence of climatic parameters on optimal design of supercritical power plants,IECEC, Energy Conversion Engineering Conference, pp. 1053–1058,
- ↑ «Supercritical steam cycles for power generation applications» (PDF). ۲۰۰۷-۱۱-۲۰. بایگانیشده از اصلی (PDF) در دسامبر ۱۷, ۲۰۰۸.
- ↑ V. Dostal؛ M.J. Driscoll (۲۰۰۷-۱۱-۲۰). «A Supercritical Carbon Dioxide Cycle for Next Generation Nuclear Reactors» (PDF). MIT-ANP-TR-100. MIT-ANP-Series.
- ↑ «Continuous Production of Biodiesel via Transesterification from Vegetable Oils in Supercritical Methanol». Energy and Fuels: ۸۱۲–۸۱۷. doi:10.1021/ef050329b.
- ↑ «FAQs – Supercritical CO2 in heat pumps and other applications». بایگانیشده از اصلی در ۶ اکتبر ۲۰۰۷. دریافتشده در ۸ دسامبر ۲۰۱۷.
- ↑ Eco Cute hot water heat pumps in Japan بایگانیشده در مارس ۶, ۲۰۰۸ توسط Wayback Machine

