نمودار فازی

نمودار فازی (به انگلیسی: Phase diagram) نوعی نمودار است که برای نشان دادن شرایطی که (فشار، دما، حجم و …) فازهای ترمودینامیکی مختلف (جامد، مایع، گاز) روی میدهند یا در حالت تعادل با یکدیگر باقی میمانند، استفاده میشود.[۱]
استفاده از نمودارهای فازی یک روش متداول برای ثبت اطلاعات مربوط به فازهای مواد و استفاده از آنهاست. یک نمودار تعادل فازی، نمایش گرافیکی دادههاست که اطلاعات مهمی را در مورد ترکیبات تکی یا چند جزئی بهدست میدهد. دیاگرامهای فازی (Phase Diagram) نقشههای راهنمایی هستند که به کمک آنها تشکیل و پایداری فازهای مختلف بررسی میشوند. نمودارهای فازی در شرایط تعادلی بدست میآیند، بنابراین نمودارهای فازی ارتباط فازها را در شرایط تعادل نشان میدهند. تحت شرایط تعادل با گذشت زمان تغییری در فازها رخ نمیدهد.[۲]
توجه شود که شرایط تعادل با گرم یا سرد کردن بسیار کند و آرام امکانپذیر است.
فاز همان حالت ماده میباشد که در ویژگیهای فیزیکی با هم تفاوت دارند و با استفاده از تغییرات فیزیکی مانند چگالی و سطوح و زبری و انعکاس نور و الگوی پراش میتوان فازها را از هم شناسایی کرد. مخلوط چند گاز یک فاز را تشکیل میدهد، زیرا گازها بهطور کامل در یکدیگر حل میشوند اما مایعات و جامدات بهطور کامل در یکدیگر حل نمیشوند و مخلوط آنها چند فاز تشکیل میدهد.
قانون فازها
[ویرایش]قانون فازها به شکل زیر تعریف میشود:
F=C-P+2
در عبارت قانون فازها، F تعداد درجات آزادی، P تعداد فازهای در حال تعادل، و C تعداد اجزای سازندهٔ سیستم میباشد که یک جزء میتواند یک عنصر، یک ماده مرکب یا یک محلول جامد باشد.
اطلاعات موجود در نمودار فازی
[ویرایش]- دمای ذوب هر ترکیب خالص
- میزان کاهش دمای ذوب هنگام ترکیب دو یا چند ماده
- وجود و میزان حلالیت در محلولهای جامد
- اثر دما بر روی میزان حلالیت
- دمای استحالههای پلیمورفیک
- وجود مایعات (مذابهایی) که در یکدیگر حل نمیشوند (ناحیهٔ عدم امتزاج)
نمودارهای تک جزئی (تکی)
[ویرایش]این نمودارها پایداری فازی مواد خالص را نشان میدهند. متغیرهای موجود دراین نمودارها: دما، فشار و حجم هستند. پس ۳ متغیر در این نمودارها وجود دارد. یک نمونه از این نمودارها در شکل ۱ نشان داده شدهاست.

با تصویر کردن این نمودار سهبعدی بر روی یکی از صفحات مختصات دکارتی، میتوان یک نمودار صفحهای بهدست آورد. گرچه در این حالت مقداری از اطلاعات موجود در نمودار از دست میرود، ولی بررسی آن بر روی کاغذ سادهتر میشود؛ که معمولاً از نمودار P-V یا P-T به این منظور استفاده میشود.
شکل شماره ۲ نحوهٔ تصویر کردن نمودار فازی PVT را بر روی صفحهٔ PT نشان میدهد.

پیکان موجود در نمودار فضایی شکل ۲ جهت دید ناظر را نشان میدهد.[۳]
نمودارها
[ویرایش]در نمودارهای فازی دما بر حسب سانتیگراد یا فارنهایت روی محور عمودی و ترکیب شیمیایی بر حسب درصد وزنی روی محور افقی نشان داده میشود. در نمودارهای فازی، ترکیب شیمیایی بر حسب درصد وزنی روی محور افقی از صفر تا صد درصد نشان داده میشود. در علم مواد نمودارهای مهمی در رابطه با ترکیبهای فازی مختلفی وجود دارد که در زیر به آنها اشاره خواهیم کرد.[۴]
اجزایی که در حالت مایع کاملاً در هم محلولند
[ویرایش]در حالت جامد کاملاً محلولند
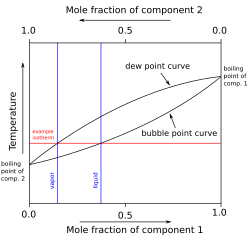
[ویرایش]در این حالت دو فلز در حالت جامد کاملاً در هم حل میشوند. نمودار فازی در این حالت به شکل زیر میباشد.
نکات مهم در رابطه با این نمودار عبارتند از:
- خط گداز
- خط انجماد
- محدوده مذاب، محلول جامد و ترکیب این دو
- نقطه انجماد و ذوب
در حالت جامد کاملاً نامحلولند (یوتکتیک)
[ویرایش]در این حالت دو فلز در حالت مذاب کاملاً در هم محلول هستند ولی در حالت جامد کاملاً نامحلول هستند. حالت نامحلول را اینگونه فرض میکنیم که حلالیت خیلی کم است. نمونهای از این حلالیت در شکل زیر که مربوط به بیسموت-کادمیوم و سیلیسیم-آلومینیوم است در شکل زیر نشان داده شدهاست.
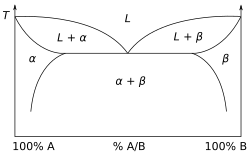
در نقطه یوتکتیک، مذاب تبدیل به دو جامد میشود یعنی فاز L تبدیل به S1,S2 میشود. به آلیاژ سمت چپ نقطه یوتکتیک، هیپو یوتکتیک و به آلیاژ سمت راست ان آلیاژ هایپر یوتکتیک میگویند.
در حالت جامد مقداری محلولند (یوتکتیک)
[ویرایش]در این حالت دو فلز در حالت مذاب کاملاً محلول بوده و در حالت جامد بهطور مختصر در یکدیگر محلول هستند. توجه شود که سیستم یوتکتیک فوق در میان سیستمها حداکثر استحکام را دارد.
یک فاز میانی با ذوب متجانس تشکیل میدهند
[ویرایش]هنگامی که فازی در شرایط هم دما به فاز دیگری تبدیل شود و هیچگونه تغییر شیمیایی در ترکیب رخ ندهد گفته میشود که تغییر فاز متجانس یا تحول متجانس رخ دادهاست. تمام فلزات خالص به صورت متجانس منجمد میشوند.
واکنش پریتکتیک
[ویرایش]در واکنش پریتکتیک به هنگام سرد کردن یک مذاب و یک جامد بهطور همزمان واکنش میدهند تا جامد جدیدی بهدست آید. این واکنش یک واکنش دما ثابت بودهاست و آلیاژها دو فازی هستند.
اجزایی که در حالت مذاب مقداری محلولند (منوتکتیک)
[ویرایش]در این حالت دو فاز مذاب که تا حدودی در هم حل میشوند و تشکیل یک مذاب جدید و یک جامد میدهد.
اجزایی که در حالت مذاب و جامد نامحلولند
[ویرایش]این قسمت کاملکننده بررسی فازهای اساسی یا نمودارهای تعادلی است که شامل حالتهای مذاب و جامدند.
تبدیلها و تحولها در حالت جامد
[ویرایش]تغییرات تعادلی و واکنشهای متعددی وجود دارند که همگی در حالت جامد رخ میدهند. این تحولها شمال چهار نوع جداگانه میباشند که در زیر به آنها اشاره میکنیم:
تغییرات آلوتروپیک
[ویرایش]دربارهٔ فلزات و ساختارهای بلوری برخی فلزها وابسته به دما ممکن است که بیش از یک ساختار بلوری داشته باشند. این خاصیت را آلوتروپی میگویند. تحول آلوتروپیک را به صورت نقطه یا نقاطی بر خط عمودی مشخص میکنند. آهن و قلع و منگنز از این دسته فلزها میباشند.
منظم و نامنظم
[ویرایش]در هنگام تشکیل یک محلول جامد اگر آهسته سرد شوند، اتمهای حل شده به محلهای معینی در شبکه حرکت میکنند، این ساختار را محلول جامد منظم گویند ولی اگر محلول جامد فرصت سرد شدن نداشته باشد اتمهای حل شونده به صورت اتفاقی در ساختار شبکه حلال پخش میشوند در این صورت میگویند آلیاژ در شرایط نامنظم قرار دارد.
واکنش یوتکتویید
[ویرایش]این واکنش شباهت زیادی به واکنش یوتکتیک دارد با این تفاوت که در این واکنش مذاب حضور ندارد و واکنش در حالت جامد میباشد. در این واکنش یک جامد به دو جامد تبدیل میشود.
واکنش پریتکتویید
[ویرایش]واکنش پریتکتویید از ترکیب دو جامد و تشکیل دو جامد دیگر حاصل میشود. این تحول از جمله تحولات در حالت جامد میباشد.
منابع
[ویرایش]- ↑ "Phase diagram". Wikipedia (به انگلیسی). 2019-12-30.
- ↑ https://en.wikipedia.org/wiki/Phase_diagram
- ↑ David, Carl. "Verwiebe's "3-D" Ice phase diagram reworked". Jump up ^
- ↑ http://chem.libretexts.org/Core/Physical_and_Theoretical_Chemistry/Physical_Properties_of_Matter/States_of_Matter/Phase_Transitions/Phase_Diagrams
- مضطرزاده، فتحالله - واهاک مارقوسیان- صلاحی، اسماعیل، درآمدی بر تعادل فازی در سرامیکها، انتشارات دانشگاه علم و صنعت ایران، ۱۳۷۸.
- Web applet: 3D Phase Diagrams for Water, Carbon Dioxide and Ammonia. Described in Glasser, Leslie; Herráez, Angel; Hanson, Robert M. (2009). "Interactive 3D Phase Diagrams Using Jmol". Journal of Chemical Education. 86 (5): 566. doi:10.1021/ed086p566.
Jump up ^
- Chandrasekhar, Sivaramakrishna (1992). Liquid Crystals (2nd ed.). Cambridge University Press. pp. 27–29, 356. ISBN 0-521-41747-3
- http://www.tulane.edu/~sanelson/eens211/2compphasdiag.html
منابعی برای مطالعهٔ بیشتر
[ویرایش]- عباس هنربخش رئوف، حجتالله شهسواری، ابوالفضل زارع «مبانی متالورژی فیزیکی و علم مواد» نمودارهای فازی دوتایی و سه تایی، جهاد دانشگاهی صنعتی امیرکبیر، ۱۳۸۵
- صادقی، سید محمد علی، تعادل فازها در محیط حلال آب، نشر دانشگاه هرمزگان، ۱۳۷۸.
قوانین و مفاهیم مرتبط
[ویرایش]- ترمودینامیک
- دمای بحرانی
- نقطهٔ سهگانه
- سالیدوس و لیکوییدوس
- قانون فازی گیبس (قانون اهرم)
- قانون لوشاتلیه (استوالد)
- معادله کلازیوس-کلاپیرون
- درصد اتمی
- درصد وزنی
- درجه آزادی
- تعادل
- آلوتروپی
- مغزهبندی (هسته بندی)
- استحاله فازی
