سولفات پتاسیم
| سولفات پتاسیم | |
|---|---|
 Arcanite
| |
| |
دیگر نامها Potassium sulphate | |
| شناساگرها | |
| شماره ثبت سیایاس | 7778-80-5 |
| پابکم | 24507 |
| کماسپایدر | 22915 |
| UNII | 1K573LC5TV |
| KEGG | D01726 |
| ChEBI | CHEBI:32036 |
| ChEMBL | CHEMBL1201793 |
| شمارهٔ آرتیئیسیاس | TT5900000 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
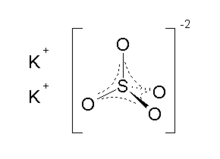
| فرمول مولکولی | K2SO4 |
| جرم مولی | 174.259 g/mol |
| شکل ظاهری | White solid |
| بوی | odorless |
| چگالی | 2.66 g/cm3[۱] |
| دمای ذوب | ۱٬۰۶۹ درجه سلسیوس (۱٬۹۵۶ درجه فارنهایت؛ ۱٬۳۴۲ کلوین) |
| دمای جوش | ۱٬۶۸۹ درجه سلسیوس (۳٬۰۷۲ درجه فارنهایت؛ ۱٬۹۶۲ کلوین) |
| انحلالپذیری در آب | 111 g/L (20 °C) 120 g/L (25 °C) 240 g/L (100 °C) |
| انحلالپذیری | slightly soluble in گلیسیرین insoluble in استون الکل کربن دیسولفید |
| اسیدی (pKa) | ~7 |
| ضریب شکست (nD) | 1.495 |
| ساختار | |
| ساختار بلوری | دستگاه بلوری راستلوزی |
| خطرات | |
| MSDS | External MSDS |
| شاخص ئییو | Not listed |
| کدهای ایمنی | R۲۲ |
| شمارههای نگهداری | S۳۶ |
| خطرات اصلی | Irritant |
| نقطه اشتعال | |
| LD50 | 6600 mg/kg |
| ترکیبات مرتبط | |
| دیگر آنیونها | Potassium selenate Potassium tellurate |
| دیگر کاتیونها | سولفات لیتیم سدیم سولفات Rubidium sulfate سزیم سولفات |
| ترکیبات مرتبط | بیسولفات پتاسیم پتاسیم سولفیت پتاسیم بیسولفیت پتاسیم پرسولفات |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
سولفات پتاسیم (به انگلیسی: Potassium sulfate) با فرمول شیمیایی K۲SO۴ یک ترکیب شیمیایی با شناسه پابکم ۲۴۵۰۷ است. که جرم مولی آن 174.259 g/mol میباشد. شکل ظاهری این ترکیب، جامد سفید است.
جستارهای وابسته[ویرایش]
منابع[ویرایش]
- ↑ Patnaik, Pradyot (2002). Handbook of Inorganic Chemicals. McGraw-Hill. ISBN 0070494398.
- «IUPAC GOLD BOOK». دریافتشده در ۱۸ مارس ۲۰۱۲.
