انرژی سطح
این مقاله دقیق، کامل و صحیح ترجمه نشده و نیازمند ترجمه به فارسی است. کل یا بخشی از این مقاله به زبانی بهجز زبان فارسی نوشته شدهاست. اگر مقصود ارائهٔ مقاله برای مخاطبان آن زبان است، باید در نسخهای از ویکیپدیا به همان زبان نوشته شود (فهرست ویکیپدیاها را ببینید). در غیر این صورت، خواهشمند است ترجمهٔ این مقاله را با توجه به متن اصلی و با رعایت سیاست ویرایش، دستور خط فارسی و برابر سازی به زبان فارسی بهبود دهید و سپس این الگو را از بالای صفحه بردارید. همچنین برای بحثهای مرتبط، مدخل این مقاله در فهرست صفحههای نیازمند ترجمه به فارسی را ببینید. اگر این مقاله به زبان فارسی بازنویسی نشود، تا دو هفتهٔ دیگر نامزد حذف میشود و/یا به نسخهٔ زبانی مرتبط ویکیپدیا منتقل خواهد شد. اگر شما اخیراً این مقاله را بهعنوان صفحهٔ نیازمند ترجمه برچسب زدهاید، لطفاً عبارت {{جا:هبک-ترجمه به فارسی|1=انرژی سطح}} ~~~~را نیز در صفحهٔ بحث نگارنده قرار دهید. |
این مقاله نیازمند تمیزکاری است. لطفاً تا جای امکان آنرا از نظر املا، انشا، چیدمان و درستی بهتر کنید، سپس این برچسب را بردارید. محتویات این مقاله ممکن است غیر قابل اعتماد و نادرست یا جانبدارانه باشد یا قوانین حقوق پدیدآورندگان را نقض کرده باشد. |
انرژی آزاد سطحی یا انرژی سطح کمیتی است که اختلال در پیوندهای بین مولکولی هنگام ایجاد یک سطح جدید را توصیف میکند. در فیزیک جامدات، مولکولهای روی سطح انرژی بیشتری در مقایسه با مولکولهای موجود در بخش عمده (حجم) مواد دارند، در غیر این صورت نیروی محرکه ای در حجم مواد ایجاد خواهد شد تا به سطح تبدیل شوند، که در ادامه بخش عمده ای از مواد را از بین میبرد (نگاه کنید به تصعید). بنابراین ممکن است انرژی سطح به عنوان انرژی اضافی در سطح یک ماده نسبت به حجم (عمده) ماده تعریف شود یا این که کار مورد نیاز برای ساختن یک سطح جدید از یک سطح خاص (قدیمی) تعریف شود. راه دیگر برای درک و شهود انرژی سطح، بررسی ارتباط آن با کار مورد نیاز برای برش یک نمونه حجم و ایجاد دو سطح جدید است.
برش یک جسم جامد به قطعات کوچکتر، پیوندهای سطحی آن را ازبین میبرد و بنابراین انرژی آزاد را افزایش میدهد. اگر برش به صورت برگشتپذیر انجام شود، در نتیجه آن بقای انرژی به معنای آن است که انرژی حاصل از فرایند برش برابر با انرژی درونی در دو سطح جدید ایجاد شده خواهد بود؛ بنابراین، مقدار انرژی سطح ماده میتواند حاصل از پیوستگی (چسبندگی) بین مواد باشد. در عمل، همه این موارد برای حالتی است که جسم در خلا بریده شده باشد. سطوح اغلب شکل خود را به دور از مدل ساده «پیوند شکسته» که در بالا ذکر شد تغییر میدهند. به نظر میرسد که آنها مناطق بسیار پویا (دینامیکی) هستند که به راحتی و سریع ساختار بندی مجدد یا واکنش نشان میدهند، به طوری که انرژی اغلب توسط فرایندهای منفعل یا جذب کاهش مییابد.

محاسبه انرژی سطح[ویرایش]
اندازه گیری انرژی سطح با اندازه گیری زاویه تماس
متداول ترین روش اندازه گیری انرژی سطح از طریق آزمایش های زاویه تماس است.[۱] در این روش، زاویه تماس سطح با چندین مایع، معمولاً آب و دیودودمتان اندازهگیری میشود. با توجه به نتایج زاویه تماس و دانستن کشش سطحی مایعات، میتوان انرژی سطح را محاسبه کرد. در عمل، این تجزیه و تحلیل بهطور خودکار توسط یک زاویه تماس سنج انجام میشود.[۲]
چندین مدل مختلف برای محاسبه انرژی سطح بر اساس خواندن و روش اندازهگیری زاویه تماس وجود دارد.[۳] متداول ترین روش OWRK است که نیاز به استفاده از دو لیکویید پروب دارد و در نهایت انرژی کل سطح را میدهد و آن را به اجزای قطبی و پراکندگی تقسیم میکند.
وش زاویه تماس با توجه به سادگی، کاربرد در طیف گستردهای از سطوح و سرعت، روش استاندارد اندازهگیری انرژی سطح محسوب میشود. این نوع اندازهگیری میتواند کاملاً خودکار و استاندارد شده باشد.[۴]
اندازه گیری انرژی سطح جامد - روش های دیگر[ویرایش]
انرژی سطح یک مایع ممکن است با کشش یک غشای مایع (که باعث افزایش سطح و در نتیجه انرژی سطح میشود) اندازهگیری شود. در این حالت، برای افزایش سطح یک توده مایع توسط یک مقدار، δA، یک مقدار کار، γδA، لازم است (در حالی که γ چگالی انرژی سطح مایع است). با این وجود، از چنین روشی نمیتوان برای اندازهگیری انرژی سطح جامد استفاده کرد زیرا کشش غشای جامد علاوه بر افزایش انرژی سطح، باعث افزایش انرژی الاستیک در حجم ماده میشود.
انرژی سطح یک جامد معمولاً در دماهای بالا اندازهگیری میشود. در چنین دماهایی خزش جامد و حتی موقعیت سطح تغییر میکند، اما با این حال حجم تقریباً ثابت است. اگر γ چگالی انرژی سطح میله استوانه ای شکل با شعاع و طول در دمای بالا و یک تنش تک محوره ثابت باشد درنهایت در معادله، تغییرات کل انرژی آزاد هلملولتز حذف میشوند و ما خواهیم داشت:
در حالیکه که انرژی آزاد Helmholtz و سطح میله است:
همچنین ، از آنجا که حجم ( ) میله ثابت است ، تغییر ( ) حجم صفر است ، یعنی:
بنابراین ، چگالی انرژی سطح می تواند به صورت زیر بیان شود:
چگالی انرژی سطح جامد را میتوان با جایگذاری ، و در معادله محاسبه کرد.
این روش تنها در صورتی معتبر است که جامد ایزوتروپیک باشد، به این معنی که انرژی سطح برای کلیه جهتهای کریستالوگرافی (بلورنگاری) یکسان است. در حالی که این تنها برای مواد جامد آمورف (شیشه ای) و مایعات صادق است، ایزوتروپی تقریب خوبی برای بسیاری از مواد دیگر است. بهطور خاص، اگر نمونه چند ضلعی باشد (بیشتر فلزات) یا توسط پودر (بیشتر سرامیکها) ساخته شدهاست، این یک تقریب خوب است.
محاسبه انرژی سطح جامد تغییر شکل یافته[ویرایش]
در تغییر شکل مواد جامد، میتوان انرژی سطح را به عنوان «انرژی مورد نیاز برای ایجاد یک واحد سطح» تعریف کرد. در واقع انرژی سطح تابعی است از تفاوت بین کل انرژیهای سیستم قبل و بعد از تغییر شکل:
محاسبه انرژی سطح از اصول اولیه (برای مثال، تئوری عملکردی چگالی) یک روش جایگزین برای اندازهگیری عملی است. انرژی سطح از متغیرهای زیر محاسبه میشود: عرض باند d، تعداد الکترونهای ظرفیتی لایه d، و عدد هم آرایی (کوئوردیناسیون) اتمها در سطح و بخش عمده جامد.[۵]
محاسبه انرژی تشکیل سطح جامد کریستالی[ویرایش]
در تئوری چگالی تابعی ، انرژی سطح را می توان از عبارت زیر محاسبه کرد:
درحالیکه که انرژی لایه سطح با استفاده از تئوری چگالی تابعی است. تعداد اتمها در لایه سطح است. انرژی عمده ای برای هر اتم است. مساحت سطح است برای یک لایه دو سطح داریم و آنها از یک نوع هستند که با عدد ۲ در مخرج خود را بروز میدهند. برای تضمین این امر، باید دال (ورقه / لایه) را با دقت ایجاد کنیم تا مطمئن شویم که سطوح بالا و پایین از یک نوع هستند.
انرژی سطحی[ویرایش]
حضور یک رابط ، کلیه پارامترهای ترمودینامیکی یک سیستم را تحت تأثیر قرار می دهد. دو مدل وجود دارد که معمولاً برای نشان دادن پدیده های سطحی استفاده می شود ، که عبارتند از مدل رابط ایدهآل گیبس و مدل گوگنهایم است. به منظور نشان دادن ترمودینامیک یک سیستم میان سطحی با استفاده از مدل گیبس ، این سیستم را می توان به سه قسمت تقسیم کرد: دو مایع غیرقابل برگشت با حجم و و یک لایه مرزی بینهایت باریک معروف به صفحه تقسیم گیبس (σ) که این دو حجم را از هم جدا می کند.

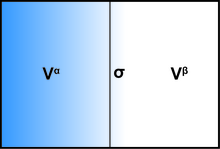
حجم کل سیستم (مدل گیبس):
تمام مقادیر گسترده سیستم را می توان به عنوان مجموعه ای از سه مؤلفه نوشت: فاز حجمی a ، فاز حجمی b ، و رابط سیگما. برخی از مثال ها شامل انرژی داخلی ( ) تعداد مولکول های ماده د ام ( ) و آنتروپی ( )هستند:
در حالی که این کمیت ها می توانند بین هر مؤلفه ای متفاوت باشند ، مقدار کل درون سیستم ثابت است. در رابط ، این مقادیر ممکن است که با فازها متفاوت باشد. غلظت مولکولهای موجود در رابط را می توان چنین تعریف کرد:
این درحالیست که و غلظت ماده را به ترتیب در فاز های حجمی و نشان میدهند. میتوان تعریف جدیدی به اسم ارایه داد که به ما امکان می دهد تعداد مولکول ها در واحد سطح را توصیف کنیم:
تکنیک های تغییر انرژی سطح[ویرایش]
متداول ترین پروتکل های اصلاح سطح عبارتند از: فعال سازی پلاسما ، عملیات شیمیایی مرطوب ، از جمله پیوند و روکش لایه های نازک.[۶][۷][۸]
تکنیک های زیادی برای تقویت ترشوندگی قابل استفاده است. از عملیات سطحی، مانند اصلاح کرونا ،[۹] اصلاح پلاسمایی و اسید اچینگ،[۱۰] می توان برای افزایش انرژی سطح بهره برد. برای کاهش انرژی سطح نیز می توان افزودنی هایی به مایع اضافه کرد. این روش اغلب در فرمولاسیون رنگ بکار می رود تا اطمینان حاصل شود که به طور مساوی روی یک سطح پخش خواهند شد.[۱۱]
جدول مقادیر انرژی سطحی[ویرایش]
| مواد | گرایش | انرژی سطح (mJ / m 2 ) |
|---|---|---|
| Polytetrafluoroethylene (PTFE) | [۱۲]19 | |
| شیشه | [۱۳]83.4 | |
| گچ | [۱۴]370 | |
| مس | [۱۵]1650 | |
| اکسید منیزیم | (100) صفحه | [۱۶]1200 |
| فلوراید کلسیم | (111) صفحه | [۱۶]450 |
| لیتیوم فلوراید | (100) صفحه | [۱۶]340 |
| کربنات کلسیم | (1010) صفحه | [۱۶]230 |
| سدیم کلرید | (100) صفحه | [۱۷]300 |
| سدیم کلرید | (110) صفحه | [۱۸]400 |
| کلرید پتاسیم | (100) صفحه | [۱۷]110 |
| فلوراید باریم | (111) صفحه | [۱۶]280 |
| سیلیکون | (111) صفحه | [۱۶]1240 |
جستارهای وابسته[ویرایش]
پیوند به بیرون[ویرایش]
منابع[ویرایش]
- ↑ Marshall, Sally J.; Bayne, Stephen C.; Baier, Robert; Tomsia, Antoni P.; Marshall, Grayson W. (2010-02-01). "A review of adhesion science". Dental Materials. 26 (2): e11–e16. doi:10.1016/j.dental.2009.11.157. ISSN 0109-5641.
- ↑ Laurén، Susanna. «How To Measure Surface Free Energy?». blog.biolinscientific.com (به انگلیسی). دریافتشده در ۲۰۲۰-۰۱-۰۵.
- ↑ Scientific, Biolin. "Surface Free Energy | Measurements". www.biolinscientific.com (به انگلیسی). Retrieved 2020-01-05.
- ↑ 14:00-17:00. "ISO 19403-2:2017". ISO (به انگلیسی). Retrieved 2020-01-05.
{{cite web}}: CS1 maint: numeric names: فهرست نویسندگان (link) - ↑ The Chemical Physics of Solid Surfaces (به انگلیسی). Vol. 10 جلد. به کوشش D.P. Woodruff. Elsevier. 2002.
{{cite book}}: نگهداری CS1: سایر موارد (link) - ↑ Becker, Holger; Gärtner, Claudia (2008-01-01). "Polymer microfabrication technologies for microfluidic systems". Analytical and Bioanalytical Chemistry (به انگلیسی). 390 (1): 89–111. doi:10.1007/s00216-007-1692-2. ISSN 1618-2650.
- ↑ Mansky, P.; Liu, Y.; Huang, E.; Russell, T. P.; Hawker, C. (1997-03-07). "Controlling Polymer-Surface Interactions with Random Copolymer Brushes". Science (به انگلیسی). 275 (5305): 1458–1460. doi:10.1126/science.275.5305.1458. ISSN 0036-8075.
- ↑ Rastogi, Abhinav; Paik, Marvin Y.; Tanaka, Manabu; Ober, Christopher K. (2010-02-23). "Direct Patterning of Intrinsically Electron Beam Sensitive Polymer Brushes". ACS Nano. 4 (2): 771–780. doi:10.1021/nn901344u. ISSN 1936-0851.
- ↑ Sakata, Isao; Morita, Mitsuhiro; Tsuruta, Natsuhi; Morita, Kenzo (1993). "Activation of wood surface by corona treatment to improve adhesive bonding". Journal of Applied Polymer Science (به انگلیسی). 49 (7): 1251–1258. doi:10.1002/app.1993.070490714. ISSN 1097-4628.
- ↑ Rosales, J.I.; Marshall, G.W.; Marshall, S.J.; Watanabe, L.G.; Toledano, M.; Cabrerizo, M.A.; Osorio, R. (1999-09). "Acid-etching and Hydration Influence on Dentin Roughness and Wettability". Journal of Dental Research (به انگلیسی). 78 (9): 1554–1559. doi:10.1177/00220345990780091001. ISSN 0022-0345.
{{cite journal}}: Check date values in:|date=(help) - ↑ Khan, Heena; Fell, John T; Macleod, Graeme S (2001-10-04). "The influence of additives on the spreading coefficient and adhesion of a film coating formulation to a model tablet surface". International Journal of Pharmaceutics. 227 (1): 113–119. doi:10.1016/S0378-5173(01)00789-X. ISSN 0378-5173.
- ↑ Adhesion & Adhesives - Science & Technology (به انگلیسی). به کوشش Kinloch, A.J.. 1987.
{{cite book}}: نگهداری CS1: سایر موارد (link) - ↑ Rhee, S. K. (1977-04-01). "Surface energies of silicate glasses calculated from their wettability data". Journal of Materials Science (به انگلیسی). 12 (4): 823–824. doi:10.1007/BF00548176. ISSN 1573-4803.
- ↑ Dundon, Merle L.; Mack, Edward (1923-11-01). "THE SOLUBILITY AND SURFACE ENERGY OF CALCIUM SULFATE". Journal of the American Chemical Society. 45 (11): 2479–2485. doi:10.1021/ja01664a001. ISSN 0002-7863.
- ↑ Udin, Harry (1951-01-01). "Grain Boundary Effect in Surface Tension Measurement". JOM (به انگلیسی). 3 (1): 63–63. doi:10.1007/BF03398958. ISSN 1543-1851.
- ↑ ۱۶٫۰ ۱۶٫۱ ۱۶٫۲ ۱۶٫۳ ۱۶٫۴ ۱۶٫۵ Gilman, John J. (1960-12-01). "Direct Measurements of the Surface Energies of Crystals". Journal of Applied Physics. 31 (12): 2208–2218. doi:10.1063/1.1735524. ISSN 0021-8979.
- ↑ ۱۷٫۰ ۱۷٫۱ Physics and Chemistry of Interfaces (به انگلیسی). به کوشش Butt, Hans-Jürgen, Kh Graf, and Michael Kappl. 2006.
{{cite book}}: نگهداری CS1: سایر موارد (link) - ↑ Lipsett, S. G.; Johnson, F. M. G.; Maass, O. (1927-04-01). "THE SURFACE ENERGY AND THE HEAT OF SOLUTION OF SOLID SODIUM CHLORIDE. I". Journal of the American Chemical Society. 49 (4): 925–943. doi:10.1021/ja01403a005. ISSN 0002-7863.
































