هیپوفیز پیشین: تفاوت میان نسخهها
ایجاد شده بهواسطهٔ ترجمهٔ صفحهٔ «Anterior pituitary» |
(بدون تفاوت)
|
نسخهٔ ۱۸ سپتامبر ۲۰۲۲، ساعت ۱۷:۰۳
| Anterior pituitary gland | |
|---|---|
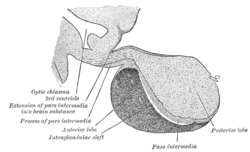 Median sagittal through the hypophysis of an adult monkey. Semidiagrammatic. | |
| جزئیات | |
| ساخته از | oral mucosa (Rathke's pouch) |
| سرخرگها | superior hypophyseal |
| سیاهرگها | hypophyseal |
| شناسهها | |
| لاتین | lobus anterior hypophysis |
| MeSH | D010903 |
| نورونیمز | 407 |
| شناسه نورولکس | birnlex_1581 |
| TA98 | A11.1.00.002 |
| TA2 | 3855 |
| FMA | 74627 |
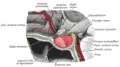
اندام اصلی سیستم غدد درون ریز ، هیپوفیز پیشین یا هیپوفیز قدامی که آدنوهیپوفیز نیز نامیده می شود لوب غددی و قدامی است که همراه با لوب خلفی ( هیپوفیز خلفی یا نوروهیپوفیز) غده هیپوفیز را تشکیل می دهد. هیپوفیز قدامی چندین فرآیند فیزیولوژیکی از جمله استرس ، رشد ، تولیدمثل و شیردهی را تنظیم می کند. عملکرد صحیح هیپوفیز قدامی و اندام های هدف و تحت تأثیر آن، اغلب از طریق آزمایش های خونی که سطح هورمون ها را اندازه گیری می کند مشخص می شود.
ساختار

غده هیپوفیز در یک محفظه ی استخوانی محافظ به نام sella turcica قرار دارد. از سه لوب تشکیل شده است: لوب قدامی، میانی و خلفی. در بسیاری از جانوران، این لوب ها متمایز هستند. با اینحال، در انسان، لوب میانی فقط چند لایه ی سلولی ضخیم و نامشخص است. در نتیجه، اغلب بخشی از هیپوفیز قدامی در نظر گرفته می شود. در همه ی جانوران، هیپوفیز قدامی گوشتی و غدهای از ترکیب عصبی هیپوفیز خلفی متمایز است.[نیازمند منبع]
عملکرد
هیپوفیز قدامی شامل پنج نوع سلول غدد درونریز است و آنها توسط هورمون هایی که ترشح می کنند نامگذاری شده اند: سوماتوتروپ (GH). لاکتوتروپ (PRL)؛ گنادوتروپ ها (LH و FSH)؛ کورتیکوتروپ ها (ACTH) و تیروتروپ ها (TSH). [۱] همچنین حاوی سلولهای فولیکولوستلیت غیر غدد درونریز است که تصور میشود جمعیت سلولهای غدد درونریز را تحریک و پشتیبانی میکنند.
هورمونهایی که از هیپوفیز قدامی ترشح میشوند، یا مستقیماً رشد را تحت تأثیر قرار می دهند یا بهصورت هیپرپلازی یا هیپرتروفی در بافت هدف و مورد تحریک. مکانیسم این هورمون ها برای اثر مستقیم بر روی بافتهای هدف یا سایر غدد درونریز برای آزادسازی هورمونها، ایجاد پاسخهای فیزیولوژیکی آبشاری متعدد است. [۲]
| هورمون | نامهای دیگر | نماد(ها) | ساختار | سلول های ترشحی | رنگآمیزی | هدف | اثر | |
|---|---|---|---|---|---|---|---|---|
| هورمون آدرنوکورتیکوتروپیک | کورتیکوتروپین | ACTH | پلی پپتید | کورتیکوتروف ها | بازوفیل | غده فوق کلیوی | ترشح گلوکوکورتیکوئید ، مینرالوکورتیکوئید و آندروژن | |
| هورمون محرک تیروئید | تیروتروپین | TSH | گلیکوپروتئین | تیروتروف ها | بازوفیل | غده تیروئید | ترشح هورمون های تیروئید | |
| هورمون محرک فولیکول | - | FSH | گلیکوپروتئین | گنادوتروف ها | بازوفیل | غدد جنسی | رشد دستگاه تناسلی | |
| هورمون رنگدانه ساز | لوتروپین | LH، ICSH | گلیکوپروتئین | گنادوتروف ها | بازوفیل | غدد جنسی | تولید هورمون جنسی | |
| هورمون رشد | سوماتوتروپین | GH، STH | پلی پپتید | سوماتوتروف ها | اسیدوفیل | کبد ، بافت چربی | باعث رشد می شود؛ متابولیسم لیپید و کربوهیدرات | |
| پرولاکتین | لاکتوتروپین | PRL | پلی پپتید | لاکتوتروف ها | اسیدوفیل | تخمدان ها، غدد پستانی ، بیضه ها ، پروستات | ترشح استروژن / پروژسترون ; شیردهی ؛ اسپرم زایی ; هایپرپلازی خوشخیم پروستات | ترشح TSH و ACTH |
اهمیت بالینی
افزایش فعالیت
پرکاری هیپوفیز است که در آن هیپوفیز مقادیر زیادی هورمون ترشح می کند. این ترشح بیش از حد اغلب منجر به تشکیل آدنوم هیپوفیز (تومور) می شود. بهطور عمده سه نوع تومور هیپوفیز قدامی و اختلالات مرتبط با آن ها وجود دارد. به عنوان مثال، آکرومگالی ناشی از ترشح بیش از حد هورمون رشد (GH) است که اغلب توسط آدنوم هیپوفیز آزاد می شود. این اختلال میتواند باعث تغییر شکل و احتمالاً مرگ شود [۵] و میتواند منجر به غولپیکری شود، یک اختلال هورمونی که در «غولها» مانند آندره غول نشان بروز یافته است که پیش از بسته شدن صفحات اپی فیزیال استخوانها در بلوغ اتفاق میافتد.۶ شایع ترین نوع تومور هیپوفیز پرولاکتینوما است که پرولاکتین را بیش از حد ترشح می کند. [۶] نوع سوم آدنوم هیپوفیز ACTH اضافی ترشح می کند که به نوبه ی خود باعث ترشح بیش از حد کورتیزول می شود و عامل بیماری کوشینگ است .۶ [۷]
کاهش فعالیت
کم کاری هیپوفیز با کاهش ترشح هورمون های آزاد شده توسط هیپوفیز قدامی تعریف می شود. برای مثال، کاهش ترشح هورمون رشد پیش از بلوغ می تواند علت کوتولگی باشد. علاوه بر این، نارسایی ثانویه آدرنال می تواند ناشی از کمبود ترشح ACTH باشد که به نوبه ی خود به قشر آدرنال سیگنالی برای تولید مقدار کافی کورتیزول نمی دهد که یک وضعیت تهدیدکننده ی زندگی است. کمکاری هیپوفیز میتواند در اثر تخریب یا برداشتن بافت قدامی هیپوفیز از طریق آسیبهای مغزی، تومور، سل یا سیفلیس و سایر علل ایجاد شود. این اختلال در گذشته با نام بیماری سیموندز شناخته می شد، اما امروزه بر پایه ی دستهبندی پایگاه داده بیماری ها به آن سندرم شیهان می گویند. [۸] اگر کمکاری هیپوفیز ناشی از از دست دادن خون همراه با زایمان باشد، این اختلال به عنوان سندرم شیهان شناخته می شود.
تصاویر بیشتر
-
The anterior pituitary is the anterior, glandular lobe of the pituitary gland.
- آدنوم هیپوفیز
- هیپوفیز خلفی
- هیپوفیتاریسم
منابع
- ↑ Le Tissier, P.R; Hodson, D.J; Lafont C; Fontanaud P; Schaeffer, M; Mollard, P. (2012) Anterior pituitary cell networks. Front Neuroendocrinol. Aug; 33(3):252-66
- ↑ Nelson, R. J. (2011) An Introduction to Behavioral Endocrinology, 4th Edition. Sunderland, MA: Sinauer Associates, Inc.شابک ۹۷۸−۰۸۷۸۹۳۶۲۰۵
- ↑ Malendowicz, L.K; Rucinski, M; Belloni, A.S; Ziolkowska, A; and Nussdorfer, G.C. (2007) Leptin and the regulation of the hypothalamic-pituitary-adrenal axis. Int Rev Cytol. 263: 63-102.
- ↑ Sone, M. and Osamura, R.Y. (2001) Leptin and the pituitary. Pituitary. Jan-Apr; 4(1-2): 15-23.
- ↑ Scacchi, Massimo; Francesco Cavagnini (2006). "Acromegaly". Pituitary. 9 (4): 297–303. doi:10.1007/s11102-006-0409-4. ISSN 1573-7403. PMID 17077948.
- ↑ Ciccarelli, E; F Camanni (June 1996). "Diagnosis and drug therapy of prolactinoma". Drugs. 51 (6): 954–965. doi:10.2165/00003495-199651060-00004. ISSN 0012-6667. PMID 8736617.
- ↑ خطای یادکرد: خطای یادکرد:برچسب
<ref> غیرمجاز؛ متنی برای یادکردهای با نامbook citeوارد نشده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Summers, V. K. (September 1947). "Diagnosis and Treatment of Simmonds' Disease". Postgraduate Medical Journal. 23 (263): 441–443. doi:10.1136/pgmj.23.263.441. ISSN 0032-5473. PMC 2529616. PMID 20258051.