توماس هنری فلویت
| توماس هنری فلویت | |
|---|---|
 فلویت در آزمایشگاهش در بیمارستان هارتلندز در سال ۱۹۸۴ | |
| زادهٔ | ۲۹ ژوئن ۱۹۲۲ شیملا، هند |
| درگذشت | ۱۲ دسامبر ۲۰۰۶ (۸۴ سال) سولیهال، انگلستان |
| محل تحصیل | دانشگاه کوئینز بلفاست |
| شناختهشده برای | روتاویروس و چند ویروس دیگر |
| پیشینه علمی | |
| شاخه(ها) | ویروسشناسی |
| محل کار | آزمایشگاه منطقه ای ویروس، بیرمنگام |
| امضاء | |
| پرونده:THFsig.png | |
توماس هنری فلویت MD (29 ژوئن ۱۹۲۲–۱۲ دسامبر ۲۰۰۶) یکی از اعضای بنیانگذار (و متعاقباً عضو) کالج سلطنتی پاتولوژیستها بود و (بر اساس امتیاز تحصلیلی) به عنوان عضو کالج سلطنتی پزشکان لندن انتخاب شد. در سال ۱۹۷۸ او رئیس کمیته راهبری سازمان بهداشت جهانی (WHO) در زمینه بیماریهای اسهالی ویروسی شد و در بین سالهای ۱۹۹۰ تا ۱۹۹۶ این سمت را در اختیار داشت. آزمایشگاه او در بیرمنگام از سال ۱۹۸۰ تا زمان بازنشستگی در سال ۱۹۸۷ رئیس مرجع تحقیقاتی سازمان بهداشت جهانی برای عفونتهای روتاویروس و یک ممتحن خارجی، مدرس مدعو و سردبیر مجلات علمی بود. او همچنین از سال ۱۹۷۷ تا ۱۹۸۳ عضو هیئت مدیره خدمات آزمایشگاهی بهداشت عمومی (اکنون آژانس امنیت سلامت بریتانیا) و از سال ۱۹۷۷ تا ۱۹۸۷ مت رئیس کمیته میکروسکوپ الکترونی خدمات آزمایشگاهی بهداشت عمومی را بر عهده داشت.
فلویت تحصیلات پزشکی خود را در دانشگاه کوئینز بلفاست به سر انجام رساند، جایی که در پایان جنگ جهانی دوم در سال ۱۹۴۵ با درجه ممتاز فارغالتحصیل شد. در سال ۱۹۵۱ با جون اِوِلین هال که پیش از او فوت کرد ازدواج نمود. آنها صاحب دو دختر به نامهای جانت آن و جودی الیزابت بودند و دختر دیگر آنها به نام پاملا مارگارت جین در دوران نوزادی درگذشت.[۱]
دوران کودکی[ویرایش]
فلویت در شیملا هند به دنیا آمد، جایی که پدرش، ویلیام ادوارد فلویت (متولد ۱۸۹۴[۲])، فارغالتحصیل دانشگاه آکسفورد، عضو سرویس جنگلداری امپراتوری بود[۳] که در سال ۱۹۶۶ به خدمات جنگلداری هند و بعد از آن به خدمات مدنی هند تبدیل شد.[۴] در سال ۱۹۱۵، پدرش طبق قانون به ارتش ذخیره هند پیوست و در ژوئیه ۱۹۱۶ ستوان دوم شد.[۵][۶] توماس فلویت در سال ۱۹۲۴ به لاهور انگلستان منتقل[۳] و در کالج کمپل در بلفاست تحصیل کرد.[۷]
سالهای اولیه ۱۹۴۵–۱۹۵۶[ویرایش]
فلویت در دانشگاه کوئین بلفاست پزشکی خواند و در سال ۱۹۴۵ با درجه ممتاز فارغالتحصیل شد. او در بیمارستان رویال ویکتوریا در بلفاست کار میکرد و از سال ۱۹۴۶ تا ۱۹۴۸ در کنفرانسهای علمی دانشگاه کوئینز در زمینه باکتریشناسی و آسیبشناسی شرکت کرد. علاقه علمی او به ویروسها با عضویت در هیئت علمی مؤسسه ملی تحقیقات پزشکی در میل هیل همراه شد، جایی که او سه سال بین سالهای ۱۹۴۸ تا ۱۹۵۱ را صرف تحقیق در مورد ویروسهای سرماخوردگی و بررسی تأثیر ویروسهای آنفولانزا بر سلولهای بدن افراد جامعه کرد. این مسئله منجر به اولین استفاده او از میکروسکوپ الکترونی شد و او را به یکی از بهترین متخصصان در زمینه کار با میکروسکوپ الکترونی تبدیل کرد. در سال ۱۹۵۱ او به عنوان مدرس باکتریشناسی به دانشگاه لیدز نقل مکان نمود و در سال ۱۹۵۳ درگیر شیوع آبله شد.[۸] این کار تا بیست و پنج سال بعد، زمانی که در آزمایشگاه مربوط به آبله در دانشکده پزشکی دانشگاه بیرمنگام، بریتانیا، منجر به مرگ جانت پارکر از اعضای آزمایشگاه شد، ادامه یافت. در سال ۱۹۵۱ با جون اولین هال ازدواج کرد و و صاحب سه دختر شد.[۴]
آزمایشگاه منطقه ای ویروس، بیرمنگام، انگلستان ۱۹۵۶–۱۹۸۷[ویرایش]
در سال ۱۹۵۶ فلووت به عنوان مشاور ویروسشناسی در بیمارستان شرقی بیرمنگام (بیمارستان فعلی هارتلندز)، جایی که او یکی از اولین آزمایشگاههای ویروس را در انگلستان تأسیس کرد، منصوب شد. آزمایشگاه او نزدیک به واحد بیماریهای عفونی بود و این موضوع به او امکان داد تا به کمک بررسی اجزای خونی و دفعی به بررسی روشهای تشخیص بالینی میکروبهای فلج اطفال، اسهال، آبله و ایدز بپردازد. او یکی از اعضای تیم مدیریت ارشد بیمارستان بود و به ایجاد آزمایشگاه ایمونولوژی منطقه ای در آنجا کمک کرد.[۷]
علایق فلویت شامل ویروسهای آنفولانزا، کوکساکی A و کوکساکی B، انواع اصلی و فرعی ویروس آبله و ویروس هپاتیت B بود. اگرچه او اولین کسی بهشمار میرفت که علت بیماری دست، پا و دهان را کشف کرده بود،[۹] در اوایل دهه ۱۹۷۰ با کشف ویروسهایی که باعث اسهال میشدند، به ویژه در نوزادان و کودکان خردسال به شهرت بینالمللی دست یافت. آغاز شد. فلویت با کشف روتاویروس یکی از شایعترین علل مرگ و میر نوزادان در کشورهای گرمسیری را تشخیص داد.[۷]
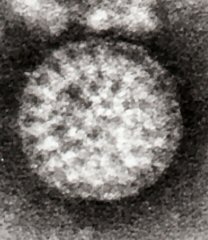
نوروویروس پیش تر به عنوان یک ویروس عفونی توسط آلبرت کاپیکیان با استفاده از میکروسکوپ الکترونی ایمنی[۱۰] کشف شده بود. روث بیشاپ و همکارانش نیز با استفاده از همین روش امیدوار بودند دیگر عوامل بیماریهای عفونی را کشف کنند. آنها ذرات مختلفی ویروسی را در بیوپسیهای روده به کمک میکروسکوپ الکترونی ریزنگار، مشاهده کرده بودند.[۱۱] آمادهسازی بخشهای ریزنگاری برای بررسی معمول بسیار دشوار بود و فلویت و همکارانش نشان دادند که این ویروسها را میتوان در روشی سادهتر با میکروسکوپ الکترونی مستقیماً در مدفوع مشاهده کرد. فلویت در آزمایشگاهش در بیرمنگام، قبل از انتشار مقاله روث بیشاپ، این ویروسها را در مدفوع کودکان بیمار مشاهده کرده بود، با این حال متوجه عفونی بودن این ذرات نشده بود. ذرات ویروس با میکروسکوپ الکترونی ظاهری چرخشکل داشتند و فلویت آنها را «روتاویروس / rotavirus» نامید؛ این ویروس تا به امروز نیز به همین نام شناخته میشوند.[۱۲] فلووت نوشت: «در انجمن ویروسشناسی ویلتشایر جنوبی و سپس در کامپتون، جرالد وود را در اواخر سال ۱۹۷۳ ملاقات کردم. او ویروسی را توصیف کرد که باعث اسهال در گوسالهها میشد. فهمیدم که ما در بچهها هم همین نوع ویروس را داشتیم. زمانی که آن ویروسی را جدا و خالص سازی کردیم، به این نتیجه رسیدیم که این ویروس با بیماریهای عفونی کودکان مرتبط است و ما آنها را روتاویروس نامیدیم.[۱۲][۱۳]
ایده اولیه او پیشنهاد نام «یوربیویروس / urbivirus» به دلیل شباهت ساختاری روتاویروس به اوربیویروس بود. روث بیشاپ، به عنوان اولین فردی که روتاویروسها را به عنوان عامل گاستروانتریت توصیف کرد نیز نام «دوویروس» را برای این میکروب پیشنهاد کرد زیرا این ویروسها در دوازدهه تکثیر میشدند و در آن زمان تصور بر این بود که پوشش خارجی دوگانه پروتئینی دارند. مقالات تحقیقاتی اولیه از دهه ۱۹۷۰ از هر دو نام استفاده میکردند.[۱۴]

فلووت کار مشترک زیادی روی روتاویروسها با دیگران انجام داد تا انواع روتاویروسها را که تقریباً خردسالان گونههای جانوری مختلف را آلوده میکنند، طبقهبندی کند.[۱۵] گروه تحقیقاتی او اولین گروهی بودند که سروتیپهای مختلف روتاویروس را توصیف کردند.[۱۶] این کار برای ساخت واکسن روتاویروس مهم بود. او همچنین دو گونه جدید از آدنوویروسها را شناسایی کرد (که بعداً انواع ۴۰ و ۴۱ نامیده شد) و همچنین وجود کالیسی ویروسها، آستروویروسها و کروناویروسهای مدفوعی در بیماریهای عفونی را تأیید کرد. همچنین او به همراه اچجی پریرا، پیکوبیرناویروسها را کشف[۱۷][۱۸] و همراه با سایر همکارانش برای اولین بار توروویروس انسانی را توصیف کرد.[۱۹]
تراژدی آبله بیرمنگام[ویرایش]

جانت پارکر آخرین فرد تاریخ بهشمار میرفت که بر اثر آبله فوت نمود. او یکی از اعضای آزمایشگاه کار بر روی ویروس واریولا (عامل ایجادکننده آبله) بود. تشخیص بیماری او توسط پروفسور آ. گِدس در بیمارستان شرقی بیرمنگام که در آن بستری شده بود، انجام گرفت. قبل از تأیید تشخیص، یکی از اعضای آزمایشگاهِ فلویت مایعی را از وزیکولهای سلولی جانت پارکر جمعآوری و آن را برای بررسی در آزمایشگاه ویروس به محوطه بیمارستان منتقل کرده بود. این کار میتوانست سبب شیوع مجدد آبله شود. فلویت به کارکنان خود دستور داد تا آزمایشگاه را با فرمالدئید ضد عفونی کنند. بخشی از بیمارستان که در ابتدا از جانت پارکر مراقبت میکرد نیز بهطور کامل ضد عفونی شد. ساختمان بخشهای ۳۱ و ۳۲ نیز بعداً مورد تخریب قرار گرفت. دو نفر از اعضای تیم فلویت نیز متعاقباً قرنطینه شدند، اما به جز مادر جانت پارکر، هیچ مورد دیگری از آبله رخ نداد. مرگ جانت و رخداد این فاجعه منجر به خودکشی پروفسور هنری بدسون شد.[۲۰]
میراث[ویرایش]
فلووت در زمانی تحصیل میکرد که اطلاعات کمی در مورد ویروسها و بیماریهای ویروسی وجود داشت و هیچ بررسی آزمایشگاهی برای کمک یا تأیید تشخیص بیماریهای عفونی وجود نداشت. فلووت یک پیشگام در عرصه خود بهشمار میرفت. امروزه آزمایشگاههای تشخیصی ویروسشناسی، مانند آزمایشگاهی که او در سال ۱۹۵۶ تأسیس کرد، در سراسر جهان یافت میشود. فلویت بیش از ۱۲۰ مقاله و نوشته علمی و پزشکی منتشر کرد.[۷] پس از معرفی واکسن روتاویروس، میزان مرگ و میر کودکان ناشی از روتاویروس در سراسر جهان از حدود ۵۰۰۰۰۰ نفر در سال در سال ۲۰۰۰ به حدود ۲۰۰۰۰۰ در سال ۲۰۱۳ رسید.[۲۱] همانطور که کشورهای بیشتری از این واکسن استفاده میکنند، میزان بروز آن در حال کاهش است.[۲۲]
منابع[ویرایش]
- ↑ Thomas Henry Flewett Royal College of Physicians
- ↑ British Library
- ↑ ۳٫۰ ۳٫۱ P. S. Sharma, The Indian Forester, Vol 50, p. xxii, (1924)
- ↑ ۴٫۰ ۴٫۱ Lives of the Fellows, Royal College of Physicians
- ↑ Army Headquarters, India (3 February 2012). Indian Army List January 1919 — Volume 1. Andrews UK Limited. p. 513. ISBN 978-1-78150-255-6.
- ↑ The London Gazette, 14 July, 1916
- ↑ ۷٫۰ ۷٫۱ ۷٫۲ ۷٫۳ Madeley, D. (2007). "Obituary Thomas Henry Flewett". BMJ. 334 (7596): 753. doi:10.1136/bmj.39167.721898.FA. PMC 1847847. خطای یادکرد: برچسب
<ref>نامعتبر؛ نام «Obituary» چندین بار با محتوای متفاوت تعریف شده است. (صفحهٔ راهنما را مطالعه کنید.). - ↑ Flewett TH. The clinical and laboratory diagnosis of variola minor (alastrim). Br J Clin Pract. 1970 Sep;24(9):397–402.
- ↑ Flewett TH, Warin RP, Clarke SK. 'Hand, foot, and mouth disease' associated with Coxsackie A5 virus. J Clin Pathol. 1963 Jan;16:53-5.
- ↑ Kapikian, AZ; Wyatt, RG; Dolin, R; Thornhill, TS; Kalica, AR; Chanock, RM (Nov 1972). "Visualization by immune electron microscopy of a 27-nm particle associated with acute infectious nonbacterial gastroenteritis". J Virol. 10 (5): 1075–81. doi:10.1128/JVI.10.5.1075-1081.1972. PMC 356579. PMID 4117963.
- ↑ Bishop, RF; Davidson, GP; Holmes, IH; Ruck, BJ (Dec 1973). "Virus particles in epithelial cells of duodenal mucosa from children with acute non-bacterial gastroenteritis". Lancet. 2 (7841): 1281–3. doi:10.1016/s0140-6736(73)92867-5. PMID 4127639.
- ↑ ۱۲٫۰ ۱۲٫۱ Flewett, TH; Woode, GN (1978). "The rotaviruses". Arch Virol. 57 (1): 1–23. doi:10.1007/bf01315633. PMC 7087197. PMID 77663.
- ↑ Letter to Dr Tilli Tansey, 8 February 1998. Woode was at the Institute for Research on Animal Diseases, Compton, Newbury, Berks. See Flewett T H, Bryden A S, Davies H, Woode G N, Bridger J C, Derrick J M. (1974) Relation between viruses from acute gastroenteritis of children and newborn calves. Lancet ii: 61–63.
- ↑ Wyatt GB, Hocking B, Bishop R, Wyatt JL. Duovirus infection as a cause of infantile gastro-enteritis in Port Moresby. P N G Med J. 1976 Sep;19(3):134-6.
- ↑ Flewett, T H.; Bryden, A S.; Davies, H A. (1975). "Virus diarrhoea in foals and other animals". Vet. Rec. 96: 477.
- ↑ Beards, GM; Pilfold, JN; Thouless, ME; Flewett, TH (1980). "Rotavirus serotypes by serum neutralisation". J Med Virol. 5 (3): 231–7. doi:10.1002/jmv.1890050307. PMID 6262451.
- ↑ Treanor, J. J. , R. Dolin. 2005. Astroviruses and picobirnaviruses. 2201–2203, in: Mandell, Douglas and Bennett’s Principles and practice of infectious diseases (6th Ed.). Mandell G. L. , Bennett J. E. , Dolin R. (Editors). Elsevier Churchill Livingstone.
- ↑ Pereira, H. G.; Flewett, T. H.; Candeias, J. A.; Barth, O. M. (1988). "A virus with a bisegmented double-stranded RNA genome in rat (Oryzomys nigripes) intestines". Journal of General Virology. 69 (11): 2749–2754. doi:10.1099/0022-1317-69-11-2749. PMID 3053986.
- ↑ Beards, G. M.; Brown, D.W.G.; Green, J.; Flewett, T. H. (1986). "Preliminary Characterisation of Torovirus-Like Particles of Humans: Comparison With Berne Virus of Horses and Breda Virus of Calves". Journal of Medical Virology. 20 (1): 67–78. doi:10.1002/jmv.1890200109. PMC 7166937. PMID 3093635.
- ↑ [۱] The Shooter Report
- ↑ Tate JE, Burton AH, Boschi-Pinto C, Parashar UD (2016). "Global, Regional, and National Estimates of Rotavirus Mortality in Children <5 Years of Age, 2000-2013". Clinical Infectious Diseases. 62 (Suppl 2): S96–S105. doi:10.1093/cid/civ1013. PMID 27059362.
- ↑ Wang, Haidong; Naghavi, Mohsen; Allen, Christine; Barber, Ryan M.; Bhutta, Zulfiqar A.; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J.; Chen, Alan Zian (2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
{{cite journal}}: Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help)
