پپتید: تفاوت میان نسخهها
Aliesmaili (بحث | مشارکتها) |
Aliesmaili (بحث | مشارکتها) |
||
| خط ۲۵: | خط ۲۵: | ||
===قطعه های پپتیدی=== |
===قطعه های پپتیدی=== |
||
قطعه های پپتیدی اجزائی از پپتید هستند که برای شناسایی یا تعیین کمیت پروتئین منبع مورد استفاده قرار می گیرند. اغلب اینها محصولات تجزیه آنزیمی است که در آزمایشگاه تحت کنترل انجام می شود، اما می تواند از تجزیه طبیعی فسیل و یا چیزهای دیگر حاصل شود. |
قطعه های پپتیدی اجزائی از پپتید هستند که برای شناسایی یا تعیین کمیت پروتئین منبع مورد استفاده قرار می گیرند. اغلب اینها محصولات تجزیه آنزیمی است که در آزمایشگاه تحت کنترل انجام می شود، اما می تواند از تجزیه طبیعی فسیل و یا چیزهای دیگر حاصل شود. <ref>{{cite journal |author=Hummel J, Niemann M, Wienkoop S, ''et al.'' |title=ProMEX: a mass spectral reference database for proteins and protein phosphorylation sites |journal=BMC Bioinformatics |volume=8|pages=216 |year=2007 |pmid=17587460 |pmc=1920535 |doi=10.1186/1471-2105-8-216}}</ref> <ref>{{cite journal |author=Webster J, Oxley D |title=Peptide mass fingerprinting: protein identification using MALDI-TOF mass spectrometry |journal=Methods in Molecular Biology |volume=310 |issue= |pages=227–40 |year=2005 |pmid=16350956 |doi=10.1007/978-1-59259-948-6_16}}</ref><ref>{{cite journal |author=Marquet P, Lachâtre G |title=Liquid chromatography-mass spectrometry: potential in forensic and clinical toxicology |journal=Journal of Chromatography. B, Biomedical Sciences and Applications |volume=733 |issue=1-2 |pages=93–118 |year=1999 |month=October |pmid=10572976 |doi=10.1016/S0378-4347(99)00147-4}}</ref> |
||
[[Image:Peptide Synthesis.svg|thumb|centre|upright=4.1|alt=Table of amino acids| Solid-phase peptide synthesis on a rink amide [[resin]] using [[Fmoc]]-α-[[amine]]-protected [[amino acid]]]] |
[[Image:Peptide Synthesis.svg|thumb|centre|upright=4.1|alt=Table of amino acids| Solid-phase peptide synthesis on a rink amide [[resin]] using [[Fmoc]]-α-[[amine]]-protected [[amino acid]]]] |
||
نسخهٔ ۲۵ ژوئن ۲۰۱۱، ساعت ۲۲:۲۸
این مقاله دقیق، کامل و صحیح ترجمه نشده و نیازمند ترجمه به فارسی است. کل یا بخشی از این مقاله به زبانی بهجز زبان فارسی نوشته شدهاست. اگر مقصود ارائهٔ مقاله برای مخاطبان آن زبان است، باید در نسخهای از ویکیپدیا به همان زبان نوشته شود (فهرست ویکیپدیاها را ببینید). در غیر این صورت، خواهشمند است ترجمهٔ این مقاله را با توجه به متن اصلی و با رعایت سیاست ویرایش، دستور خط فارسی و برابر سازی به زبان فارسی بهبود دهید و سپس این الگو را از بالای صفحه بردارید. همچنین برای بحثهای مرتبط، مدخل این مقاله در فهرست صفحههای نیازمند ترجمه به فارسی را ببینید. اگر این مقاله به زبان فارسی بازنویسی نشود، تا دو هفتهٔ دیگر نامزد حذف میشود و/یا به نسخهٔ زبانی مرتبط ویکیپدیا منتقل خواهد شد. اگر شما اخیراً این مقاله را بهعنوان صفحهٔ نیازمند ترجمه برچسب زدهاید، لطفاً عبارت {{جا:هبک-ترجمه به فارسی|1=پپتید}} ~~~~را نیز در صفحهٔ بحث نگارنده قرار دهید. |
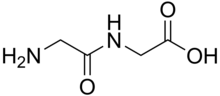

پـِپتیدها (از واژهٔ یونانی πεπτίδια به معنی :گواردنی کوچک، گوارَک) بسپارهای کوچکی هستند که از به هم پیوستن اسیدهای آمینه با ترتیب مشخصی تشکیل شدهاند. پیوند بین هر اسید آمینه با اسید آمینهٔ بعدی پیوند آمید یا پیوند پپتیدی نامیده میشود. پروتئینها، مولکولهای بسپپتیدیای (و یا حتی چند زیرواحد بسپپتیدی، موسوم به ساختار نوع چهارم) هستند. تمایز بین آنها در این است که پپتیدها رشتههایی کوتاه و بسپپتیدها/پروتئینها رشتههایی بلند از اسید آمینه هستند.(این تاپیک رو من دارم تکمیل می کنم لطفا یه تاپیک دیگر را تکمیل کنید)
تعریف
یک تعریف این است که ، زنجیره ساخته شده از ترکیب آمینواسیدها به اندازه کافی کوچک باشد، به جای پروتئین، پپتید می گوییم. به هر حال ، با ظهور روش های ترکیب بهتر، پپتیدهایی به طول صدها آمینواسید ، شامل پرتئین کامل مانند ubiquitin ، می توان ساخت.
تعریف دیگر یک خط تقسیم فرضی با تقریب به طول 50 اسیدآمینه ،مشخص می کند (برخی از افراد طول کمتری در نظر می گیرند). این تعریف تا حدودی اختیاری است. پپتیدهای طولانی، مانند amyloid beta به بیماری آلزایمر مربوط می شود،می تواند به عنوان پروتئین در نظر گرفت . و پروتئین های کوچک مانندinsulin ، به عنوان پپتید در نظر گرفته می شود.
انواع پپتید
در اینجا کلاس های اصلی پپتید ، برطبق طریقه ساخت آنها آورده شده است:
پپتیدهای شیر
پپتیدهای شیر به وسیله شکست آنزیمی توسط آنزیم های گوارشی از پروتئین های شیر به دست می آیند یا هنگام تخمیر شیر توسط باکتری lactobacilli ایجاد می شوند. چندین پپتید شیر، در مطالعات بالینی نشان دادند ، که اثرات ضد فشار خون بر روی حیوانات دارند(همچنین ببینید Lactotripeptides ) .
پپتیدهای ریبوزومی
پپتیدهای ریبوزومی به وسیله ترجمه mRNA ترکیب می شوند. این توابع معمولا در ارگانیسم های بزرگتر،مانند هرمون ها وجوددارند. بعضی از ارگانیسم ها ، پپتیدها را به عنوان آنتی بادی تولید می کنند،مثلاmicrocins ا .[۱] . هنگامی که آنها ترجمه میشوند، آمینواسیدهای باقی مانده ، توسط ریبوزوم مورد استفاده قرار می گیرند.[۲]. به هر حال، این پپتید ها ، بارها تغییر بعد از انتقال دارند، مانند phosphorylation, hydroxylation, sulfonation, palmitylation, glycosylation و ساخت ترکیبات سولفور. در حالت عادی آنها خطی هستند، اگرچه ساختارهای قوسی نیز مشاهده شده اند. کاربرد عجیب دیگر نیز وجوددارد ،مانند راسميک شدن L-آمین.اسید به D-آمینواسید در platypus venom ا. [۳]
پپتیدهای غیرریبوزومی
این پپتیدها به جای ریبوزوم ،به وسیله آنزیم هایی که مختص هر پپتید است تولید می شوند[۴]. معروف ترین پپتید غیرریبوزومی glutathione است که جزئی از سیستم ضداکسنده بیشتر ارگانیسم های هوازی است. پپتید غیرریبوزومی معروف دیگر در تک سلولی ها ، گیاهان و قارچ ها یافت می شود. [۵] [۶] این پپتیدها اغلب دایره ای هستند و می توانند پیچیدگی ساختاری دایره ای زیادی داشته باشند، اگرچه پپتیدهای غیرریبزومی خطی نیز وجود دارند. [۷]
پپتن
پپتن از شیر و یا گوشت حیوانات به هنگام تجزیه مشتق می شود. به علاوه برای تولید پپتیدهای کوچک مواد نتیجه شده شامل چربی، فلزات، نمک، ویتامین، وخیلی دیگر از مواد زیستی ترکیب می شوند. پپتن به عنوان واسط تغذیه در باکتری ها و قارچ ها استفاده می شود. [۸]
قطعه های پپتیدی
قطعه های پپتیدی اجزائی از پپتید هستند که برای شناسایی یا تعیین کمیت پروتئین منبع مورد استفاده قرار می گیرند. اغلب اینها محصولات تجزیه آنزیمی است که در آزمایشگاه تحت کنترل انجام می شود، اما می تواند از تجزیه طبیعی فسیل و یا چیزهای دیگر حاصل شود. [۹] [۱۰][۱۱]

پپتیدها در بیولوژی مولکولی
پپتیدها اخیرا به چند دلیل در بیولوژی مولکولی به جایگاه ویژه ای رسیده اند. اول اینکه پپتیدها اجازه تولید آنتی بادی پپتید در حیوانات بدون نیاز به پالایش پروتئین مورد نظر را می دهند. از این مورد برای ساختن آنتی بادی در خرگوش یا موش در برابر پروتئین ، استفاده می شود.
دلیل دیگراین است که پپتید در اندازه گیری طیف سنجی جرمی مفید است. اجازه مشخص سازی جرم پروتئینی که بر پایه پپتید است را، می دهد. در این مورد پپتیدها اغلب با محلول گوارش بعد از جداسازی ذرات الکتروفورز از پروتئین ، تولید می شود. پپتید اخیرا برای مطالعه ساختار و توابع پروتئین ، استفاده شده است. برای مثال ، ترکیب پپتیدها می تواند جهت تحقیق در مورد فهمیدن اینکه کجا تعامل بین پروتئین و پپتید اتفاق می افتد ، استفاده کرد. سولفور عنصری است که در تعدادی از چند-پپتیدها ، وجود دارد.
پپتیدهای بازداشتی، در تحقیقات بالینی ، برای تست تاثیر پپتید بر پروتئین های سرطان و دیگر بیماری ها استفاده می شود.
پپتیدهای معروف در انسان
خانواده پپتیدهای در این قسمت، پپتیدهای ریبوزومی هستند، معمولا با فعالیت هورمونی. آنها در جایی که علائم تابع آنها فعال شود در رگهای خونی ، رها می شوند.
- انواع پپتیدها
- The Tachykinin peptides
- Vasoactive intestinal peptides
- Pancreatic polypeptide-related peptides
- Opioid peptides
- Calcitonin peptides
منبع
مشارکتکنندگان ویکیپدیا. «Peptide». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۶ اکتبر ۲۰۰۸.
- ↑ Duquesne S, Destoumieux-Garzón D, Peduzzi J, Rebuffat S (2007). "Microcins, gene-encoded antibacterial peptides from enterobacteria". Natural Product Reports. 24 (4): 708–34. doi:10.1039/b516237h. PMID 17653356.
{{cite journal}}: Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Pons M, Feliz M, Antònia Molins M, Giralt E (1991). "Conformational analysis of bacitracin A, a naturally occurring lariat". Biopolymers. 31 (6): 605–12. doi:10.1002/bip.360310604. PMID 1932561.
{{cite journal}}: Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Torres AM, Menz I, Alewood PF; et al. (2002). "D-Amino acid residue in the C-type natriuretic peptide from the venom of the mammal, Ornithorhynchus anatinus, the Australian platypus". FEBS Letters. 524 (1–3): 172–6. doi:10.1016/S0014-5793(02)03050-8. PMID 12135762.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Meister A, Anderson ME (1983). "Glutathione". Annual Review of Biochemistry. 52 (1): 711–60. doi:10.1146/annurev.bi.52.070183.003431. PMID 6137189.
- ↑ Hahn M, Stachelhaus T (2004). "Selective interaction between nonribosomal peptide synthetases is facilitated by short communication-mediating domains". Proceedings of the National Academy of Sciences of the United States of America. 101 (44): 15585–90. doi:10.1073/pnas.0404932101. PMC 524835. PMID 15498872.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Finking R, Marahiel MA (2004). "Biosynthesis of nonribosomal peptides1". Annual Review of Microbiology. 58 (1): 453–88. doi:10.1146/annurev.micro.58.030603.123615. PMID 15487945.
- ↑ Du L, Shen B (2001). "Biosynthesis of hybrid peptide-polyketide natural products". Current Opinion in Drug Discovery & Development. 4 (2): 215–28. PMID 11378961.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Payne JW (1976). "Peptides and micro-organisms". Advances in Microbial Physiology. 13: 55–113. doi:10.1016/S0065-2911(08)60038-7. PMID 775944.
- ↑ Hummel J, Niemann M, Wienkoop S; et al. (2007). "ProMEX: a mass spectral reference database for proteins and protein phosphorylation sites". BMC Bioinformatics. 8: 216. doi:10.1186/1471-2105-8-216. PMC 1920535. PMID 17587460.
{{cite journal}}: Explicit use of et al. in:|author=(help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ Webster J, Oxley D (2005). "Peptide mass fingerprinting: protein identification using MALDI-TOF mass spectrometry". Methods in Molecular Biology. 310: 227–40. doi:10.1007/978-1-59259-948-6_16. PMID 16350956.
- ↑ Marquet P, Lachâtre G (1999). "Liquid chromatography-mass spectrometry: potential in forensic and clinical toxicology". Journal of Chromatography. B, Biomedical Sciences and Applications. 733 (1–2): 93–118. doi:10.1016/S0378-4347(99)00147-4. PMID 10572976.
{{cite journal}}: Unknown parameter|month=ignored (help)
