اسینتوباکتر بومانی
| Acinetobacter baumannii | |
|---|---|
| |
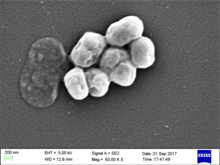
| Acinetobacter baumannii | |
| Scientific classification | |
| Domain: | Bacteria |
| Phylum: | Pseudomonadota |
| Class: | Gammaproteobacteria |
| Order: | Pseudomonadales |
| Family: | Moraxellaceae |
| Genus: | Acinetobacter |
| Species: | A. baumannii
|
| Binomial name | |
| Acinetobacter baumannii Bouvet and Grimont 1986[۱]
| |
اسینتوباکتر بومانی یک باکتری گرم منفی، تقریباً گرد، میله ای شکل (کوکوباسیلوس) است. نام این باکتری از نام باکتریشناس پل باومن گرفته شدهاست.[۲] این باکتری یک پاتوژن فرصت طلب در انسان است و برای افرادی که سیستم ایمنی ضعیفی دارند تأثیر میگذارد و به عنوان یک عفونت بیمارستانی (بیمارستانی) اهمیت آن در حال افزایش است. در حالی که گونههای دیگر از جنس آسینتوباکتر اغلب در نمونههای خاک یافت میشوند (که منجر به این تصور غلط رایج میشود که A. baumannii نیز یک ارگانیسم خاک است)، اسینتوباکتر بومانی بهطور تقریبی منحصراً از محیطهای بیمارستانی جدا شدهاست.[۳] با اینکه این باکتری گاهی اوقات در نمونههای خاک و آب محیطی یافت شدهاست،[۴] اما زیستگاه طبیعی آن هنوز مشخص نیست.
باکتریهای جنس اسینتوباکتر فاقد تاژک هستند که از این ساختار بسیاری از باکتریها برای حرکت (حرکت موجی و حرکت جهشی توسط نوع IV pili) از آن استفاده میکنند. تحرک در A. baumannii همچنین ممکن است به دلیل دفع اگزوپلی ساکارید باشد، که یک لایه از زنجیرههای قندی با وزن مولکولی بالا در پشت باکتری برای حرکت به جلو ایجاد میکند.[۵] میکروبیولوژیستهای بالینی معمولاً اعضای جنس آسینتوباکتر را از دیگر جنسهای خانواده موراکسیلاسه با انجام آزمایش اکسیداز، به عنوان Acinetobacter spp، متمایز میکنند. باکتریهای اسینتوباکتر تنها اعضای موراکسیلاسه هستند که فاقد آنزیم سیتوکروم c اکسیداز هستند.
اسینتوباکتر بومانی بخشی از مجموعه ACB است (A. baumannii , A. calcoaceticus، و گونههای ژنوم Acinetobacter 13TU). تعیین گونههای خاص اعضای مجموعه ACB دشوار است و آنها دارای بیشترین ارتباط بالینی در بین اعضای این جنس هستند.[۶][۷] اسینتوباکتر بومانی همچنین به عنوان یک پاتوژن ESKAPE (انتروکوکوس فاسیوم، استافیلوکوکوس اورئوس، کلبسیلا پنومونیه، اسینتوباکتر بومانی، سودوموناس آئروژینوزا، و گونههای انتروباکتر) شناسایی شدهاست . اسینتوباکتر بومانی و سودوموناس آئروژینوزا و گونههای انتروباکتر، گروهی از پاتوژنهایی هستند که دارای نرخ بالایی از مقاومت آنتیبیوتیکی هستند که مسئول اکثر عفونتهای بیمارستانی هستند.[۸]
OmpA
[ویرایش]چسبندگی میتواند یک عامل تعیینکننده حیاتی در بیماریزایی باکتریها باشد. توانایی اتصال به سلولهای میزبان به باکتریها این اجازه را میدهد تا با روشهای مختلف با آنها تعامل داشته باشند، چه توسط سیستم ترشحی نوع III یا صرفاً با نگه داشتن باکتری در برابر حرکت مایعات. پروتئین غشای خارجی A (OmpA) نشان داده شدهاست که در چسبیدن اسینتوباکتر بومانی به سلولهای اپیتلیال نقش دارد که این حالت به باکتریها اجازه میدهد تا از طریق مکانیسم زیپ به سلولها حمله کنند.[۹] همچنین نشان داده شد که پروتئین OmpA در میتوکندری سلولهای اپیتلیال متمرکز میشود و با تحریک تولید گونههای فعال اکسیژن باعث نکروز میشود.[۱۰]
مقاومت آنتیبیوتیکی
[ویرایش]مکانیسمهای مقاومت آنتیبیوتیکی را میتوان به سه گروه طبقهبندی کرد. اول، مقاومت را میتوان با کاهش نفوذ پذیری از غشا یا افزایش انتشار به خارج آنتیبیوتیک و در نتیجه جلوگیری از دسترسی به هدف به دست آورد. دوم، باکتریها میتوانند از طریق جهش ژنتیکی یا اتغییرات پس از ترجمه، از گیرنده آنتیبیوتیک محافظت کنند، و در آخر، آنتیبیوتیکها را میتوان مستقیماً با هیدرولیز یا تغییرات در آنتیبیوتیکها غیرفعال کرد. یکی از مهمترین سلاحها در تسلیحات اسینتوباکتر، انعطافپذیری ژنتیکی چشمگیر آن است که جهشها و بازآراییهای سریع ژنتیکی را تسهیل کرده و همچنین ادغام عوامل خارجی که توسط عناصر ژنتیکی متحرک حمل میشوند. از این میان، توالیهای ژنتیکی الحاقی یکی از نیروهای کلیدی در شکلدهی ژنوم باکتریها و در نهایت تکامل در نظر گرفته میشوند.[۱۱]
جزایر مقاومتی AbaR
[ویرایش]جزایر بیماریزایی، ساختارهای ژنتیکی نسبتاً رایج در پاتوژنهای باکتریایی هستند که از دو یا چند ژن مجاور تشکیل شدهاند که ویرولانس (بیماریزایی) یک پاتوژن را افزایش میدهند. آنها ممکن است حاوی ژنهایی باشند که سموم را رمزگذاری میکنند، خون را منعقد میکنند یا به باکتریها اجازه میدهند در مقابل آنتیبیوتیکها مقاومت کنند. جزایر مقاومت نوع AbaR نمونه ای از مقاوم به دارو در اسینتوباکتر بومانی هستند. ژنهای مقاومت آنتیبیوتیکی معمولاً بین باکتریهای گرم منفی از طریق پلاسمیدها از طریق کونژوگه (هم یوغی) منتقل میشوند که ایجاد سویههای مقاوم جدید را تسریع میکند. AbaR حاوی چندین ژن برای مقاومت آنتیبیوتیکی است که همگی توسط توالیهای الحاقی احاطه شدهاند.
پمپهای افلاکس
[ویرایش]پمپهای افلاکس، ساختارهای پروتئینی هستند که از انرژی برای پمپاژ به بیرون آنتیبیوتیکها و سایر مولکولهای کوچکی که وارد سیتوپلاسم باکتری و فضای پری پلاسمیک شدهاند، استفاده میکنند. با پمپاژ مداوم آنتیبیوتیکها به خارج سلول، باکتریها میتوانند غلظت آنتیبیوتیک معین مورد نیاز برای از بین بردن آنها را افزایش دهند. اسینتوباکتر بومانی دارای دو پمپ جریان اصلی است که مقاومت آن را به ضد میکروبی آنها افزایش میدهند. اولین مورد، AdeB، نشان داده شدهاست که مسئول مقاومت آمینوگلیکوزیدها است.[۱۲] دوم، AdeDE، مسئول خروج طیف گستردهای از سوبستراها، از جمله تتراسایکلین، کلرامفنیکل و کارباپنمهای مختلف است.[۱۳] بسیاری از پمپهای جریان دیگر در سویههای مقاوم اسینتوباکتربومانی نقش دارند.[۱۱]
RNAهای کوچک
[ویرایش]RNAهای کوچک باکتری RNAهای غیر کد کننده ای هستند که فرایندهای سلولی مختلف را تنظیم میکنند. بهطور تجربی sRNA و AbsR25 در سویه MTCC 1425 (ATCC15308) تأیید شدهاند که یک سویه (مقاوم به چند دارو) وجود دارد که به ۱۲ آنتیبیوتیک مقاومت نشان میدهد. sRNA AbsR25 میتواند در تنظیم پمپ جریان و مقاومت دارویی نقش داشته باشد.[۱۴]
آنزیم بتالاکتاماز
[ویرایش]نشان داده شدهاست که اسینتوباکتر بومانی حداقل یک بتالاکتاماز تولید میکند که آنزیمی است که مسئول شکستن حلقه لاکتام چهار اتمی آنتیبیوتیکهای بتالاکتام است. آنتیبیوتیکهای بتالاکتام از نظر ساختاری با پنی سیلین مرتبط هستند که موجب مهار سنتز دیواره سلولی میشود. با شکسته شدن حلقه لاکتام در این آنتیبیوتیکها، این آنتیبیوتیکها برای باکتریها بیضرر میشوند.
تشکیل بیوفیلم
[ویرایش]اسینتوباکتر بومانی به دلیل توانایی برای زنده ماندن بر روی سطوح مصنوعی برای طولانی مدت مورد توجه قرار گرفتهاست، بنابراین این شرایط به اسینتوباکتر بومانی اجازه میدهد که در محیط بیمارستان باقی بماند و تصور میشود که این به دلیل توانایی آن در تشکیل بیوفیلم باشد.[۱۵] در بسیاری از باکتریهایی که بیوفیلم تشکیل میدهند، این فرایند توسط تاژک انجام میگیرد. اما برای اسینتوباکتر بومانی، به نظر میرسد که این فرایند توسط مویک (پیلی) انجام میشود. علاوه بر این، نشان داده شد که اختلال در chaperone pili و ژنهای آشر csuC و csuE مانع از تشکیل بیوفیلم میشود.[۱۶] نشان داده شدهاست که متابولیسم میکروارگانیسمها را در بیوفیلم تغییر میکند که ممکن است به دلیل کمتر بودن مواد مغذی در ااعماق بیوفیلم باشد، و در نتیجه باعث کاهش حساسیت آنها را به آنتیبیوتیکها میشود. متابولیسم کندتر میتواند از جذب آنتیبیوتیک در باکتری یا از انجام عملکرد آنتیبیوتیکهای خاص جلوگیری کند. بیوفیلم همچنین یک مانع فیزیکی در برابر مولکولهای بزرگتر ایجاد میکند و ممکن است از خشک شدن باکتریها جلوگیری کنند.[۴][۱۷]
علائم و نشانههای عفونت
[ویرایش]اسینتوباکتر بومانی یک پاتوژن فرصت طلب با طیف وسیعی از بیماریهای مختلف است که هر کدام علائم خاص خود را دارند. برخی از انواع احتمالی عفونت اسینتوباکتر بومانی عبارتند از:[نیازمند منبع]
- پنومونی
- عفونتهای جریان خون
- مننژیت
- عفونت زخم و محل جراحی، از جمله فاسیای نکروزان
- عفونتهای دستگاه ادراری
علائم عفونت اسینتوباکتر بومانی، غالباً از سایر عفونتهای فرصت طلب ناشی از سایر باکتریهای فرصت طلب مانند کلبسیلا پنومونیه و استرپتوکوک پنومونیه، قابل تشخیص نیستند.[نیازمند منبع]
علائم عفونت اسینتوباکتر بومانی به نوبه خود از تب و لرز، کهیر، گیجی یا حالات روانی تغییر یافته، درد یا سوزش هنگام ادرار کردن، میل شدید به ادرار کردن مکرر، حساسیت به نور شدید، تهوع (با یا بدون استفراغ) متغیر است. دردهای عضلانی و قفسه سینه، مشکلات تنفسی و سرفه (با یا بدون مخاط زرد، سبز یا خونی).[۱۸] در برخی موارد، اسینتوباکتر بومانی ممکن است هیچ گونه عفونت یا علائمی نداشته باشد، همانند کلون سازی در زخم باز یا محل تراکئوستومی.[نیازمند منبع]
درمان
[ویرایش]هنگامی که عفونتها توسط ایزولههای اسینتوباکتر حساس به آنتیبیوتیک ایجاد میشوند، ممکن است چندین گزینه درمانی وجود داشته باشد، از جمله یک سفالوسپورین با طیف وسیع (سفتازیدیم یا سفپیم)، یک مهارکننده ترکیبی بتالاکتام/بتا-لاکتاماز (یعنی یکی شامل سولباکتام)، یا یک کارباپنم (به عنوان مثال، ایمی پنم یا مروپنم). از آنجایی که اکثر عفونتهای حاصل از این باکتری در حال حاضر به چندین دارو مقاوم هستند، تعیین حساسیت سویه خاص برای موفقیت درمان ضروری است. در گذشته، عفونتها با ایمی پنم یا مروپنم درمان میشدند، اما افزایش مداوم مقاومت به کارباپنم در اسینتوباکتر بومانی مشاهده شدهاست.[۱۹] در نتیجه، روشهای درمانی اغلب بر روی پلیمیکسینها، بهویژه کولیستین بازمیگردند.[۲۰][۲۱] آنتیبیوتیک کولیستین به عنوان آخرین راه حل در نظر گرفته میشود، زیرا این دارو اغلب باعث آسیب کلیه و سایر عوارض جانبی میشود.[۲۲] روشهای پیشگیری در بیمارستانها در افزایش شستن دستها و روشهای دقیقتر استریلیزاسیون متمرکز هستند.[۲۳] عفونت حاصل از اسینتوباکتر بومانی اخیراً با استفاده از فاژ درمانی، درمان شدهاست.[۲۴] فاژها ویروسهایی هستند که بهطور اختصاصی به باکتریها حمله میکنند[۲۵] و همچنین نشان داده شدهاست که اسینتوباکتر بومانی را نسبت به آنتیبیوتیکهایی که معمولاً در برابر آن مقاومت میکنند را دوباره حساس میکنند.[۲۶]

دانشمندان MIT، مؤسسه Broad's Harvard's Broad's CSAIL و MIT's CSAIL ترکیبی به نام هالیسین را کشف کردند که میتواند بهطور مؤثر اسینتوباکتر بومانی را بکشد.[۲۷][۲۸]
بروز در بیمارستانها
[ویرایش]عفونتهای اسینتوباکتر بومانی، که به عنوان یک عفونت فرصت طلب از آن یاد میشود، در بیمارستانها بسیار شایع هستند. با این حال، اسینتوباکتر بومانی خطر بسیار کمی برای افراد سالم دارد.[۲۹] با این حال، عواملی که خطر عفونت را افزایش میدهند عبارتند از:
- داشتن سیستم ایمنی ضعیف
- بیماری مزمن ریه
- دیابت
- طولانی شدن مدت اقامت در بیمارستان
- بیماری که نیاز به استفاده از دستگاه تنفس مصنوعی بیمارستانی دارد
- درمان زخم باز در بیمارستان
- درمانهایی که نیاز به دستگاههایی دارند که به داخل بدن وارد میشوند مانند کاتترهای ادراری
اسینتوباکتر بومانی میتواند از طریق تماس مستقیم با سطوح، اشیاء و پوست افراد آلوده، منتقل گردد.[۱۸]
اسینتوباکتر بومانی معمولاً توسط یک بیمار که این باکتری در بدن آن کلونیزه شده، به بیمارستان وارد میشود. این باکتری به دلیل توانایی زنده ماندن بر روی سطوح مصنوعی و مقاومت در برابر خشک شدن، میتواند برای مدتی باقی بماند و احتمالاً بیماران جدید را مبتلا کند. به دلیل استفاده مداوم از آنتیبیوتیکها توسط بیماران در بیمارستان، مشکوک به رشد شیوع اسینتوباکتر بومانی در محیطهای بیمارستانی است.[۳۰] اسینتوباکتر میتواند از طریق تماس فرد به فرد یا تماس با سطوح آلوده منتقل شود.[۳۱] اسینتوباکتر بومانی میتواند از طریق زخمهای باز، کاتترها و لولههای تنفسی وارد شود. در مطالعهای در بخش مراقبتهای ویژه اروپا در سال ۲۰۰۹، مشخص شد که اسینتوباکتر بومانی مسئول ۱۹٫۱ درصد موارد پنومونی مرتبط با ونتیلاتور است.[۳۲]
منابع
[ویرایش]- ↑ Parte, A.C. "Acinetobacter". LPSN.
- ↑ Lin, Ming-Feng; Lan, Chung-Yu (2014). "Antimicrobial Resistance in Acinetobacter baumannii: From Bench to Bedside". World Journal of Clinical Cases. 2 (12): 787–814. doi:10.12998/wjcc.v2.i12.787. PMC 4266826. PMID 25516853.
- ↑ Antunes, Luísa C.S.; Visca, Paolo; Towner, Kevin J. (August 2014). "Acinetobacter baumannii: evolution of a global pathogen". Pathogens and Disease. 71 (3): 292–301. doi:10.1111/2049-632X.12125. PMID 24376225.
- ↑ ۴٫۰ ۴٫۱ Yeom, Jinki; Shin, Ji-Hyun; Yang, Ji-Young; Kim, Jungmin; Hwang, Geum-Sook; Bundy, Jacob Guy (6 March 2013). "1H NMR-Based Metabolite Profiling of Planktonic and Biofilm Cells in Acinetobacter baumannii 1656-2". PLOS ONE. 8 (3): e57730. Bibcode:2013PLoSO...857730Y. doi:10.1371/journal.pone.0057730. PMC 3590295. PMID 23483923.
- ↑ McQueary, Christin N.; Kirkup, Benjamin C.; Si, Yuanzheng; Barlow, Miriam; Actis, Luis A.; Craft, David W.; Zurawski, Daniel V. (30 June 2012). "Extracellular stress and lipopolysaccharide modulate Acinetobacter baumannii surface-associated motility". Journal of Microbiology. 50 (3): 434–443. doi:10.1007/s12275-012-1555-1. PMID 22752907.
- ↑ O'Shea, MK (May 2012). "Acinetobacter in modern warfare". International Journal of Antimicrobial Agents. 39 (5): 363–75. doi:10.1016/j.ijantimicag.2012.01.018. PMID 22459899.
- ↑ Gerner-Smidt, P (October 1992). "Ribotyping of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex". Journal of Clinical Microbiology. 30 (10): 2680–5. doi:10.1128/JCM.30.10.2680-2685.1992. PMC 270498. PMID 1383266.
- ↑ Rice, LB (15 April 2008). "Federal funding for the study of antimicrobial resistance in nosocomial pathogens: no ESKAPE". The Journal of Infectious Diseases. 197 (8): 1079–81. doi:10.1086/533452. PMID 18419525.
- ↑ Choi, Chul Hee; Lee, Jun Sik; Lee, Yoo Chul; Park, Tae In; Lee, Je Chul (2008). "Acinetobacter baumannii invades epithelial cells and outer membrane protein A mediates interactions with epithelial cells". BMC Microbiology. 8 (1): 216. doi:10.1186/1471-2180-8-216. PMC 2615016. PMID 19068136.
- ↑ Lee, Jun Sik; Choi, Chul Hee; Kim, Jung Wook; Lee, Je Chul (23 June 2010). "Acinetobacter baumannii outer membrane protein a induces dendritic cell death through mitochondrial targeting". The Journal of Microbiology. 48 (3): 387–392. doi:10.1007/s12275-010-0155-1. PMID 20571958.
- ↑ ۱۱٫۰ ۱۱٫۱ Kyriakidis, I; Vasileiou, E; Pana, Z-D; Tragiannidis, A (2021). "Acinetobacter baumannii Antibiotic Resistance Mechanisms". Pathogens. 10 (373): 373. doi:10.3390/pathogens10030373. PMC 8003822. PMID 33808905.
- ↑ Magnet, S; Courvalin, P; Lambert, T (December 2001). "Resistance-nodulation-cell division-type efflux pump involved in aminoglycoside resistance in Acinetobacter baumannii strain BM4454". Antimicrobial Agents and Chemotherapy. 45 (12): 3375–80. doi:10.1128/aac.45.12.3375-3380.2001. PMC 90840. PMID 11709311.
- ↑ Chau, SL; Chu, YW; Houang, ET (October 2004). "Novel resistance-nodulation-cell division efflux system AdeDE in Acinetobacter genomic DNA group 3". Antimicrobial Agents and Chemotherapy. 48 (10): 4054–5. doi:10.1128/aac.48.10.4054-4055.2004. PMC 521926. PMID 15388479.
- ↑ Sharma, Rajnikant; Arya, Sankalp; Patil, Supriya Deepak; Sharma, Atin; Jain, Pradeep Kumar; Navani, Naveen Kumar; Pathania, Ranjana (2014-01-01). "Identification of novel regulatory small RNAs in Acinetobacter baumannii". PLOS ONE. 9 (4): e93833. Bibcode:2014PLoSO...993833S. doi:10.1371/journal.pone.0093833. ISSN 1932-6203. PMC 3976366. PMID 24705412.
- ↑ Espinal, P; Martí, S; Vila, J (January 2012). "Effect of biofilm formation on the survival of Acinetobacter baumannii on dry surfaces". The Journal of Hospital Infection. 80 (1): 56–60. doi:10.1016/j.jhin.2011.08.013. PMID 21975219.
- ↑ Tomaras, AP; Dorsey, CW; Edelmann, RE; Actis, LA (December 2003). "Attachment to and biofilm formation on abiotic surfaces by Acinetobacter baumannii: involvement of a novel chaperone-usher pili assembly system". Microbiology. 149 (Pt 12): 3473–84. doi:10.1099/mic.0.26541-0. PMID 14663080.
- ↑ Worthington, RJ; Richards, JJ; Melander, C (7 October 2012). "Small molecule control of bacterial biofilms". Organic & Biomolecular Chemistry. 10 (37): 7457–74. doi:10.1039/c2ob25835h. PMC 3431441. PMID 22733439.
- ↑ ۱۸٫۰ ۱۸٫۱ "What Is Acinetobacter Baumannii?". Everyday Health. Retrieved 18 April 2017.
- ↑ Su, CH; Wang, JT; Hsiung, CA; Chien, LJ; Chi, CL; Yu, HT; Chang, FY; Chang, SC (2012). "Increase of carbapenem-resistant Acinetobacter baumannii infection in acute care hospitals in Taiwan: Association with hospital antimicrobial usage". PLOS One. 7 (5): e37788. Bibcode:2012PLoSO...737788S. doi:10.1371/journal.pone.0037788. PMC 3357347. PMID 22629456.
{{cite journal}}: Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help) - ↑ Abbo, A; Navon-Venezia, S; Hammer-Muntz, O; Krichali, T; Siegman-Igra, Y; Carmeli, Y (January 2005). "Multidrug-resistant Acinetobacter baumannii". Emerging Infectious Diseases. 11 (1): 22–9. doi:10.3201/eid1101.040001. PMC 3294361. PMID 15705318.
{{cite journal}}: Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help) - ↑ Falagas, Matthew E.; Vardakas, Konstantinos Z.; Kapaskelis, Anastasios; Triarides, Nikolaos A.; Roussos, Nikolaos S. (May 2015). "Tetracyclines for multidrug-resistant Acinetobacter baumannii infections". International Journal of Antimicrobial Agents. 45 (5): 455–460. doi:10.1016/j.ijantimicag.2014.12.031. ISSN 1872-7913. PMID 25801348.
- ↑ Spapen, H; Jacobs, R; Van Gorp, V; Troubleyn, J; Honoré, PM (25 May 2011). "Renal and neurological side effects of colistin in critically ill patients". Annals of Intensive Care. 1 (1): 14. doi:10.1186/2110-5820-1-14. PMC 3224475. PMID 21906345.
{{cite journal}}: Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help) - ↑ "Acinetobacter in Healthcare Settings". CDC. Retrieved 8 April 2013.
- ↑ "He was dying. Antibiotics weren't working. Then doctors tried a forgotten treatment". Mother Jones (به انگلیسی). Retrieved 2018-05-17.
- ↑ Altamirano, Fernando L. Gordillo; Barr, Jeremy J. (20 March 2019). "Phage Therapy in the Postantibiotic Era". Clinical Microbiology Reviews. 32 (2). doi:10.1128/CMR.00066-18. PMC 6431132. PMID 30651225.
- ↑ Gordillo Altamirano, Fernando; Forsyth, John H.; Patwa, Ruzeen; Kostoulias, Xenia; Trim, Michael; Subedi, Dinesh; Archer, Stuart K.; Morris, Faye C.; Oliveira, Cody (February 2021). "Bacteriophage-resistant Acinetobacter baumannii are resensitized to antimicrobials". Nature Microbiology. 6 (2): 157–161. doi:10.1038/s41564-020-00830-7. PMID 33432151.
- ↑ Ray, Tiernan (13 March 2020). "MIT's deep learning found an antibiotic for a germ nothing else could kill". ZDNet.
- ↑ Stokes, Jonathan M.; Yang, Kevin; Swanson, Kyle; Jin, Wengong; Cubillos-Ruiz, Andres; Donghia, Nina M.; MacNair, Craig R.; French, Shawn; Carfrae, Lindsey A. (20 February 2020). "A Deep Learning Approach to Antibiotic Discovery". Cell. 180 (4): 688–702.e13. doi:10.1016/j.cell.2020.01.021. PMC 8349178. PMID 32084340.
- ↑ "Acinetobacter in Healthcare Settings". Centers for Disease Control and Prevention. US Department of Health and Human Services. Retrieved 18 April 2017.
- ↑ Dijkshoorn, Lenie; Nemec, Alexandr; Seifert, Harald (December 2007). "An increasing threat in hospitals: multidrug-resistant Acinetobacter baumannii". Nature Reviews Microbiology. 5 (12): 939–951. doi:10.1038/nrmicro1789. PMID 18007677.
- ↑ "Acinetobacter in Healthcare Settings - HAI - CDC". www.cdc.gov. Retrieved 2 April 2018.
- ↑ Koulenti, Despoina; Lisboa, Thiago; Brun-Buisson, Christian; Krueger, Wolfgang; Macor, Antonio; Sole-Violan, Jordi; Diaz, Emili; Topeli, Arzu; DeWaele, Jan (August 2009). "Spectrum of practice in the diagnosis of nosocomial pneumonia in patients requiring mechanical ventilation in European intensive care units". Critical Care Medicine. 37 (8): 2360–2369. doi:10.1097/CCM.0b013e3181a037ac. PMID 19531951.
