ویروپلاسم
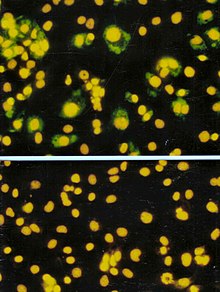
ویروپلاسم (به انگلیسی: viroplasm) که گاهی «کارخانه ویروس» نیز شناخته میشود،[۱] یک جسم انکلوزیونی در سلول است که درون آن تکثیر و تولید ویروس اتفاق میافتد به همین علت این اجسام به عنوان کارخانههای تولید ویروس در سلول نظر گرفته میشوند. ویروپلاسمهای زیادی میتواند در یک سلول آلوده ایجاد شود که در میکروسکوپ الکترونی به صورت بخشهای متراکم به دیده میشود. اطلاعات بسیار کمی در مورد مکانیسم تشکیل ویروپلاسم وجود دارد و تحقیقاتی برای درک آن همچنان ادامه دارد.
تعریف
[ویرایش]ویروپلاسم یک محفظه بزرگ اطراف هسته یا سیتوپلاسمی است که در آن تکثیر و مونتاژ ویروس اتفاق میافتد.[۲] تشکیل ویروپلاسم در اثر فعل و انفعالات بین ویروس و سلول آلوده ایجاد میشود و در این بخشها محصولات ویروسی و موارد مورد نیاز برای تکثیر ایجاد میگردند.[۲]
ساختار و شکلگیری
[ویرایش]ویروپلاسمها در ناحیه پرینوکلر یا در سیتوپلاسم سلولهای آلوده تجمع مییابند و در اوایل چرخهٔ ایجاد عفونت تشکیل میشوند.[۲][۳] تعداد و اندازه ویروپلاسمها به گونه ویروس، نقصهای ویروس، گونه میزبان و مرحله عفونت بستگی دارد.[۴] به عنوان مثال، ویروپلاسمهای میمی ویروس اندازهای مشابه با هسته میزبانشان، آمیب آکانتاموبا پلی فاگا دارند.[۵]
بسته به مرحله چرخه تکثیر ویروس، یک ویروس میتواند تغییراتی را در ترکیب و سازماندهی سلولهای سلولی و بخشهای غشایی سلول میزبان ایجاد کند.[۱] این فرایند شامل تعدادی از فعل و انفعالات پیچیده و رویدادهای سیگنالدهنده بین عوامل ویروسی و سلول میزبان است.
ویروپلاسمها در اوایل عفونت تشکیل میشوند. در بسیاری از موارد، بازآراییهای سلولی ناشی از عفونت ویروسی (ادغام ژنوم ویروس در سلول میزبان) به ساخت اجزای پیچیدهتر در ویروپلاسمها کمک میکند. ویروپلاسم جایی است که اجزایی مانند آنزیمهای رپلیکاز، مواد ژنتیکی ویروس و پروتئینهای مورد نیاز برای همانندسازی متمرکز میشوند و در نتیجه کارایی همانندسازی را افزایش میدهند.[۱] در زمان ساخت اجزای ویروس، مقادیر زیادی ریبوزوم، اجزای سنتزی پروتئین، چاپرونهای تاشو پروتئین و میتوکندری به کار گرفته میشوند. برخی از اجزای غشاء سلولی نیز برای تکثیر ویروسی مورد استفاده قرار میگیرند و در برخی از پروتئینها برای تولید پوششهای ویروسی، زمانی که ویروسها دارای پوشش است، استفاده میشوند. تکثیر ویروس، سنتز پروتئین و ساخت اجزا نیاز به مقدار قابل توجهی انرژی دارد که توسط خوشههای بزرگ میتوکندری در حاشیه ویروپلاسمها تأمین میشود. کارخانه ویروس اغلب توسط غشایی که از شبکه آندوپلاسمی زبر یا عناصر اسکلت سلولی مشتق شده است محصور میشود.[۲][۳]
در سلولهای حیوانی، ذرات ویروس توسط جمعآوری وابسته به میکروتوبول بر اساس بیگانه یا ناقض بودن پروتئین در نزدیکی مرکز سازماندهی میکروتوبول (MTOC) جمع میشوند، بنابراین ویروسپلاسمهای ویروسهای حیوانی بهطور کلی در نزدیکی MTOC قرار دارند.[۲][۶] MTOCها در سلولهای گیاهی یافت نمیشوند به همین علت ویروسهای گیاهی باعث ساخت مجدد ساختار غشا سلولی میشوند تا ویروسپلاسم را از جنس غشاء سلول تشکیل دهند (این عملکرد عمدتاً در ویروسهای RNA گیاهان دیده میشود).[۳]
عملکرد
[ویرایش]ویروپلاسم مکانی در داخل سلول آلوده است که در آن تکرار و جمعآوری ویروسی صورت میگیرد.[۲] قالب بندی ویروسپلاسم به کمک غشا، اجزای مورد نیاز ویروس را برای تکثیر ژنوم و مورفوژنز ذرات ویروس جدید فراهم، بنابراین باعث افزایش بهرهوری فرآیندتکثیر ویروس میشود.[۲] استفاده از غشاءهای سلولی و سیتو اسکلت برای تولید کارخانههای تکثیر ویروس نیز میتواند به روشهای دیگر به بقای ویروس کمک کند. اختلال غشاء سلولی میتواند، به عنوان مثال، انتقال پروتئینهای ایمنی به سطح سلولهای آلوده را کُند کند و ویروس را از پاسخهای ایمنی ذاتی سلول محافظت کند. همچنین تنظیم مجدد سیتو اسکلت میتواند انتشار ویروس را تسهیل[۱] و آن در برابر تخریب توسط پروتیازها و نیوکلیازها محافظت کند.[۳]
در ویروس موزاییک گل کلم (CaMV)، ویروپلاسم، انتقال ویروس توسط شته ناقل را بهبود میبخشند. هنگامی که حشره یک سلول گیاهی آلوده یا سلولی در نزدیکی سلولهای آلوده را نیش میزند، ویروپلاسمها به آزاد سازی ویریونها و سرایت آن کمک میکنند.[۷]
ویروسهای دارای ویروپلاسم
[ویرایش]ویروپلاسمها در گروههای مختلفی از ویروسهای یوکاریوتی که خود را در درون سیتوپلاسم آنها سلول تکثیر میکنند، دیده میشود. با این حال، ویروپلاسمهای ویروسهای گیاهی به اندازه ویروسهای حیوانی مورد مطالعه قرار نگرفتهاند.[۲] ویروپلاسمهای در ویروس موزاییک گل کلم،[۸] روتاویروس،[۹] ویروس واکسینیا[۱۰] و ویروس کوتوله برنج یافت شدهاند.[۱۱] این کارخانههای ویروسی در زیر میکروسکوپ الکترونی، پر چگالی به نظر میرسند و در سیتوپلاسم سلول نامحلولاند.[۲]
| طبقهبندی بالتیمور | خانواده | گونهها |
| I: ویروسهای dsDNA | پاکسویریده آسفارویریده ایریدوویریده میمیویریده |
ویروس واکسینیا[۱۲] ویروس تب خوکی آفریقاییویروس قورباغه[۲] میمی ویروس آکانتامبا پلی فاگا
ویروس هرپس سیمپلکس[۲] |
| II: ویروسهای ssDNA | ||
| III: ویروسهای dsRNA | رئوویریده | رئوویروس پرندگان |
| IV: ویروسهای (+)ssRNA | توگاویریده فلاویریده |
ویروس سرخجه فلاوی ویروس[۲] |
| V: (-) ویروسهای ssRNA | رابدوویریده
پریبونیاویریده |
ویروس هاری ویروس ارتوبونیا |
| VI: ویروسهای ssRNA-RT | رتروویریده | ویروس نقص ایمنی انسانی |
| VII: ویروسهای dsDNA-RT | کالیموویریده | ویروس موزاییک گل کلم |
امکان تکامل مشترک با میزبان
[ویرایش]ساختارهای انباشته در ویروپلاسم ممکن است از بخشهای عملکردی ویروسی در برابر تخریب توسط سیستمهای دفاعلی سلولی محافظت کنند. به عنوان مثال، تشکیل کارخانههای ویروسی ویروپلاسم (ASFV) بسیار شبیه به تشکیل آگرزوم است.[۲] آگرزوم یک اندامک دور از هسته است که در آن پروتئینهای ناقص و ناکارآمد توسط اجزای سلول برای تخریب به آن انتقال مییابند. احتمال میرود که ویروپلاسم میتواند محصول یک تکامل مشترک بین ویروس و میزبان آن باشد.[۷] این امکان وجود دارد که یک پاسخ سلولی که در ابتدا برای کاهش نقص عملکردی پروتئینهای بیگانه یا ناکارآمد طراحی شده بوده است، توسط ویروسهای سیتوپلاسمی برای بهبود تکثیر، سنتز کپسید ویروس مورد استفاده قرار گرفته باشد.[۷] از طرف دیگر، فعالسازی مکانیسمهای دفاعی میزبان ممکن است شامل جداسازی اجزای ویروس برای جلوگیری از انتشار و به دنبال آن خنثیسازی آنها باشد. برای مثال، ویروپلاسمهای ویروسهای پستانداران حاوی عناصر خاصی از اجزای تخریب کننده سلول هستند که ممکن است مکانیسمهای محافظتی سلولی را در برابر ورود اجزای ویروسی از بین ببرد.[۱۳] با توجه به تکامل همزمان ویروسها با سلولهای میزبانشان، تغییرات در ساختار سلول ناشی از عفونت، احتمالاً ترکیبی از این دو استراتژی را شامل میشود.[۲]
استفاده در تشخیص
[ویرایش]وجود ویروپلاسمها برای تشخیص برخی عفونتهای ویروسی استفاده میشود. درک پدیدههای تجمع ویروس و پاسخ سلولی به حضور ویروس، و نقش آنها در تکثیر ویروس یا مهار آن، ممکن است به توسعه رویکردهای درمانی جدید علیه عفونتهای ویروسی در سلولهای حیوانی و گیاهی کمک کند.[۳]
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ ۱٫۰ ۱٫۱ ۱٫۲ ۱٫۳ Netherton C, Moffat K, Brooks E, Wileman T (2007). "A guide to viral inclusions, membrane rearrangements, factories, and viroplasm produced during virus replication". Advances in Virus Research. 70: 101–82. doi:10.1016/S0065-3527(07)70004-0. ISBN 978-0-12-373728-1. PMC 7112299. PMID 17765705.
- ↑ ۲٫۰۰ ۲٫۰۱ ۲٫۰۲ ۲٫۰۳ ۲٫۰۴ ۲٫۰۵ ۲٫۰۶ ۲٫۰۷ ۲٫۰۸ ۲٫۰۹ ۲٫۱۰ ۲٫۱۱ ۲٫۱۲ ۲٫۱۳ Novoa RR, Calderita G, Arranz R, Fontana J, Granzow H, Risco C (February 2005). "Virus factories: associations of cell organelles for viral replication and morphogenesis". Biology of the Cell. 97 (2): 147–72. doi:10.1042/bc20040058. PMC 7161905. PMID 15656780.
- ↑ ۳٫۰ ۳٫۱ ۳٫۲ ۳٫۳ ۳٫۴ Moshe A, Gorovits R (October 2012). "Virus-induced aggregates in infected cells". Viruses. 4 (10): 2218–32. doi:10.3390/v4102218. PMC 3497049. PMID 23202461.
- ↑ Shalla TA, Shepherd RJ, Petersen LJ (April 1980). "Comparative cytology of nine isolates of cauliflower mosaic virus". Virology. 102 (2): 381–8. doi:10.1016/0042-6822(80)90105-1. PMID 18631647.
- ↑ Suzan-Monti M, La Scola B, Barrassi L, Espinosa L, Raoult D (March 2007). "Ultrastructural characterization of the giant volcano-like virus factory of Acanthamoeba polyphaga Mimivirus". PLOS ONE. 2 (3): e328. Bibcode:2007PLoSO...2..328S. doi:10.1371/journal.pone.0000328. PMC 1828621. PMID 17389919.

- ↑ Wileman T (May 2006). "Aggresomes and autophagy generate sites for virus replication". Science. 312 (5775): 875–8. Bibcode:2006Sci...312..875W. doi:10.1126/science.1126766. PMID 16690857.
- ↑ ۷٫۰ ۷٫۱ ۷٫۲ Bak A. , Gargani D. , Macia J-L. , Malouvet E. , Vernerey M_S. , Blanc S. and Drucker, M. Virus factories of Cauliflower mosaic virus are virion reservoirs that engage actively in vector-transmission. 2013 journal of Virology
- ↑ Xiong C, Muller S, Lebeurier G, Hirth L (1982). "Identification by immunoprecipitation of cauliflower mosaic virus in vitro major translation product with a specific serum against viroplasm protein". The EMBO Journal. 1 (8): 971–6. doi:10.1002/j.1460-2075.1982.tb01280.x. PMC 553144. PMID 16453427.
- ↑ Nilsson M, von Bonsdorff CH, Weclewicz K, Cohen J, Svensson L (March 1998). "Assembly of viroplasm and virus-like particles of rotavirus by a Semliki Forest virus replicon". Virology. 242 (2): 255–65. doi:10.1006/viro.1997.8987. PMID 9514960.
- ↑ Szajner P, Weisberg AS, Wolffe EJ, Moss B (July 2001). "Vaccinia virus A30L protein is required for association of viral membranes with dense viroplasm to form immature virions". Journal of Virology. 75 (13): 5752–61. doi:10.1128/JVI.75.13.5752-5761.2001. PMC 114291. PMID 11390577.
- ↑ Wei T, Kikuchi A, Suzuki N, Shimizu T, Hagiwara K, Chen H, Omura T (September 2006). "Pns4 of rice dwarf virus is a phosphoprotein, is localized around the viroplasm matrix, and forms minitubules". Archives of Virology. 151 (9): 1701–12. doi:10.1007/s00705-006-0757-4. PMID 16609816.
- ↑ Sodeik, B; Doms, RW; Ericsson, M; Hiller, X; Hilaler, G; Machamer, CE (May 1993). "Assembly of vaccinia virus: role of the intermediate compartment between the endoplasmic reticulum and the Golgi stacks". The Journal of Cell Biology. 121 (3): 521–41. CiteSeerX 10.1.1.274.2733. doi:10.1083/jcb.121.3.521. PMC 2119557. PMID 8486734.
- ↑ Kopito RR (December 2000). "Aggresomes, inclusion bodies and protein aggregation". Trends in Cell Biology. 10 (12): 524–30. doi:10.1016/s0962-8924(00)01852-3. PMID 11121744.

