لیتیم سیانید
| لیتیم سیانید[۱][۲][۳] | |||
|---|---|---|---|
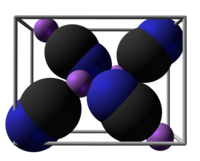
| |||
| |||
| شناساگرها | |||
| شماره ثبت سیایاس | 2408-36-8 | ||
| پابکم | 75478 | ||
| کماسپایدر | 68007 | ||
| شمارهٔ یواِن | 1935 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| خصوصیات | |||
| فرمول مولکولی | LiCN | ||
| جرم مولی | 32.959 g/mol | ||
| شکل ظاهری | پودر سفید | ||
| چگالی | 1.073 g/cm3 (18 °C) | ||
| دمای ذوب | ۱۶۰ درجه سلسیوس (۳۲۰ درجه فارنهایت؛ ۴۳۳ کلوین) Dark colored | ||
| دمای جوش | N/A | ||
| انحلالپذیری در آب | انحلال پذیر | ||
| kH | N/A | ||
| ساختار | |||
| ساختار بلوری | - | ||
| Fourfold | |||
| خطرات | |||
| طبقهبندی ئییو | T+, Very Toxic N, Dangerous for the environment | ||
| کدهای ایمنی | 26/27/28-32-50/53 | ||
| شمارههای نگهداری | 7-28-29-45-60-61 | ||
| لوزی آتش | |||
| نقطه اشتعال | |||
| دمای خودآتشگیری | |||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| Infobox references | |||
|
| |||
لیتیم سیانید یک ترکیب معدنی با فرمول شیمیایی LiCN است. این ماده یک نمک سمی، سفید رنگ، نمناک و محلول در آب است که فقط کاربردهای زیبایی دارد.
تولید[ویرایش]
لیتیم سیانید از واکنش میان لیتیم هیدروکسید و هیدروژن سیانید به دست میآید. برای انجام ابن واکنش در مقیاس آزمایشگاهی از استون سیانوهیدرین به عنوان جایگزین HCN استفاده میکنند:[۴]
- (CH 3) 2 C (OH) CN + LIH → (CH 3) 2 CO + LiCN + H 2
کاربرد[ویرایش]
اگر این ماده تا دمای نزدیک به ۶۰۰ درجه سانتیگراد گرم شود، به سیانامید و کربن تجزیه میشود. اسیدها واکنش میدهند و هیدروژن سیانید تشکیل میدهند.[۵]
از لیتیم سیانید میتوان به عنوان شناساگر برای سیانودار کردن ترکیبات آلی بهره برد.[۶]
- RX + LiCN → RCN
منابع[ویرایش]
- ↑ J. A. Lely, J. M. Bijvoet (1942), "The Crystal Structure of Lithium Cyanide", Recueil des Travaux Chimiques des Pays-Bas, vol. 61, London: WILEY-VCH Verlag, doi:10.1002/recl.19420610402
- ↑ Haynes, W.M (2013), "Bernard Lewis", in Bruno, Thomas. (ed.), Handbook of Chemistry and Physics (93 ed.), Boca Raton, Florida: Fitzroy Dearborn, archived from the original on 24 July 2017, retrieved 10 April 2021
- ↑ Material Safety Data Sheet: Lithium Cyanide, 0.5M Solution in N,N-Dimethylformamide, Fisher Scientific, 16 June 1999
- ↑ Tom Livinghouse (1981). "Trimethylsilyl Cyanide: Cyanosilylation of p-Benzoquinone". Org. Synth. 60: 126. doi:10.15227/orgsyn.060.0126.
- ↑ "Kirk-Othmer Encyclopedia of Chemical Technology". Kirk‐Othmer Encyclopedia of Chemical Technology. Wiley-VCH. 2010. doi:10.1002/0471238961.0325011416051903.a01.pub2. ISBN 978-0471238966.
- ↑ Harusawa, Shinya; Yoneda, Ryuji; Omori, Yukie; Kurihara, Takushi (1987). "Non-aqueous cyanation of halides using lithium cyanide". Tetrahedron Letters. Elsevier. 28 (36): 4189–4190. doi:10.1016/S0040-4039(00)95575-8.



