نوسینرسن
 | |
| دادههای بالینی | |
|---|---|
| نامهای تجاری | Spinraza |
| نامهای دیگر | IONIS-SMNRx, ISIS-SMNRx |
| دادهها | |
| کد ATC |
|
| وضعیت قانونی | |
| وضعیت قانونی |
|
| دادههای فارماکوکینتیک | |
| متابولیسم | هیدرولیز از طریق (۳’- و ۵’) اگزونوکلئاز |
| نیمهعمر حذف | ۱۳۵ تا ۱۷۷ روز (در مایع مغزی-نخاعی)، ۶۳ تا ۸۷ روز (در پلاسما) |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| دراگبنک | |
| کماسپایدر | |
| UNII | |
| KEGG | |
| دادههای فیزیکی و شیمیایی | |
| فرمول شیمیایی | C234H323N61Na17O128P17S17[۲] |
| جرم مولی | 7501 Da[۲] g·mol−1 |
| مدل سه بعدی (جیمول) | |
| |
نوسینـِرسن (انگلیسی: Nusinersen)[۱] با نامِ تجاریِ اسپینرازا (انگلیسی: Spinraza)[۳] نام دارویی است که برای درمانِ بیماریِ نادرِ آتروفی عضلانی نخاعی (SMA)[۴] بهکار میرود.
این دارو در دسامبر ۲۰۱۶ توسط «سازمان غذا و دارو آمریکا» و در مه ۲۰۱۷ توسط «آژانس دارویی اروپا» بهعنوان نخستین دارویِ درمانِ این بیماری، مورد تأیید واقع شد[۵][۶] و سپس در کشورهای دیگری همچون کانادا (ژوئیه ۲۰۱۷)،[۷] ژاپن (ژوئیه ۲۰۱۷)،[۸] برزیل (اوت ۲۰۱۷)[۹] و سوئیس (سپتامبر ۲۰۱۷)[۱۰] نیز مورد پذیرش قرار گرفت.
مصارف دارویی[ویرایش]
این دارو در درمانِ بیماریِ آتروفی عضلانی نخاعی ناشی از جهش ژن SMN1 بکار میرود و نحوهٔ تجویز آن، تزریقِ مستقیم بهدرونِ مجرای نخاعی است.[۲] در کارآزماییهای بالینی، این دارو پیشرفت بیماری را متوقف نموده و در حدود ۶۰٪ از نوزادان مبتلا به نوع ۱ بیماری، عملکرد سلولهای عصبی حرکتی را بهصورت فاحشی بهبود بخشید.[۲]
عوارض جانبی[ویرایش]
همچون سایر داروهای آنتیسِـنس (ژندرمانی)، احتمال لختهشدن خون، ترومبوسیتوپنی و آسیب کلیوی وجود دارد.[۲]
در کارآزماییهای بالینی انجامشده، افرادی که تحت درمان با این دارو بودند، خطر و احتمالِ بیشتری برای ابتلا به عفونتهای دستگاه تنفسی فوقانی و تحتانی، احتقان، عفونت گوش، یبوست، آسپیراسیون ریوی، دنداندرآوردنِ نامعمول و کژپشتی داشتند. یکی از نوزادان، افتِ شدید نمک و تعدادی دیگر راش پوستی پیدا کردند. همچنین احتمال کاهش یا اختلال رشد در نوزادان و کودکان وجود دارد. کارآزماییهای بالینی قدیمیتر، شایعترین عوارض این دارو را بهصورت سردرد، دردِ پشت و عوارض ناشی از پونکسیون کمری گزارش شدهاست.[۲]
برخی از افراد ممکن است علیه دارو پادتن بسازند. تا به امروز (دسامبر ۲۰۱۶) مشخص نشدهاست که این مسئله، چه تأثیری بر روی عملکرد دارو و بیخطری آن خواهد گذاشت.[۲]
فارماکولوژی[ویرایش]
بیماری آتروفی عضلانی نخاعی در اثرِ جهشِ ژنی، از نوعِ «جهش کارکردزُدا» (Loss-of-Function mutation) در ژن SMN1 ایجاد می شود. کارِ این ژن آن است که ساخته شدن نوعی پروتئین به نام پروتئینِ بقای سلول عصبی حرکتی (SMN) را کُد میکند. علت اینکه جنین زنده میماند آن است که هنوز ژن SMN2 باعث میشود مقدار اندکی از این پروتئین حیاتی ساخته شود. داروی نوسینِـرسن کارش این است که در ساختار SMN2 از طریق فرایند «پیرایش دگرسان» (Alternate Splicing)، تغییراتی میدهد و آنرا تبدیل به SMN1 میکند و بدین ترتیب، مجدداً سطح پروتئین حیاتیِ SMN در دستگاه عصبی مرکزی، بالا میرود.[۱۱]
نوسینرسن هم در دستگاه عصبی مرکزی و هم در بافتهای محیطی پخش میشود.[۲]
نیمهعمر دارو در حدود ۱۳۵ تا ۱۷۷ روز در مایع مغزی-نخاعی و ۶۳ تا ۸۷ روز در پلاسمای خون است. متابولیسم دارو از طریق هیدرولیز وابسته به (۳’- و ۵’) اگزونوکلئاز انجام میشود و تداخلی با سیتوکروم پی ۴۵۰ ندارد. راه اصلی دفع دارو و متابولیتهایش از بدن، احتمالاً از طریق ادرار است.[۲]
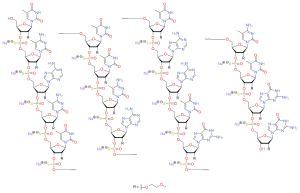
ساختار شیمیایی[ویرایش]
نوسینرسن یک «اولیگونوکلئوتید آنتیسنس» است که در آن، گروهِ ۲’-هیدروکسیِ حلقهٔ ریبوفورانوزیل، با عامل ۲’-اکسیژن-۲-متوکسیاتیل جایگزین شده و پیوندهای فسفات نیز جایشان را به پیوندهای تیوفسفات دادهاند.[۲][۱۱]
جامعه و فرهنگ[ویرایش]
بهای هر آمپول اسپینرازا در آمریکا ۱۲۵٬۰۰۰ دلار آمریکا است و هزینه درمان در سال اول ۷۵۰٬۰۰۰ دلار آمریکا و در سالهای بعدی ۳۷۵٬۰۰۰ دلار آمریکا است. طبق گزارش نیویورک تایمز، اسپینرازا یکی از گرانترین داروهای جهان است.[۱۲]
تا اکتبر ۲۰۱۷ میلادی، این دارو در ایالات متحده آمریکا، فرانسه (فقط برای نوع ۱ و ۲ بیماری)، آلمان (تمامی انواع)، ایسلند (تمامی انواع)، ایتالیا (تمامی انواع) و ژاپن (فقط نوع ۱ بیماری) تحت پوشش بیمه بودهاست.[۳]
در اکتبر ۲۰۱۷ میلادی، مقامات مسئول در دانمارک این دارو را فقط برای عدهٔ معدودی از مبتلایان به نوع ۱ بیماری (نوزادان) توصیه کردند و از پذیرش آن به عنوان داروی استانداردِ درمانی در همهٔ انواع این بیماری، سر باز زدند، چرا که قیمت نامعقول آنرا در مقایسه با اثرات بالینی بدستآمده، زیاد میدانند.[۱۳]
تا ماه مه ۲۰۱۹ میلادی، نوسینرسن در ۴۰ کشور جهان جزء بیمهٔ خدمات درمانی همگانی است.[۱۴]
منابع[ویرایش]
- ↑ ۱٫۰ ۱٫۱ "International Nonproprietary Names for Pharmaceutical Substances (INN). Recommended International Nonproprietary Names: List 74" (PDF). World Health Organization. pp. 413–14. Retrieved 13 March 2017.
- ↑ ۲٫۰۰ ۲٫۰۱ ۲٫۰۲ ۲٫۰۳ ۲٫۰۴ ۲٫۰۵ ۲٫۰۶ ۲٫۰۷ ۲٫۰۸ ۲٫۰۹ "Nusinersen US Label" (PDF). FDA. December 2016. For updates see FDA index page for NDA 209531
- ↑ ۳٫۰ ۳٫۱ "Nusinersen". AdisInsight. Retrieved 1 January 2017.
- ↑ Ottesen, Eric W. (2017-01-01). "ISS-N1 makes the first FDA-approved drug for spinal muscular atrophy". Translational Neuroscience (به انگلیسی). 8 (1): 1–6. doi:10.1515/tnsci-2017-0001. ISSN 2081-6936. PMC 5382937. PMID 28400976.
- ↑ Grant, Charley (2016-12-27). "Surprise Drug Approval Is Holiday Gift for Biogen". Wall Street Journal. ISSN 0099-9660. Retrieved 2016-12-27.
- ↑ "Spinraza (nusinersen)". European Medicines Agency. Archived from the original on 28 اكتبر 2017. Retrieved 2017-10-27.
{{cite web}}: Check date values in:|archive-date=(help) - ↑ "Biogen's SPINRAZA™ (nusinersen) Receives Notice of Compliance from Health Canada for the Treatment of 5q Spinal Muscular Atrophy (SMA)". Cision. 2017-07-04. Archived from the original on 4 December 2017. Retrieved 3 December 2017.
- ↑ "Biogen to launch Spinraza in Japan soon". 2017-07-10.
- ↑ "Remédio inédito para atrofia muscular espinhal é liberado" (به پرتغالی). 2017-08-25.
- ↑ "Spinraza – Zulassung nun auch in der Schweiz" (به آلمانی). SMA Schweiz. 2017-09-30.
- ↑ ۱۱٫۰ ۱۱٫۱ Zanetta, C; Nizzardo, M; Simone, C; Monguzzi, E; Bresolin, N; Comi, GP; Corti, S (1 January 2014). "Molecular Therapeutic Strategies for Spinal Muscular Atrophies: Current and Future Clinical Trials". Clinical Therapeutics. 36 (1): 128–40. doi:10.1016/j.clinthera.2013.11.006. PMID 24360800.
- ↑ Katie Thomas (December 30, 2016). "Costly Drug for Fatal Muscular Disease Wins F.D.A. Approval". New York Times.
- ↑ Medicinrådet siger nej til lægemiddel til børn med muskelsvind: 'Urimeligt' dyrt Retrieved October 13 2017.
- ↑ "Spinraza access by country". TreatSMA (به انگلیسی). Retrieved 2019-05-28.
- مشارکتکنندگان ویکیپدیا. «Nusinersen». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۳ دسامبر ۲۰۱۷.
بیشتر بخوانید[ویرایش]
- Finkel, Richard S; Chiriboga, Claudia A; Vajsar, Jiri; Day, John W; Montes, Jacqueline; De Vivo, Darryl C; Yamashita, Mason; Rigo, Frank; Hung, Gene; Schneider, Eugene; Norris, Daniel A; Xia, Shuting; Bennett, C Frank; Bishop, Kathie M (2016). "Treatment of infantile-onset spinal muscular atrophy with nusinersen: A phase 2, open-label, dose-escalation study". The Lancet. 388 (10063): 3017. doi:10.1016/S0140-6736(16)31408-8.
