برقکافت آب
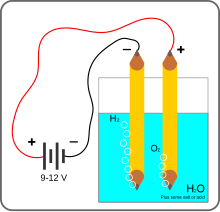
برقکافت آب یا الکترولیز آب (به انگلیسی: Electrolysis of water) فرایندی متداول جهت تجزیه آب به عناصر سازنده آن یعنی اکسیژن و هیدروژن است که در آن از یک جریان الکتریکی مستقیم و دو الکترود بهره گرفته میشود. از منبع جریان برق DC برای دو الکترود یا صفحه فلزی (از فلزات نجیب نظیر پلاتین یا ایریدیم) استفاده میشود که هر دو الکترود وارد آب میشوند و از آنجا که آب خالص رسانایی ناچیز و هدایت جریان الکتریکی یک میلیونیم آب دریا دارد باید مقداری الکترولیت (اسید، باز یا نمک فلزی) اضافه شود. در مجاورت الکترود آند آب اکسایش میابد و سبب تولید اکسیژن، پروتون و الکترون میشود که گازهای اکسیژن تولید شده بصورت حباب از ظرف نیم واکنش آندی خارج میشود و الکترونهای تولید از طریق الکترود آندی به بخش الکترود کاتدی حرکت میکند و یونهای هیدروژن ایجاد شده از طریق غشای مبادله کننده پروتون به بخش الکترود کاتدی میروند و با الکترونهای موجود سبب کاهش هیدروژن و تولید حبابهای هیدروژن میشود.
فرایند برقکافت نیاز به حرارت و الکتریسیته دارد و لذا در چندین حالت دما بالا، فشار بالا و غیره انجام میشود. برقکافت بخار که در دمای بالا انجام میشود، به منظور کاهش میزان الکتریسیته مصرفی مورد استفاده قرار میگیرد. ا[۱]
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ Daneshpour, Raheleh; Mehrpooya, Mehdi (2018-11). "Design and optimization of a combined solar thermophotovoltaic power generation and solid oxide electrolyser for hydrogen production". Energy Conversion and Management (به انگلیسی). 176: 274–286. doi:10.1016/j.enconman.2018.09.033.
{{cite journal}}: Check date values in:|date=(help)
- "Electrolysis of Water". Experiments on Electrochemistry. Archived from the original on 20 December 2004. Retrieved November 20, 2005.
- "Electrolysis of Water". Do Chem 044. Archived from the original on 14 March 2006. Retrieved November 20, 2005.
- EERE 2008 - 100 kgH2/day Trade Study
- NREL 2006 - Electrolysis technical report
