دیمتیلکادمیوم
| دیمتیلکادمیوم | |
|---|---|
| |
| شناساگرها | |
| شماره ثبت سیایاس | ۵۰۶-۸۲-۱ |
| پابکم | ۱۰۴۷۹ |
| کماسپایدر | ۱۰۲۵۴۴۷۶ |
| UNII | 0T3G3H597H |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | C2H6Cd۱ |
| جرم مولی | ۱۴۲٫۴۸ g mol−1 |
| شکل ظاهری | مایع بیرنگ |
| بوی | بسیار بدبو؛ ناخوشایند؛ فلزی؛ نامطلوب |
| چگالی | 1.985 گرم بر میلیلیتر |
| دمای ذوب | −۴٫۵ درجه سلسیوس (۲۳٫۹ درجه فارنهایت؛ ۲۶۸٫۶ کلوین) |
| دمای جوش | ۱۰۶ درجه سلسیوس (۲۲۳ درجه فارنهایت؛ ۳۷۹ کلوین) |
| انحلالپذیری در آب | با آب واکنش نشان میدهد. |
| خطرات | |
| GHS pictograms |   
|
| سیستم هماهنگ جهانی طبقهبندی و برچسبگذاری مواد شیمیایی | خطرناک |
| GHS hazard statements | H225, H250, H252, H260, H301, H330, H350, H360 |
| GHS precautionary statements | P101, P102, P103, P231, P222, P301+310, P303+361+353, P305+351+338, P403+233, P422, P501 |
| خطرات اصلی | بسیار سمی است، با آب واکنش میدهد و متان آزاد میکند. |
| لوزی آتش | |
| نقطه اشتعال | |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| Infobox references | |
|
| |
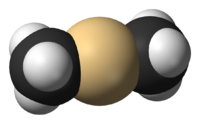
دیمتیلکادمیوم (انگلیسی: Dimethylcadmium) یک ترکیب آلی کادمیوم با فرمول Cd(CH3)2 است. دیمتیلکادمیوم یک مایع بیرنگ و بسیار سمی است که در هوا بخار میشود. این ماده یک مولکول خطی است که طول پیوند C-Cd آن ۲۱۳ پیکومتر است.[۱] این ترکیب استفاده محدودی به عنوان یک واکنشگر در سنتز آلی و در برآرایی بخار فلز-آلی (MOCVD) دارد. از این ترکیب شیمیایی همچنین در سنتز نانوذرات کادمیم سلنید استفاده شدهاست، اگرچه شیمیدانان تلاش کردهاند تا به دلیل سمی بودن این مولکول، از مادهٔ دیگری برای این استفاده بهخصوص استفاده کنند.[۲]
دیمتیلکادمیوم از طریق پردازش مولکول کادمیوم دیهیالید با واکنشگر گرینیارد متیل یا متیللیتیم ساخته میشود:[۳]
- CdBr
2 + 2 CH
3MgBr → Cd(CH
3)
2 + 2 MgBr
2
از همین روش، نخستین بار برای تولید این ترکیب استفاده شد.[۴]
دیمتیلکادمیوم یک اسید لوئیس ضعیف است که با دیاتیل اتر یک ترکیب اضافی فرار ایجاد میکند. یک ترکیب اضافی زرد و حساس به هوا نیز با ۲٬۲'-بی پیریدین تشکیل میشود.[۳]
منابع
[ویرایش]- ↑ Felix Hanke; Sarah Hindley; Anthony C. Jones; Alexander Steiner (2016). "The Solid State Structures of the High and Low Temperature Phases of Dimethylcadmium". Chemical Communications. 52 (66): 10144–10146. doi:10.1039/c6cc05851e. PMID 27457504.
- ↑ Julia Hambrock; Alexander Birkner; Roland A. Fischer (2001). "Synthesis of CdSe nanoparticles using various organometallic cadmium precursors". Journal of Materials Chemistry. 11 (12): 3197–3201. doi:10.1039/B104231A.
- ↑ ۳٫۰ ۳٫۱ Douglas F. Foster; David J. Cole-Hamilton (1997). "Electronic Grade Alkyls of Group 12 and 13 Elements". Inorganic Syntheses. Vol. 31. pp. 21–66. doi:10.1002/9780470132623.ch7. ISBN 9780470132623.
- ↑ Erich Krause (1917). "Einfache Cadmiumdialkyle (I. Mitteilung über organische Cadmium-Verbindungen)". Berichte der deutschen chemischen Gesellschaft. 50 (2): 1813–1822. doi:10.1002/cber.19170500292.

