دیهیدروکسیلدار کردن نامتقارن شارپلس
| دیهیدروکسیلدار کردن نامتقارن شارپلس | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| نامگذاری شده پس از | کارل شارپلس | ||||||||||
| نوع واکنش | واکنش افزایشی | ||||||||||
| Reaction | |||||||||||
| |||||||||||
| شناسهها | |||||||||||
| در درگاه شیمی آلی | sharpless-dihydroxylation | ||||||||||
| RSC ontology ID | RXNO:0000142 | ||||||||||
دیهیدروکسیلاسیون یا دیهیدروکسیلدار کردن نامتقارن شارپلس (به انگلیسی: Sharpless asymmetric dihydroxylation) (همچنین با نام بیهیدروکسیلاسیون شارپلس نیز شناخته میشود) واکنش شیمیایی یک آلکن با اسمیم تتراکسید در حضور یک لیگاند کینین کایرال برای تشکیل یک دیال مجاور است. این واکنش برای آلکنهای دارای هر استخلافی انجام پذیر است، اغلب انانتیوگزینی بالایی در آن مشاهده میشود، با انتخاب دیهیدروکینیدین (DHQD) در مقابل دیهیدروکینین (DHQ) به عنوان لیگاند، کایرالیته محصول نهایی کنترل میشود. واکنشهای دیهیدروکسیلدار کردن نامتقارن نیز بسیار مکانگزین هستند و محصولات حاصل از واکنش پیوند دوگانه غنی از الکترون در بستر را فراهم میکنند.[۱][۲][۳]
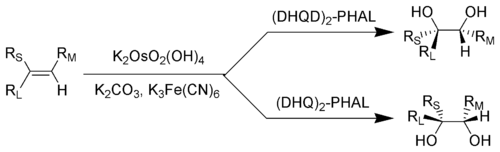
R L = بزرگترین استخلاف. R M = استخلاف با اندازه متوسط. R S = کوچکترین استخلاف
انجام این واکنش با استفاده از مقدار کاتالیزوری از اسمیم تتراکسید معمول است که پس از واکنش با بازاکسندههایی مانند پتاسیم فریسیانید[۴][۵] یا N-متیلمورفولین N-اکسید بازسازی میشود.[۶][۷] این عمل بهطور چشمگیری مقدار اسمیم تتراکسید مورد نیاز را که ماده ای بسیار سمی و گران است، کاهش میدهد. این چهار واکنشگر به صورت پیش مخلوط (مخلوط-AD) در دسترس هستند. مخلوط حاوی (DHQ)2-PHAL را محلوط AD آلفا و مخلوط حاوی (DHQD)2-PHAL را مخلوط AD بتا مینامند.[۸]
محصولات این واکنش که دیالهای کایرال هستند، در سنتز آلی اهمیت بالایی دارند. ایجاد ویژگی کایرالیته به واکنش دهندههای غیرکایرال از طریق استفاده از کاتالیزورهای کایرال یک مفهوم مهم در سنتز آلی است. این واکنش نخستین بار توسط کارل بری شارپلس و با توسعه واکنش دیهیدروکسیلدار کردن راسمیک آپجان که از قبل شناخته شده بود، معرفی شد. وی به خاطر این کشف سهمی از جایزه نوبل شیمی در سال ۲۰۰۱ را دریافت کرد.
برای مطالعهٔ بیشتر
[ویرایش]- Jacobsen, E. N.; Marko, I.; Mungall, W. S.; Schroeder, G.; Sharpless, K. B. (1988). "Asymmetric dihydroxylation via ligand-accelerated catalysis". J. Am. Chem. Soc. 110 (6): 1968–1970. doi:10.1021/ja00214a053.
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ Noe, Mark C.; Letavic, Michael A.; Snow, Sheri L. (15 December 2005). "Asymmetric Dihydroxylation of Alkenes". Org. React. 66 (109): 109–625. doi:10.1002/0471264180.or066.02. ISBN 0-471-26418-0.
- ↑ Kolb, H. C.; Van Nieuwenhze, M. S.; Sharpless, K. B. (1994). "Catalytic Asymmetric Dihydroxylation". Chem. Rev. 94 (8): 2483–2547. doi:10.1021/cr00032a009.
- ↑ Gonzalez, Javier; Aurigemma, Christine; Truesdale, Larry (2004), "Synthesis of (+)-(1S,2R)- and (−)-(1R,2S)-trans-2-Phenylcyclohexanol Via Sharpless Asymmetric Dihydroxylation (AD)", Org. Synth., 79: 93, doi:10.15227/orgsyn.079.0093
- ↑ Minato, M.; Yamamoto, K.; Tsuji, J. (1990). "Osmium tetraoxide catalyzed vicinal hydroxylation of higher olefins by using hexacyanoferrate(III) ion as a cooxidant". J. Org. Chem. 55 (2): 766–768. doi:10.1021/jo00289a066.
- ↑ Oi, R.; Sharpless, K. B. (1996), "3-[(1S)-1,2-Dihydroxyethyl]-1,5-Dihydro-3H-2,4-Benzodioxepine", Org. Synth., 73: 1, doi:10.15227/orgsyn.073.0001; Coll. Vol., 9: 251
{{citation}}: Missing or empty|title=(help) - ↑ VanRheenen, V.; Kelly, R. C.; Cha, D. Y. (1976). "An improved catalytic OsO4 oxidation of olefins to cis-1,2-glycols using tertiary amine oxides as the oxidant". Tetrahedron Lett. 17 (23): 1973–1976. doi:10.1016/s0040-4039(00)78093-2.
- ↑ McKee, B. H.; Gilheany, D. G.; Sharpless, K. B. (1992), "(R,R)-1,2-Diphenyl-1,2-ethanediol (Stilbene diol)", Org. Synth., 70: 47, doi:10.15227/orgsyn.070.0047; Coll. Vol., 9: 383
{{citation}}: Missing or empty|title=(help) - ↑ Sharpless, K. B.; Amberg, Willi; Bennani, Youssef L.; Crispino, Gerard A.; Hartung, Jens; Jeong, Kyu Sung; Kwong, Hoi Lun; Morikawa, Kouhei; Wang, Zhi Min (1992). "The osmium-catalyzed asymmetric dihydroxylation: A new ligand class and a process improvement". J. Org. Chem. 57 (10): 2768–2771. doi:10.1021/jo00036a003.
{{cite journal}}: Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help)
