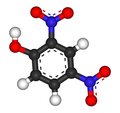
۴٬۲-دینیتروفنول
| ۴٬۲-دینیتروفنول | |||
|---|---|---|---|
| |||
24-dinitrophenol | |||
دیگر نامها Solfo Black | |||
| شناساگرها | |||
| شماره ثبت سیایاس | 51-28-5 | ||
| پابکم | 1493 | ||
| کماسپایدر | 1448 | ||
| UNII | Q13SKS21MN | ||
| شمارهٔ یواِن | 0076 1320 | ||
| دراگبانک | DB04528 | ||
| KEGG | C02496 | ||
| ChEBI | CHEBI:42017 | ||
| ChEMBL | CHEMBL273386 | ||
| جیمول-تصاویر سه بعدی | Image 1 Image 2 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | C6H4N2O5 | ||
| جرم مولی | 184.106 | ||
| چگالی | 1.683 g/cm³ | ||
| دمای ذوب | ۱۰۸ درجه سلسیوس (۲۲۶ درجه فارنهایت؛ ۳۸۱ کلوین) | ||
| دمای جوش | ۱۱۳ درجه سلسیوس (۲۳۵ درجه فارنهایت؛ ۳۸۶ کلوین) | ||
| اسیدی (pKa) | 4.114 | ||
| خطرات | |||
| کدهای ایمنی | R۱۰ R۲۳ R۲۴ R۲۵ R33 | ||
| شمارههای نگهداری | S۱ S۲ S۲۸ S۳۷ S45 | ||
| لوزی آتش | |||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
۴،۲-دینیتروفنول (به انگلیسی: 2,4-Dinitrophenol) با فرمول شیمیایی C6H4N2O5 یک ترکیب شیمیایی با شناسه پابکم 1493 است. که جرم مولی آن 184.106 میباشد.این ماده جامد زرد رنگ و کریستالی است که بوی شیرین و کپک زدگی دارد. تصعید میشود، با بخار فرار است و در اکثر حلالهای آلی و همچنین محلولهای قلیایی آبی محلول است.[1] هنگامی که به شکل خشک است، دارای قابلیت انفجار شدید است و خطر انفجار آنی دارد.[2] این ماده پیش ساز سایر مواد شیمیایی است و از نظر بیوشیمیایی فعال است و فسفوریلاسیون اکسیداتیو را از زنجیره انتقال الکترون در سلول های دارای میتوکندری جدا می کند و به کاتیون های هیدروژن اجازه می دهد از فضای بین غشایی به ماتریکس میتوکندری عبور کنند. فسفوریلاسیون اکسیداتیو یک مرحله بسیار تنظیمشده در تنفس هوازی است که از جمله عوامل دیگر، توسط سطوح طبیعی سلولی ATP مهار میشود. جدا کردن آن منجر به هدر رفتن انرژی شیمیایی از رژیم غذایی و ذخایر انرژی مانند تری گلیسیرید به عنوان گرما با حداقل تنظیم می شود و منجر به دمای بدن به طور خطرناکی می شود که ممکن است به گرمازدگی تبدیل شود. استفاده از آن به عنوان یک کمک رژیم غذایی با عوارض جانبی شدید، از جمله تعدادی مرگ و میر شناخته شده است.
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- «IUPAC GOLD BOOK». دریافتشده در ۱۸ مارس ۲۰۱۲.