معادله هامت
معادله هامت (به انگلیسی: Hammet Equation) ، رابطهای در شیمیفیزیک آلی است که سرعت واکنش و ثابت تعادل در نوع مشخصی از واکنشهای آلی را به هم مرتبط میسازد.
لوییس هامت[ویرایش]
مطالعات محققی به نام لوییس هامت (۱۸۹۴-۱۹۸۷) نشان داد که بین ویژگی های الکترونی اسیدها و بازهای آلی با ثابت های تعادل و واکنشپذیری آنها ارتباط مستقیمی وجود دارد.
تشریح معادله[ویرایش]
معادله به صورت زیر است:
در اینجا K ثابت تعادل، K0 ثابت تعادل برای اتم هیدروژن (مرجع)، ρ ثابت واکنش و σ ثابت جانشینی است. در مواردی که گروه استخلافی ، ویژگی الکترونکشندگی دارد، مثل گروه نیترو، ثابت تعادل افزایش پیدا می کند و بسته به موقعیتی که این گروه جانشین شده روی حلقه آروماتیک انتخاب می کند - متا یا پارا - این اختلاف بیشتر می شود.
در موردی که گروه استخلافی الکتروندهنده مثل اتیل به حلقه آروماتیک متصل شده است ثابت تعادل کاهش پیدا کرده است.
استخلافهای گوناگون[ویرایش]
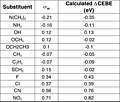
مقدار ثابت جانشینی برای گروههای استخلافی گوناگون:
| گروه جانشینشونده | اثر پارا | اثر متا |
|---|---|---|
| دیمتیلآمین | -۰٫۸۳ | -۰٫۲۱۱ |
| آمینو | -۰٫۶۶ | -۰٫۱۶۱ |
| متوکسی | -۰٫۲۶۸ | +۰٫۱۱۵ |
| اتوکسی | -۰٫۲۵ | +۰٫۰۱۵ |
| متیل | -۰٫۱۷۰ | -۰٫۰۶۹ |
| هیچیک | ۰٫۰۰۰ | ۰٫۰۰۰ |
| فلوئور | +۰٫۰۶۲ | +۰٫۳۳۷ |
| کلرو | +۰٫۲۲۷ | +۰٫۳۷۳ |
| برمو | +۰٫۲۳۲ | +۰٫۳۹۳ |
| یدو | +۰٫۲۷۶ | +۰٫۳۵۳ |
| سیانو | +۰٫۶۶ | +۰٫۵۶ |
| نیترو | +۰٫۷۷۸ | +۰٫۷۱۰ |
نگارخانه[ویرایش]
منابع[ویرایش]
- ↑ Louis P. Hammett (1935). "Some Relations between Reaction Rates and Equilibrium Constants". Chem. Rev. 17 (1): 125–136. doi:10.1021/cr60056a010.