نئوپلازی دروناپیتلیومی دهانه رحم: تفاوت میان نسخهها
ایجادشده به کمک به ویکیفا و Dexbot، ابرابزار، اصلاح ارقام برچسب: جمع عربی واژگان فارسی |
(بدون تفاوت)
|
نسخهٔ ۲۷ آوریل ۲۰۲۳، ساعت ۰۳:۳۱
| نئوپلازی دروناپیتلیومی دهانه رحم | |
|---|---|
| نامهای دیگر | دیسپلازی دهانه رحم |
 | |
| نمایی از نئوپلازی دروناپیتلیومی دهانه رحم از نوع CIN-1 پس از آمادهسازی با استیک اسید | |
| تخصص | پزشکی زنان |
| طبقهبندی و منابع بیرونی | |
نئوپلازی دروناپیتلیومی دهانه رحم (انگلیسی: Cervical intraepithelial neoplasia) یا به اختصار «CIN» که به آن دیسپلازی دهانه رحم هم میگویند، رشد غیرطبیعی سلولهای سطحی دهانه رحم است که بالقوه، قابلیت تبدیل به سرطان دهانه رحم را دارد.[۱] بهطور خاص، اصطلاح CIN به تغییر شکل بالقوه پیشسرطانی سلولهای دهانه رحم اشاره دارد.
این تغییر معمولاً در محل اتصال بافت پوششی سنگفرشی واژن به بافت پوششی استوانهای آندوسرویکس (کانال ابتدایی دهانه رحم) رخ میدهد.[۲] این تغییرات همچنین میتواند در دیوارههای واژن و اپیتلیوم فرج رخ دهد. نئوپلازی دروناپیتلیومی دهانه رحم در مقیاس ۱ تا ۳ درجهبندی میشود که ۳ غیرطبیعیترین است (به بخش طبقهبندی در زیر مراجعه کنید).
وجود عفونت ویروس پاپیلوم انسانی (HPV) برای ایجاد نئوپلازی دروناپیتلیومی دهانه رحم ضروری است، اما همه مبتلایان به این عفونت، به سرطان دهانه رحم مبتلا نمیشوند.[۳] بسیاری از زنان مبتلا به عفونت ویروس پاپیلوم انسانی هرگز به CIN یا سرطان دهانه رحم مبتلا نمیشوند. بهطور معمول، عفونت ویروس پاپیلوم انسانی خودبهخود برطرف میشود.[۴] با این حال، کسانی که عفونت درازمدت ویروس پاپیلوم انسانی دارند که بیش از یک یا دو سال طول بکشد، در معرض خطر بالاتری برای ایجاد درجات بالای نئوپلازی دروناپیتلیومی دهانه رحم هستند.[۵]
همچون سایر نئوپلازیهای داخل اپیتلیال، «نئوپلازی دروناپیتلیومی دهانه رحم» هم سرطان نیست و معمولاً قابل درمان است.[۳] اکثر موارد نئوپلازی دروناپیتلیومی دهانه رحم یا بدون تغییر باقی میماند یا توسط سیستم ایمنی فرد بدون نیاز به مداخله از بین میرود. با این حال، درصد کمی از موارد در صورت عدم درمان به سرطان دهانه رحم، (معمولاً از نوعِ سرطان سلول سنگفرشی دهانه رحم یا SCC)، تبدیل میشود.[۶]
علائم و نشانهها
نئوپلازی دروناپیتلیومی دهانه رحم علائم اختصاصی و مخصوصبهخود ندارد.
بهطور کلی، علائم و نشانههای سرطان دهانه رحم عبارتند از:[۷]
- خونریزی غیرطبیعی یا بعد از یائسگی
- ترشح غیرطبیعی
- تغییرات در عملکرد مثانه یا روده
- درد لگن هنگام معاینه
- ظاهر غیرطبیعی هنگام مشاهده یا لمس دهانه رحم توسط پزشک
عفونت ویروس پاپیلوم انسانی فرج و واژن میتواند باعث زگیل تناسلی یا بدون علامت باشد.
علل
علت نئوپلازی دروناپیتلیومی دهانه رحم، عفونت مزمن دهانه رحم با ویروس پاپیلوم انسانی به خصوص عفونت با ویروسهای پاپیلوم پرخطر نوع ۱۶ یا ۱۸ است. تصور میشود که عفونتهای پرخطر ویروس پاپیلوم انسانی توانایی غیرفعال کردن ژنهای سرکوبگر تومور مانند ژن پی۵۳ و ژن RB بنابراین به سلولهای آلوده اجازه میدهد تا بدون کنترل رشد کنند و جهشهای متوالی را جمعآوری کنند و در نهایت منجر به سرطان شوند.[۱]
مشخص شدهاست که برخی از زنان در معرض خطر بیشتری برای ابتلا به نئوپلازی دروناپیتلیومی دهانه رحم هستند:[۱][۸]
- عفونت با یک انواع پرخطر HPV، مانند ۱۶، ۱۸، ۳۱، یا ۳۳
- کمبود ایمنی (مانند عفونت HIV)
- رژیم غذایی نامناسب
- شرکای جنسی متعدد
- عدم استفاده از کاندوم
- سیگار کشیدن
علاوه بر این، ثابت شده که تعدادی از عوامل خطر احتمال ابتلای فرد به نوع CIN 3 (سرطان درجا) را افزایش میدهند (پائین را ببینید):[۹]
- زنانی که قبل از ۱۷ سالگی زایمان میکنند
- زنانی که بیش از ۱ حاملگی کامل (full term) دارند
پاتوفیزیولوژی

اولین تغییر میکروسکوپی مربوط به CIN، دیسپلازی اپیتلیال یا پوشش سطحی دهانه رحم است که اساساً توسط بیمار قابل تشخیص نیست. اکثر این تغییرات در محل اتصال بافت سنگفرشی یا ناحیه دگرسانی یا تغییر بافت دهانه رحم (transformation zone) رخ میدهد، یعنی ناحیهای از بافت ناپایدار دهانه رحم که مستعد تغییرات غیرطبیعی است.[۲] تغییرات سلولی مرتبط با عفونت ویروس پاپیلوم انسانی، مانند کویلوسیتها نیز معمولاً در نئوپلازی دروناپیتلیومی دهانه رحم دیده میشود. در حالی که عفونت با ویروس پاپیلوم انسانی برای ایجاد نئوپلازی دروناپیتلیومی لازم است، اکثر زنان مبتلا به عفونت ویروس پاپیلوم انسانی به ضایعات داخل اپیتلیال درجه بالا یا سرطان مبتلا نمیشوند. ویروس پاپیلوم انسانی به تنهایی عامل ایجادکننده نیست.[۱۰]
از میان ۱۰۰ نوع مختلف از ویروس پاپیلوم انسانی، تقریباً ۴۰ نوع شناخته شدهاست که بر بافت پوششی ناحیه مقعدی-تناسلی اثر میگذارد و میزان احتمال متفاوتی برای ایجاد تغییرات بدخیم دارند.[۱۱]
تشخیص
امروزه تشخیص ویروس پاپیلوم انسانی با آزمایشی دقیق به نام «دایجین اچپیوی» (Digene HPV) انجام میشود است که هم میتواند به عنوان آزمایشی مستقل در تشخیص به کار رود و هم به عنوان روشی کمکی هنگام انجام آزمایش پاپ اسمیر که خود یک روش غربالگری است و امکان بررسی سلولها (اما نه ساختار بافتی مورد نیاز برای تشخیص) را فراهم میکند. کولپوسکوپی با بیوپسی هدفدار، روش استاندارد تشخیص این بیماری است. نمونهبرداری جاروبی آندوسرویکال در زمان پاپ اسمیر برای تشخیص آدنوکارسینوما و پیشسازهای آن همراه با آگاهی پزشک/بیمار در مورد علائم شکمی مرتبط با سرطان رحم و سرطان تخمدان ضروری است. تشخیص CIN یا کارسینوم دهانه رحم نیاز به بیوپسی برای تجزیه و تحلیل بافتشناسی دارد.
طبقهبندی

در گذشته، تغییرات غیرطبیعی سلولهای بافت پوششی دهانه رحم به صورت دیسپلازی اپیتلیال «خفیف»، «متوسط» یا «شدید» توصیف میکردند. در سال ۱۹۸۸ مؤسسه ملی سرطان «سیستم بتسدا برای گزارش تشخیصهای سلولشناسی دهانه رحم/واژن» را ایجاد کرد.[۱۲] این سیستم راهی همسان برای توصیف سلولهای اپیتلیال غیرطبیعی و تعیین کیفیت نمونه فراهم میکند، بنابراین راهنمایی روشنی برای مدیریت بالینی درمان ارائه میدهد.
این ناهنجاریها به زیرگروههای «سنگفرشی» یا «غدهای» طبقهبندی شدند و سپس براساس مرحله دیسپلازی دستهبندی شدند: سلولهای غیرطبیعی (آتیپیک)، خفیف، متوسط، شدید و کارسینوم (سرطان).[۱۳]
بسته به عوامل متعدد و محل قرارگیری ضایعه، نئوپلازی دروناپیتلیومی دهانه رحم ممکن است در هر یک از سه مرحله شروع شود و احتمال دارد پیشرفت یا پسرفت کند.[۱۴]
نئوپلازی دروناپیتلیومی دهانه رحم در درجههای زیر طبقهبندی میشود:
| درجهٔ بافتی | نمای سلولی مرتبط | توضیح | تصویر |
|---|---|---|---|
| CIN 1 (درجه ۱) | ضایعهٔ دروناپیتلیومی سنگفرشی با درجهٔ پائین (LSIL) |
|
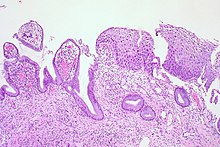
|
| CIN 2/3 (درجه ۲/۳) | ضایعهٔ دروناپیتلیومی سنگفرشی با درجهٔ بالا (HSIL) |
|
|
| CIN 2 (درجهٔ ۲) |
|
 | |
| CIN 3 (درجهٔ ۳) |
|
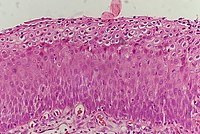 |


تغییر در اصطلاحشناسی
«کالج آسیبشناسی آمریکا» و «انجمن کولپوسکوپی و آسیبشناسی دهانه رحم آمریکا» در سال ۲۰۱۲ گرد هم آمدند تا تغییراتی را در اصطلاحات پزشکی این حوزه منتشر نموده و ضایعات سنگفرشی دستگاه تناسلی مرتبط با ویروس پاپیلوم انسانی را به صورت LSIL یا HSIL به شرح زیر توصیف کنند:[۱۶]
- CIN 1 با عنوان جدید LSIL شناخته میشود.
- CIN 2 که در اثر گونههٔ پی۱۶ نباشد (که گونهٔ پرخطر این ویروس است) LSIL نامیده میشود. آنهایی که p16 مثبت هستند، HSIL نامیده میشوند.
- CIN 3 با عنوان جدید HSIL شناخته میشود.
غربالگری
دو روش غربالگری موجود عبارتند از: پاپ اسمیر و آزمایش برای تشخیص ویروس پاپیلوم انسانی. نئوپلازی دروناپیتلیومی دهانه رحم معمولاً با آزمایش غربالگری پاپ اسمیر کشف میشود. هدف از این آزمایش تشخیص تغییرات بالقوه پیش سرطانی از طریق نمونهگیری تصادفی از ناحیهٔ دگرسانی (تغییر) بافتی (transformation zone) است. نتایج پاپ اسمیر ممکن است با استفاده از «سیستم بتسدا» گزارش شود (به بالا مراجعه کنید). حساسیت و ویژگی این آزمون در یک مرور سیستماتیک با نگاه به دقت آزمون متغیر بود. یک نتیجه غیرطبیعی پاپ اسمیر ممکن است منجر به توصیه برای انجام کولپوسکوپی دهانه رحم شود که یک روش تشخیصی در مطب است که طی آن، دهانه رحم با بزرگنمایی موضعی بهدقت بررسی میشود. بیوپسی از هر ناحیهای که ظاهر غیرطبیعی دارد، گرفته میشود.
انجام کولپوسکوپی معمولاً بسیار دردناک است و بنابراین پژوهشگران تلاش کردهاند تا از بهترین روشهای تسکین درد برای زنان مبتلا به نئوپلازی دروناپیتلیومی که کولپوسکوپی میشوند، استفاده کنند. پژوهشها نشان میدهد که در مقایسه با دارونما، تزریق یک بیحسکننده موضعی و تنگکننده عروق به دهانه رحم (دارویی که باعث باریک شدن رگهای خونی میشود) ممکن است میزان خونریزی و درد در طول کولپوسکوپی را کاهش دهد.[۱۷]
آزمایش ویروس پاپیلوم انسانی میتواند بسیاری از انواع پرخطر این ویروس را که ایجادکنندهٔ نئوپلازی دروناپیتلیومی هستند، شناسایی کند. غربالگری ویروس پاپیلوم انسانی یا به صورت آزمایشی همزمان با پاپ اسمیر انجام میشود یا میتواند پس از آزمایش پاپ اسمیر که سلولهای غیرطبیعی را نشان میدهد، انجام شود که به آن تست رفلکس میگویند. بسامد غربالگری بر اساس دستورالعملهای «انجمن اختلالات دستگاه تناسلی-تحتانی» (ASCCP) تعیین شدهاست. سازمان جهانی بهداشت همچنین دستورالعملهای غربالگری و درمانی برای ضایعات پیشسرطانی دهانه رحم و پیشگیری از بروز سرطان دهانه رحم دارد.
پیشگیری اولیه
واکسیناسیون پیشگیری از عفونت ویروس پاپیلوم انسانی رویکردی برای پیشگیری اولیه از نئوپلازی دروناپیتلیومی دهانه رحم و بروز سرطان دهانه رحم است.
| واکسن | گونهای از ویروس که هدف واکسن است | به چه کسانی تزریق میشود؟ | تعداد دوزها | بهترین زمان ایمنسازی |
|---|---|---|---|---|
| گارداسیل - چهار ظرفیتی | ۶ و ۱۱ (هامل ایجاد زگیل تناسلی) ۱۶ و ۱۸ (عامل ایجاد حدود ۷۰٪ از سرطانهای دهانه رحم)[۱۸] | پسران و دختران ۹ تا ۲۶ سال | ۳ | پیش از نخستین فعالیت جنسی یک مدت کوتاهی پس از آن |
| سرواریکس - دو ظرفیتی | ۱۶ و ۱۸ | دختران ۹ تا ۲۵ سال | ۳ | |
| گارداسیل ۹ - نُه ظرفیتی | ۶، ۱۱، ۱۶، ۱۸، ۳۱، ۳۳، ۴۵، ۵۲ و ۵۸ (عامل ایجاد حدود ۲۰٪ از سرطانهای دهانه رحم)[۱۹] | پسران و دختران ۹ تا ۲۶ سال | ۳ |
توجه به این نکته مهم است که این واکسنها در برابر تمام انواع ویروس پاپیلوم انسانی دخیل در سرطان، محافظت ایجاد نمیکنند؛ بنابراین غربالگری سرطان همچنان در افراد واکسینهشده توصیه میشود.
پیشگیری ثانویه
مدیریت مناسب با نظارت و درمان رویکردی برای پیشگیری ثانویه از سرطان دهانه رحم در افراد مبتلا به نئوپلازی دروناپیتلیومی دهانه رحم است.
مدیریت درمانی

درمان CIN 1 یا دیسپلازی خفیف، در صورتی که درگیری با آن کمتر از دو سال طول بکشد، توصیه نمیشود.[۲۰] معمولاً وقتی بیوپسی CIN 1 را گزارش میکند، زن مبتلا به عفونت ویروس پاپیلوم انسانی است که ممکن است طی ۱۲ ماه خود به خود برطرف شود؛ بنابراین، به جای درمان، با آزمایش و پایشهای متعدد بعدی، پیگیری میشود.[۲۰] در زنان جوان نظارت دقیق بر پیشرفت ضایعات CIN 2 نیز منطقی به نظر میرسد.[۶]
درمان برای CIN با درجه بالاتر (شدیدتر) شامل برداشتن یا تخریب سلولهای غیرطبیعی دهانه رحم با انجماد، الکتروکوتر (سوزاندن با جریان برق)، سوزاندن با اشعه لیزر، روش برش با جراحی الکتریکی حلقهای (LEEP)، یا مخروطبرداری دهانه رحم است. آستانه معمول برای آغاز درمان، مرحلهٔ CIN 2+ است، اگرچه ممکن است رویکرد محدودتری برای افراد جوان و زنان باردار اتخاذ شود. یک بررسی کاکرین شواهد روشنی پیدا نکرد که نشان دهد کدام روش جراحی برای درمان نئوپلازی دروناپیتلیومی بهتر است.[۲۱] شواهد علمی نشان میدهد که گرچه رتینوئیدها در جلوگیری از پیشرفت نئوپلازی دروناپیتلیومی مؤثر نیستند، اما ممکن است در ایجاد پسرفت بیماری در افراد مبتلا به CIN2 مؤثر باشند.[۲۲] واکسنهای درمانی در حال حاضر تحت آزمایشات بالینی هستند. نرخ عود مادام العمر CIN حدود ۲۰٪ است،[نیازمند منبع] اما مشخص نیست چه نسبتی از این موارد عفونتهای جدید هستند تا عود عفونت اصلی.
پژوهشهای انجام شده برای بررسی اینکه آیا آنتیبیوتیکهای پیشگیرانه میتوانند به پیشگیری از عفونت، در زنانی که تحت برداشتن ناحیه تبدیل دهانه رحم قرار میگیرند، کمک کند، شواهد با کیفیتی ارائه ندادند.[۲۳]
درمان جراحی نئوپلازی دروناپیتلیومی با افزایش خطر ناباروری یا کمباروری همراه است. مطالعه موردشاهدی نشان داد که این افزایش خطر تقریباً دو برابر است.[۲۴]
یافتههای مطالعات مشاهدهای با کیفیت پایین نشان میدهد که زنانی که تحت درمان نئوپلازی دروناپیتلیومی در دوران بارداری قرار میگیرند، ممکن است در معرض افزایش خطر زایمان زودرس باشند.[۲۵][۲۶] افراد مبتلا به اچآیوی و CIN 2+، در ابتدا باید بر پایهٔ توصیههای عمومی استوار بر دستورالعملهای «انجمن اختلالات دستگاه تناسلی-تحتانی» (بهروز شده در سال ۲۰۱۲) مدیریت شوند.[۲۷]
عواقب
قبلاً تصور میشد که پیشرفتِ نئوپلازی دروناپیتلیومی درجه ۱ تا ۳ دهانه رحم به سمت سرطان، بهصورت خطی است.[۲۸][۲۹][۳۰]
با این حال بیشتر نئوپلازی دروناپیتلیومی خود به خود پسرفت میکنند. در صورت عدم درمان، حدود ۷۰ درصد از CIN 1 ظرف یک سال پسرفت میکند. ۹۰ درصد ظرف دو سال پسرفت خواهند کرد.[۳۱] حدود ۵۰ درصد موارد CIN 2 بدون درمان در طی دو سال پسرفت میکنند.[۳۲]
پیشرفت به سرطانهای دهانه رحم درجا (CIS) تقریباً در ۱۱ درصد از موارد CIN 1 و ۲۲ درصد از موارد CIN 2 رخ میدهد. پیشرفت به سمت سرطان مهاجم تقریباً در ۱٪ از موارد CIN 1 و ۵٪ از موارد CIN 2، و دست کم ۱۲٪ از موارد CIN 3 رخ میدهد.[۳]
پیشرفت به سوی سرطانی شدن، معمولاً ۱۵ سال - با دامنه ۳ تا ۴۰ سال - طول میکشد. همچنین، شواهد نشان میدهد که سرطان میتواند بدون پیشرفت قابل تشخیص در درجههای مختلف نئوپلازی دروناپیتلیومی روی دهد و نئوپلازی داخل اپیتلیال با درجه بالا میتواند بدون وجود درجه پایینتر اتفاق بیوفتد.[۱][۲۸][۳۳]
پژوهش نشان میدهد که درمان نئوپلازی دروناپیتلیومی دهانه رحم بر شانس باردار شدن فرد تأثیر نمیگذارد، اما با افزایش خطر سقط جنین در سهماهه دوم بارداری همراه است.[۳۴]
همهگیرشناسی
سالانه بین ۲۵۰٬۰۰۰ تا ۱ میلیون زن آمریکایی مبتلا به نئوپلازی دروناپیتلیومی دهانه رحم تشخیص داده میشوند. زنان میتوانند در هر سنی درگیر نئوپلازی دروناپیتلیومی شوند، اما معمولاً در سنین ۲۵ تا ۳۵ سالگی به آن مبتلا میشوند.[۱] برآورد سالانه بروز نئوپلازی دروناپیتلیومی دهانه رحم در ایالات متحده آمریکا در میان افرادی که تحت غربالگری قرار میگیرند، ۴٪ برای CIN 1 و ۵٪ برای CIN 2 و CIN 3 است.[۳۵]
منابع
- ↑ ۱٫۰ ۱٫۱ ۱٫۲ ۱٫۳ ۱٫۴ Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson; Mitchell, Richard N. (2007). Robbins Basic Pathology (8th ed.). Saunders Elsevier. pp. 718–721. ISBN 978-1-4160-2973-1.
- ↑ ۲٫۰ ۲٫۱ "Colposcopy and treatment of cervical intraepithelial neoplasia: a beginners manual". screening.iarc.fr. Retrieved 2018-12-20.
- ↑ ۳٫۰ ۳٫۱ ۳٫۲ Section 4 Gynecologic Oncology > Chapter 29. Preinvasive Lesions of the Lower Genital Tract > Cervical Intraepithelial Neoplasia in:Bradshaw, Karen D.; Schorge, John O.; Schaffer, Joseph; Halvorson, Lisa M.; Hoffman, Barbara G. (2008). Williams' Gynecology. McGraw-Hill Professional. ISBN 978-0-07-147257-9.
- ↑ "Human papillomavirus (HPV) and cervical cancer". www.who.int (به انگلیسی). Retrieved 2018-12-18.
- ↑ Boda D, Docea AO, Calina D, Ilie MA, Caruntu C, Zurac S, Neagu M, Constantin C, Branisteanu DE, Voiculescu V, Mamoulakis C, Tzanakakis G, Spandidos DA, Drakoulis N, Tsatsakis AM (March 2018). "Human papilloma virus: Apprehending the link with carcinogenesis and unveiling new research avenues (Review)". International Journal of Oncology. 52 (3): 637–655. doi:10.3892/ijo.2018.4256. PMC 5807043. PMID 29393378.
- ↑ ۶٫۰ ۶٫۱ Tainio K, Athanasiou A, Tikkinen KA, Aaltonen R, Cárdenas J, Glazer-Livson S, et al. (February 2018). "Clinical course of untreated cervical intraepithelial neoplasia grade 2 under active surveillance: systematic review and meta-analysis". BMJ. 360: k499. doi:10.1136/bmj.k499. PMC 5826010. PMID 29487049.
- ↑ DiSaia PJ, Creasman WT (2007). "Invasive cervical cancer.". Clinical Gynecologic Oncology (7th ed.). Philadelphia: Mosby Elsevier. p. 55.
- ↑ Heard I (January 2009). "Prevention of cervical cancer in women with HIV". Current Opinion in HIV and AIDS. 4 (1): 68–73. doi:10.1097/COH.0b013e328319bcbe. PMID 19339941. S2CID 25047280.
- ↑ International Collaboration of Epidemiological Studies of Cervical Cancer (2006-09-01). "Cervical carcinoma and reproductive factors: collaborative reanalysis of individual data on 16,563 women with cervical carcinoma and 33,542 women without cervical carcinoma from 25 epidemiological studies". International Journal of Cancer. 119 (5): 1108–1124. doi:10.1002/ijc.21953. ISSN 0020-7136. PMID 16570271. S2CID 29433753.
- ↑ Beutner KR, Tyring S (May 1997). "Human papillomavirus and human disease". The American Journal of Medicine. 102 (5A): 9–15. doi:10.1016/s0002-9343(97)00178-2. PMID 9217657.
- ↑ de Villiers EM, Fauquet C, Broker TR, Bernard HU, zur Hausen H (June 2004). "Classification of papillomaviruses". Virology. 324 (1): 17–27. doi:10.1016/j.virol.2004.03.033. PMID 15183049.
- ↑ Soloman D (1989). "The 1988 Bethesda System for reporting cervical/vaginal cytologic diagnoses: developed and approved at the National Cancer Institute workshop in Bethesda, MD, December 12-13, 1988". Diagnostic Cytopathology. 5 (3): 331–4. doi:10.1002/dc.2840050318. PMID 2791840. S2CID 19684695.
- ↑ Solomon D, Davey D, Kurman R, Moriarty A, O'Connor D, Prey M, et al. (April 2002). "The 2001 Bethesda System: terminology for reporting results of cervical cytology". JAMA. 287 (16): 2114–9. doi:10.1001/jama.287.16.2114. PMID 11966386.
- ↑ Melnikow J, Nuovo J, Willan AR, Chan BK, Howell LP (October 1998). "Natural history of cervical squamous intraepithelial lesions: a meta-analysis". Obstetrics and Gynecology. 92 (4 Pt 2): 727–35. doi:10.1097/00006250-199810001-00046. PMID 9764690.
- ↑ Nagi CS, Schlosshauer PW (August 2006). "Endocervical glandular involvement is associated with high-grade SIL". Gynecologic Oncology. 102 (2): 240–3. doi:10.1016/j.ygyno.2005.12.029. PMID 16472847.
- ↑ Darragh TM, Colgan TJ, Thomas Cox J, Heller DS, Henry MR, Luff RD, et al. (January 2013). "The Lower Anogenital Squamous Terminology Standardization project for HPV-associated lesions: background and consensus recommendations from the College of American Pathologists and the American Society for Colposcopy and Cervical Pathology". International Journal of Gynecological Pathology. 32 (1): 76–115. doi:10.1097/PGP.0b013e31826916c7. PMID 23202792. S2CID 205943774.
- ↑ Gajjar K, Martin-Hirsch PP, Bryant A, Owens GL (July 2016). "Pain relief for women with cervical intraepithelial neoplasia undergoing colposcopy treatment". The Cochrane Database of Systematic Reviews. 7 (7): CD006120. doi:10.1002/14651858.cd006120.pub4. PMC 6457789. PMID 27428114.
- ↑ Lowy DR, Schiller JT (May 2006). "Prophylactic human papillomavirus vaccines". The Journal of Clinical Investigation. 116 (5): 1167–73. doi:10.1172/JCI28607. PMC 1451224. PMID 16670757.
- ↑ "FDA approves Gardasil 9 for prevention of certain cancers caused by five additional types of HPV". U.S. Food and Drug Administration (FDA) (press release). 10 December 2014. Archived from the original on 10 January 2015. Retrieved 28 February 2015.
- ↑ ۲۰٫۰ ۲۰٫۱ American Congress of Obstetricians and Gynecologists, "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, American Congress of Obstetricians and Gynecologists, retrieved August 1, 2013
- ↑ Martin-Hirsch, Pierre PL; Paraskevaidis, Evangelos; Bryant, Andrew; Dickinson, Heather O (2013-12-04). "Surgery for cervical intraepithelial neoplasia". Cochrane Database of Systematic Reviews. 2014 (12): CD001318. doi:10.1002/14651858.cd001318.pub3. ISSN 1465-1858. PMC 4170911. PMID 24302546.
- ↑ Helm, C. William; Lorenz, Douglas J; Meyer, Nicholas J; Rising, William WR; Wulff, Judith L (2013-06-06). "Retinoids for preventing the progression of cervical intra-epithelial neoplasia". Cochrane Database of Systematic Reviews (6): CD003296. doi:10.1002/14651858.cd003296.pub3. ISSN 1465-1858. PMID 23740788.
- ↑ Kietpeerakool C, Chumworathayi B, Thinkhamrop J, Ussahgij B, Lumbiganon P (January 2017). "Antibiotics for infection prevention after excision of the cervical transformation zone". The Cochrane Database of Systematic Reviews. 1 (10): CD009957. doi:10.1002/14651858.cd009957.pub2. PMC 6464760. PMID 28109160.
- ↑ Kyrgiou M, Koliopoulos G, Martin-Hirsch P, Arbyn M, Prendiville W, Paraskevaidis E (February 2006). "Obstetric outcomes after conservative treatment for intraepithelial or early invasive cervical lesions: systematic review and meta-analysis". Lancet. 367 (9509): 489–98. doi:10.1016/S0140-6736(06)68181-6. PMID 16473126. S2CID 31397277.
- ↑ Kyrgiou M, Athanasiou A, Paraskevaidi M, Mitra A, Kalliala I, Martin-Hirsch P, et al. (July 2016). "Adverse obstetric outcomes after local treatment for cervical preinvasive and early invasive disease according to cone depth: systematic review and meta-analysis". BMJ. 354: i3633. doi:10.1136/bmj.i3633. PMC 4964801. PMID 27469988.
- ↑ Kyrgiou M, Athanasiou A, Kalliala IE, Paraskevaidi M, Mitra A, Martin-Hirsch PP, et al. (November 2017). "Obstetric outcomes after conservative treatment for cervical intraepithelial lesions and early invasive disease". The Cochrane Database of Systematic Reviews. 11 (11): CD012847. doi:10.1002/14651858.cd012847. PMC 6486192. PMID 29095502.
- ↑ Massad LS, Einstein MH, Huh WK, Katki HA, Kinney WK, Schiffman M, et al. (April 2013). "2012 updated consensus guidelines for the management of abnormal cervical cancer screening tests and cancer precursors". Journal of Lower Genital Tract Disease. 17 (5 Suppl 1): S1–S27. doi:10.1097/LGT.0b013e318287d329. PMID 23519301. S2CID 12551963.
- ↑ ۲۸٫۰ ۲۸٫۱ Agorastos T, Miliaras D, Lambropoulos AF, Chrisafi S, Kotsis A, Manthos A, Bontis J (July 2005). "Detection and typing of human papillomavirus DNA in uterine cervices with coexistent grade I and grade III intraepithelial neoplasia: biologic progression or independent lesions?". European Journal of Obstetrics, Gynecology, and Reproductive Biology. 121 (1): 99–103. doi:10.1016/j.ejogrb.2004.11.024. PMID 15949888.
- ↑ Hillemanns P, Wang X, Staehle S, Michels W, Dannecker C (February 2006). "Evaluation of different treatment modalities for vulvar intraepithelial neoplasia (VIN): CO(2) laser vaporization, photodynamic therapy, excision and vulvectomy". Gynecologic Oncology. 100 (2): 271–5. doi:10.1016/j.ygyno.2005.08.012. PMID 16169064.
- ↑ Rapp L, Chen JJ (August 1998). "The papillomavirus E6 proteins". Biochimica et Biophysica Acta (BBA) - Reviews on Cancer. 1378 (1): F1-19. doi:10.1016/s0304-419x(98)00009-2. PMID 9739758.
- ↑ Bosch FX, Burchell AN, Schiffman M, Giuliano AR, de Sanjose S, Bruni L, Tortolero-Luna G, Kjaer SK, Muñoz N (August 2008). "Epidemiology and natural history of human papillomavirus infections and type-specific implications in cervical neoplasia". Vaccine. 26 Suppl 10 (Supplement 10): K1-16. doi:10.1016/j.vaccine.2008.05.064. PMID 18847553. 18847553.
- ↑ «Cervical intraepithelial neoplasia: Management». UpToDate. ۵ ژانویه ۲۰۲۳.
- ↑ Monnier-Benoit S, Dalstein V, Riethmuller D, Lalaoui N, Mougin C, Prétet JL (March 2006). "Dynamics of HPV16 DNA load reflect the natural history of cervical HPV-associated lesions". Journal of Clinical Virology. 35 (3): 270–7. doi:10.1016/j.jcv.2005.09.001. PMID 16214397.
- ↑ Kyrgiou M, Mitra A, Arbyn M, Paraskevaidi M, Athanasiou A, Martin-Hirsch PP, et al. (September 2015). Cochrane Gynaecological, Neuro-oncology and Orphan Cancer Group (ed.). "Fertility and early pregnancy outcomes after conservative treatment for cervical intraepithelial neoplasia". The Cochrane Database of Systematic Reviews. 2016 (9): CD008478. doi:10.1002/14651858.CD008478.pub2. PMC 6457639. PMID 26417855.
- ↑ Insinga RP, Glass AG, Rush BB (July 2004). "Diagnoses and outcomes in cervical cancer screening: a population-based study". American Journal of Obstetrics and Gynecology. 191 (1): 105–13. doi:10.1016/j.ajog.2004.01.043. PMID 15295350.
| در ویکیانبار پروندههایی دربارهٔ نئوپلازی دروناپیتلیومی دهانه رحم موجود است. |
