کنترل ترمودینامیکی در مقابل واکنش سنتیکی

کنترل واکنش ترمودینامیکی یا کنترل واکنش سینتیکی در یک واکنش شیمیایی میتواند ترکیبات موجود در مخلوط محصولات واکنش را تعیین کند، زمانی که مسیرهای رقابتی به محصولات مختلف منجر میشوند و شرایط واکنش بر روی انتخابپذیری یا استرئوانتیوسلکتیویتی تأثیر میگذارد. این تمایز مهم است زمانی که محصول A سریعتر از محصول B شکل میگیرد، زیرا انرژی فعالسازی برای محصول A کمتر از آن برای محصول B است، با این حال محصول B پایدارتر است. در چنین مواردی، A محصول سینتیکی است و تحت کنترل سینتیکی قرار دارد و B محصول ترمودینامیکی است و تحت کنترل ترمودینامیکی قرار دارد.[۱][۲][۳]
شرایط واکنش، مانند دما، فشار یا حلال، تأثیری بر روی مسیر واکنش مورد علاقه، یعنی کنترل سینتیکی یا کنترل ترمودینامیکی، خواهند داشت. توجه کنید که این تنها در صورتی درست است که انرژی فعالسازی دو مسیر متفاوت باشد و یکی از مسیرها دارای Ea (انرژی فعالسازی) کمتری باشد.
پیشرفت کنترل ترمودینامیکی یا سینتیکی، ترکیب نهایی محصول را تعیین میکند زمانی که این مسیرهای واکنش رقابتی به محصولات مختلف منجر میشوند. شرایط واکنش، همانطور که گفته شد، بر روی انتخابپذیری واکنش تأثیر میگذارد - به عبارت دیگر، کدام مسیر انتخاب میشود.
سنتز ناهمسانگردی یک حوزه است که در آن تمایز بین کنترل سینتیکی و ترمودینامیکی بهویژه مهم است. زیرا جفت انانتیومرها، برای همه اقتضایات، انرژی آزاد گیبس یکسانی دارند، کنترل ترمودینامیکی به طور ضروری مخلوط راسمیکی را تولید میکند. بنابراین، هر واکنش کاتالیزی که محصول با اختلاف انانتیومریک غیر صفر را فراهم میکند، حداقل تحت کنترل سینتیکی جزئی است. (در بسیاری از تبدیلات ناهمسانگردی استوکیومتریک، محصولات انانتیومری به واقع به صورت یک کمپلکس با منبع کیرالیته قبل از مرحله کار، تشکیل میشوند، که به طور فنی واکنش را یک دیاستئرئوسلکتیو میکند. اگرچه چنین واکنشهایی همچنان معمولاً تحت کنترل سینتیکی هستند، اما کنترل ترمودینامیکی حداقل به طور اصولی ممکن است.)
محدوده
[ویرایش]در واکنش های دیلز-آلدرواکنش
[ویرایش]دیلز-آلدر سیکلوپنتادیئن با فوران میتواند دو محصول ایزومری تولید کند. در دمای اتاق، کنترل واکنش سینتیکی حاکم است و ایزومر 2 کمپایدارتر به عنوان محصول اصلی واکنش شکل میگیرد. در دمای ۸۱ درجه سانتیگراد و پس از زمان واکنش طولانی، تعادل شیمیایی میتواند برقرار شود و ایزومر 1 ترمودینامیکی پایدارتر شکل میگیرد.[۴]محصول exo به دلیل کمپیچیدگی استریک کمتر، پایدارتر است، در حالی که محصول endo به دلیل هماندازی مداری در حالت انتقال، مورد ترجیح قرار میگیرد.

یک مثال بینظیر و بسیار کمیاب از کنترل واکنش ترمودینامیکی و سینتیکی کامل در فرآیند واکنش دایلز-آلدر ترکیبات بیس-فوریل دیآینهای ۳ با هگزافلورو-۲-بوتین یا دیمتیل استیلن دیکاربوکسیلات (DMAD) در سال ۲۰۱۸ کشف و شرح داده شده است.[۵][۶] در دمای پایین، واکنشها به صورت کیموسلکتیو(انتخاب شیمیایی) اتفاق میافتند و منجر به صرفاً تشکیل محصولات جفت-[۴+۲] سایکلو ادیشن (۵) میشوند. تشکیل انحصاری محصولات دومینو (۶) در دمای بالا مشاهده میشود.

محاسبات نظری DFT واکنش بین هگزافلورو-۲-بوتین و دیآینهای ۳a-c انجام شد. واکنش با شروع به [4+2] سایکلو ادیشن CF3C≡CCF3 در یکی از بخشهای فوران به صورت هماهنگ از طریق TS1 رخ میدهد و مرحله محدود کننده سرعت کل فرآیند با پتانسیل فعالسازی ΔG‡ ≈ 23.1-26.8 kcal/mol است.
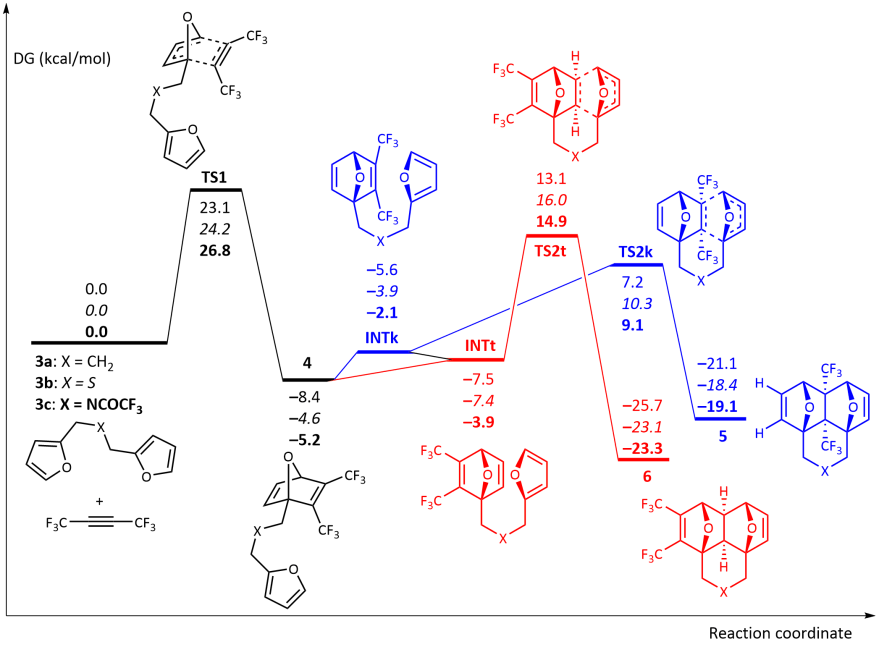
واکنش میتواند از طریق دو کانال رقابتی، یعنی یا منجر به تولید محصولات نوع پینسر 5 از طریق TS2k شود یا باعث تشکیل محصول دومینو 6 از طریق TS2t شود. محاسبات نشان داد که کانال اول به لحاظ سینتیکی مطلوبتر است (ΔG‡ ≈ 5.7-5.9 kcal/mol). در عین حال، محصولات دومینو 6 نسبت به 5 پایدارتر هستند (ΔG‡ ≈ 4.2-4.7 kcal/mol) و این موضوع ممکن است باعث ایزومریزاسیون 5 به 6 در دمای بالا شود. در واقع، میزان فعالسازی محاسبه شده برای ایزومریزاسیون 5 به 6 از طریق واکنش دایلز-آلدر رترویی 5 و سپس سایکلوادیشن [۴+۲] داخلمولکولی در میانجی زنجیرهای 4 برای تولید 6، 34.0-34.4 kcal/mol است.
منابع
[ویرایش]- ↑ Organic Chemistry, 3rd ed., M. A. Fox & J. K. Whitesell, Jones & Bartlett, 2004 شابک ۰−۷۶۳۷−۲۱۹۷−۲
- ↑ A Guidebook to Mechanism in Organic Chemistry, 6th Edition, Peter Sykes, Pearson Prentice Hall, 1986. شابک ۰−۵۸۲−۴۴۶۹۵−۳
- ↑ Introduction to Organic Chemistry I, Seth Robert Elsheimer, Blackwell Publishing, 2000 شابک ۰−۶۳۲−۰۴۴۱۷−۹
- ↑ Advanced Organic Chemistry Part A: Structure and Mechanisms, 5th ed., Francis A. Carey, Richard J. Sundberg, 2007 شابک ۹۷۸−۰−۳۸۷−۴۴۸۹۹−۲
- ↑ Kseniya K. Borisova, Elizaveta A. Kvyatkovskaya, Eugeniya V. Nikitina, Rinat R. Aysin, Roman A. Novikov, and Fedor I. Zubkov. “A Classical Example of Total Kinetic and Thermodynamic Control. The Diels-Alder Reaction between DMAD and Bis-furyl Dienes.” J. Org. Chem., 2018, 83 (8), pp 4840-4850. doi:10.1021/acs.joc.8b00336 https://pubs.acs.org/doi/abs/10.1021/acs.joc.8b00336
- ↑ Kseniya K. Borisova, Eugeniya V. Nikitina, Roman A. Novikov, Victor N. Khrustalev, Pavel V. Dorovatovskii, Yan V. Zubavichus, Maxim L. Kuznetsov, Vladimir P. Zaytsev, Alexey V. Varlamov and Fedor I. Zubkov. “Diels–Alder reactions between hexafluoro-2-butyne and bis-furyl dienes: kinetic versus thermodynamic control.” Chem. Commun., 2018, 54, pp 2850-2853. doi:10.1039/c7cc09466c http://pubs.rsc.org/en/content/articlelanding/2018/cc/c7cc09466c#!divAbstract
