مهندسی بافت عصبی
مهندسی بافت عصبی (انگلیسی: Neural tissue engineering) مهندسی بافت عصبی یک زمینه ویژهای از مهندسی بافت است. مهندسی بافت عصبی اصولاً به دنبال استراتژیهایی است برای از بین بردن التهاب و فساد الیاف در هنگام کاشتن مواد خارجی. اغلب مواد خارجی در شکل پیوندها و داربستها کاشته میشوند تا احیای عصب را بهبود بخشند و آسیب ناشی از اعصاب هر دو سیستم عصبی مرکزی (CNS) و سیستم عصبی محیطی (PNS) را جبران کنند.
معرفی[ویرایش]
سیستم عصبی به دو بخش تقسیم میشود: CNS و PNS. CNS شامل مغز و نخاع است، در حالی که PNS شامل اعصابی است که از مغز و نخاع منشأ میگیرد و بقیه بدن را از به حرکت درمیاورد. نیاز به مهندسی بافت عصبی ناشی از دشوار بودن بازسازی مجدد سلولهای عصبی و بافتهای عصبی بعد از رخ دادن آسیب عصبی است. PNS برخی قابلیتهای بازسازی سلولهای عصبی را دارد اما به صورت محدود. یافتههای تشکیل بافت عصبی سلولهای بنیادی بزرگسالان در CNS در کالبدشکافی بافت عصبی، ناحیه سابونتوکرال (SVZ) و نخاع دیده میشود. آسیبهای ناشی از CNS میتواند ناشی از سکته مغزی، اختلالات از بین برنده عصب، ضربه روحی یا هر گونه بیماری مغزی غیرروانی باشد. تعدادی روش که در حال حاضر برای درمان آسیبهای ناشی از CNS مورد بررسی قرار میگیرند عبارتند از: کاشت سلولهای بنیادی مستقیماً در محل آسیب، تحویل عاملهای شیمیایی مورفوژن به محل جراحت یا رشد سلولهای عصبی در شرایط آزمایشگاهی با سلولهای بنیادی عصبی یا سلولهای نمونه پیشرو در یک چهارچوب ۳ بعدی. استفاده پیشنهادی از چهارچوبهای فیبری پلیمر الکترو اسپون برای زیربناهای اصلاح عصبی به حداقل سال ۱۹۸۶ در یک برنامه کاربردی NIH SBIR از Simon برمی گردد. برای PNS، یک عصب جدا شده میتواند با استفاده از پیوند یا هدایت عصب موجود از طریق یک کانال مجدداً برقرار شود و حرکت کند.
تحقیقات اخیر برای ایجاد قشر مینیاتوری، که به عنوان corticopoiesis شناخته میشود، و مدلهای مغز، به نام organoids cerebral، تکنیکهایی هستند که میتوانند زمینه بازسازی بافت عصبی را افزایش دهند. پیش سازهای بومی غشایی در کورتیکوپوئیس، بافتهای عصبی هستند که میتوانند بهطور مؤثر در مغز قرار گیرند. Organoidهای مغزی، سلولهای بنیادی به بلوغ نرسیده سه بعدی هستند که به بخشهای قشر مغز گسترش مییابند، نشان میدهد که یک پتانسیل برای جداسازی و ایجاد برخی از بافتهای عصبی معین با استفاده از پیش سازهای عصبی وجود دارد.
وضعیت دیگری که برای کاشتن بافت خارجی مورد نیاز است استفاده از الکترودهای ضبط است. ایمپلنتهای الکترود مزمن ابزاری هستند که در حال حاضر در برنامههای تحقیقاتی برای ثبت سیگنالها از مناطق قشر مغزی استفاده میشود. تحقیق در مورد تقویت نورونهای PNS در بیماران مبتلا به فلج و پروتز، میتواند بیشتر از شناخت تقویت مجدد بافت عصبی در PNS و CNS باشد. این تحقیق قادر به ساخت یکی از جنبههای دشوار مهندسی بافت عصبی، تقویت عملکردی بافتهای عصبی، قابل کنترل تر.
CNS[ویرایش]
عوامل آسیب CNS[ویرایش]
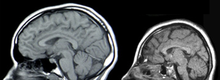
سه علت اصلی برای آسیب به سیستم عصبی CNS وجود دارد: سکته مغزی، آسیب مغز آسیب دیده (TBI) یا عوارض رشدی. سکته مغزی به عنوان هموراژیک (زمانی که یک رگ نقطه نظر نظر خونرسانی به مغز آسیب میبیند) یا ایسکمیک (زمانی که یک لخته خون جریان خون را از طریق رگ مغز متوقف میکند) طبقهبندی میشود. هنگامی که یک خونریزی اتفاق میافتد، خون به بافت اطراف میرسد و باعث مرگ بافت میشود، در حالی که خونریزیهای ایسکمیک ناشی از فقدان جریان خون به بافتهای خاص است. آسیب مغز آسیب دیده به وسیله نیروهای خارجی که بر روی جمجمه یا نخاع اثر میگذارد، ایجاد میشود. مشکلات مربوط به رشد CNS در رشد بافت غیرطبیعی در طول توسعه و در نتیجه کاهش عملکرد CNS است.
درمانها و تحقیقات کنونی[ویرایش]
کاشت سلولهای بنیادی در محل جراحت[ویرایش]
یک روش برای درمان آسیب به سیستم عصبی مرکزی، شامل کشت سلولهای بنیادی در شرایط آزمایشگاهی و کاشت سلولهای بنیادی غیرمستقیم به محل آسیب مغزی میشود. سلولهای بنیادی که بهطور مستقیم در محل آسیب قرار میگیرند، مانع از تشکیل شکاف زیستی میشوند و باعث رشد نوروژنزیس ناشی از بیمار میشوند، همچنین خطر ابتلا به تومور، التهاب و مهاجرت سلولهای بنیادی را از محل جراحت برطرف میکند. تومورژیسنس میتواند به دلیل ماهیت کنترل نشده سلولهای بنیادی ایجاد شود، التهاب میتواند به علت رد سلولهای کاشته شده توسط سلولهای میزبان رخ دهد و ماهیت بسیار مهاجرت سلولهای بنیادی باعث میشود که سلولها از محل جراحت دور شوند، بنابراین اثر دلخواه بر روی محل آسیب دیده را ندارد. سایر نگرانیهای مهندسی بافت عصبی عبارتند از ایجاد منابع ایمنی سلولهای بنیادی و دستیابی به نتایج قابل تکرار از درمانی به درمانی دیگر.
در عوض، این سلولهای بنیادی میتوانند به عنوان حامل برای درمانهای دیگر عمل کنند، اگر چه اثرات مثبت استفاده از سلولهای بنیادی به عنوان مکانیسم تحویل تأیید نشدهاست. تحویل سلولهای بنیادی مستقیم باعث افزایش اثر مثبت میشود اگر آنها به سلولهای عصبی در شرایط آزمایشگاهی هدایت شوند. به این ترتیب، خطرات ناشی از سلولهای بنیادی غیرمستقیم کاهش مییابد؛ علاوه بر این، آسیبهایی که حد خاصی ندارند، میتوانند بهطور مؤثری درمان شوند.

تحویل مولکولها به محل آسیب[ویرایش]
مولکولهایی که بازسازی بافت عصبی را بهبود میدهند، از جمله داروهای دارویی، عوامل رشد شناخته شده به عنوان مورفوژنها و miRNA نیز میتواند بهطور مستقیم به محل بافت CNS آسیب دیده معرفی شود. نوروژنزیس در حیواناتی دیده میشود که با داروهای روانگردان درمان میشوند از طریق ممانعت از بازجذب سروتونین و القاء نوروژنزیس در مغز. هنگامی که سلولهای بنیادی تمایز مییابند، سلولها مورفوژنهایی به عنوان عامل رشد گیاه برای بهبود رشد سلامتی ترشح میکنند. این مورفوژنها به حفظ هوموتازیستها و مسیرهای سیگنالینگ عصبی کمک میکند و میتوانند به محل آسیب برای بهبود آسیب بافتهای آسیب دیده تحویل داده شوند. در حال حاضر، تحویل مورفوژن به دلیل تعاملات مورفوژنها با بافت آسیب دیده حداقل منافع دارد. مورفوژنهایی که در بدن ذاتی نسیتند، اثر محدودی بر روی بافت آسیب دیده دارند به خاطر اندازه فیزیکی و تحرک محدود آنها در بافت CNS. برای درمان مؤثر، مورفوژنها باید در محل آسیب در یک غلظت خاص و ثابت حضور داشته باشد. همچنین نشان داده شدهاست که miRNA تحت تأثیر نوروژنزیس با هدایت تمایز سلولهای عصبی غیر تشخیصی قرار میگیرد.
کاشت بافت عصبی توسعه یافته در شرایط آزمایشگاهی[ویرایش]
یک روش سوم برای درمان آسیبهای ناشی از CNS این است که بافت مصنوعی خارج از بدن را به داخل محل آسیب وارد کند. این روش میتواند آسیبهایی را که از حفرههای بزرگ تشکیل شدهاست، درمان کند، جایی که مقدار بیشتری از بافتهای عصبی نیاز به جایگزینی و بازسازی دارند. بافت عصبی در محیط آزمایشگاهی با سلولهای ساقه عصبی یا پیش سلولی در یک چهارچوب سه بعدی تشکیل میشود و بدنهای جنینی (EBs) را تشکیل میدهد. این EBها شامل یک حوزهای از سلولهای بنیادی هستند که سلولهای درونی آنها سلولهای عصبی تقسیم نشده هستند و سلولهای اطراف آن بهطور فزایندهای متفاوت هستند. چهارچوبهای سه بعدی برای پیوند بافت به محل آسیب استفاده میشوند و رابط کاربری مناسب بین بافت مصنوعی و مغز را ایجاد میکنند. چهارچوبها باید: سازگار با محیط زیست، قابل تجزیه زیستی، محل جراحت مناسب، شبیه به بافت موجود در کشش و سختی، و حمایت از سلولها و بافتهای در حال رشد باشد. ترکیبی از استفاده از سلولهای بنیادی مستقیم و چهارچوبها برای حمایت از سلولهای عصبی و بافتها، بقای سلولهای بنیادی در محل صدمه را افزایش میدهد که موجب افزایش کارایی درمان میشود.
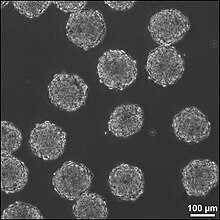
۶ نوع مختلف چهارچوب وجود دارد که برای درمان آسیب بافت عصبی در این روش مورد استفاده قرار میگیرد هیدروژل مایع از زنجیر پلیمرهای هیدروفوبیک متقاطع هستند و سلولهای بنیادی عصبی روی سطح ژل رشد میکنند یا در طول اتصال متقابل زنجیرههای پلیمری به ژل متصل میشوند. اشکال اصلی هیدروژلهای مایع، حفاظت محدودی از سلولهایی است که پیوند دارند. چهارچوبهای حمایتی از ساختارهای جامد شکل یا ساختارهای میکروپروس ساخته شدهاند و میتوانند به عنوان حامل برای سلولهای پیوند شده عمل کنند یا برای عوامل رشدی که سلولهای بنیادی در هنگام تمایز سلولهای ترشح میکنند. سلولها در سطح ماتریس در لایههای دو بعدی قرار دارند. چهارچوبهایهای حمایتی به علت اندازه چهارچوب به راحتی به محل آسیب مغزی پیوند میخورند. آنها یک ماتریس ترویج چسبندگی و تجمع سلول را فراهم میکنند، بنابراین در حال افزایش کاشت سلولی سالم افزایش یافته هستند. هموار کردن چهارچوبها میتواند بر اساس ابریشم، پلی ساکارید یا بر اساس مواد دیگر مانند هیدروژل غنی از کلاژن باشد. در حال حاضر این ژلها با الگوهای میکروتیک بر روی سطح برای بهبود رشد عضلانی افزایش مییابد. این چهارچوبها عمدتاً برای بازسازی استفاده میشود که نیاز است در یک جهت خاص مانند جراحتهای نخاعی رخ دهد. چهارچوبهای مجتمع اساساً برای حفاظت از سلولهای پیوند شده از نیروهای مکانیکی استفاده میشود که در معرض روند کاشت در محل آسیب قرار دارند. این چهارچوب همچنین احتمال ایجاد سلولهای التهابی را که در محل آسیب دیدگی قرار دارند، کاهش میدهد و به چهارجوبهایی با سلولهای بنیادی منتقل میشود. مشاهده شدهاست که رگهای خونی از طریق چهارچوب رشد میکنند، بنابراین جهارچوب و سلولها در بافت میزبان ادغام میشوند. ترکیبی از جهارجوبهای مهندسی ارائه میدهد گزینهای برای چهارچوب سه بعدی که میتواند هر دو الگوی ضروری برای چسبندگی سلول و انعطافپذیری برای انطباق با محیط همیشه در حال تغییر در محل صدمه را داشته باشد. جهارجوب ECM Decellularized یک گزینه برای چهارچوبها است زیرا آنها بافت بافتی نزدیک تری دارند، اما این چهارچوبها فقط در حال حاضر میتوانند از قطع و مجروح شدن برداشت شوند. این چهارچوبهای سه بعدی را میتوان با استفاده از اشباع ذرات، فوم گاز، پیوند فیبر، ریختهگری حلال یا تکنیکهای الکتروفیزین ساخت. هر تکنیک یک چهارچوب با خواص مختلف نسبت به تکنیکهای دیگر ایجاد میکند. پیروی از موفقیت چهارچوبهای سه بعدی به CNS نشان داده شدهاست که بستگی دارد به مرحلهای که سلولها تمایز یافتهاند. مراحل بعدی تأمین یک پروتئین کارآمدتر میباشد، در حالی که سلولهای پیش از مواجهه باید در معرض عواملی قرار گیرند که سلولها را مجبور به تمایز و در نتیجه به شکلی مناسب به سیگنالهای دریافت شده سلولها در محل آسیب ناشی از CNS پاسخ دهد. فاکتور نوروتروفیک مشتق شده مغز یک عامل پتانسیل بالقوه برای بهبود فعالسازی نورونهای حاصل از سلولهای ES در مکانهای آسیب دیدگی CNS است.
PNS[ویرایش]
عوامل آسیب PNS[ویرایش]
ضربه به شبکه عصبی بیرونی میتواند باعث آسیب شدید به عنوان یک اختلال عصبی شود، که عصب را به دو بخش پروگزیمال و دیستال تقسیم میکند. عصب دیستال به علت عدم فعالیت در طول زمان از بین میرود، در حالی که انتهای پروگزیمال در طول زمان متورم میشود. انتهای دیستال به سرعت ناپدید نمیشود و تورم انتهای پروگزیمال آن را غیرفعال نمیکند، بنابراین روشهای بازسازی اتصال بین دو انتهای عصب بررسی میشود.
درمانهای فعلی و تحقیقات[ویرایش]
اتصال دوباره با جراحی[ویرایش]
یکی از روشهای درمان صدمات ناشی از آسیب PNS، اتصال عصب قطع شده با گرفتن دو انتهای عصب و بخیه آنها به وسیله جراحی است. وقتی که اعصاب بخیه شوند، قسمتهای کوچک هرعصب دوباره به هم متصل میشوند و عصب را دوباره بازسازی میکنند. اگر چه این روش برای شکافهایی که فاصله کوچکی بین انتهای عصبهای پروگزیمال و دیستال ایجاد میکند، کارساز است، این روش به علت فشاری که باید روی انتهای عصب گذاشته شود، برای فاصلههای بیشتر کارا نیست. این تنش منجر به انحطاط عصبی میشود و بنابراین عصب نمیتواند بازسازی شود ویک اتصال عصبی کارا تشکیل دهد.
پیوند بافت[ویرایش]
پیوند بافت از اعصاب یا سایر مواد استفاده میکند تا دو انتهای عصب قطع شده را به هم متصل کند. سه دسته از پیوندهای بافتی وجود دارد: پیوندهای انسانی، پیوندهای غیرانسانی و پیوند غیرسلولی. پیوند بافت اتولوگ اعصاب را از بخشهای مختلف بدن بیمار برای پر کردن شکاف بین دو انتهای عصب آسیب دیده پیوند میزند. این عصبها معمولاً اعصابهای پوستی هستند، اما عصبهای دیگر نیزمورد تحقیق قرار گرفتهاند که نتایج امیدوارکننده است. این گروه از پیوندهای عصبی اتولوگ از استاندارد طلایی فعلی برای پیوند عصبی PNS برخوردار هستند و این به علت طبیعت سازگار با بافت زنده پیوند عصب اتولوگ است، اما مشکلاتی در رابطه با برداشتن عصب از خود بیمار و توانایی ذخیره مقدار زیادی از پیوند اتولوگ برای استفاده آینده وجود دارد پیوندهای غیرانسانی و پیوند غیرسلولی (از جمله مواد مبتنی بر ECM) بافتهایی هستند که از بیمار نمیآیند، بلکه میتوانند از مرغها (که به عنوان بافت آلوژنیک شناخته میشوند) یا حیوانات (که به عنوان بافت زنیوژنیک شناخته میشوند) برداشت شوند. در حالیکه این بافتها دارای مزیت بیشتری نسبت به بافتهای انسانی هستند زیرا بافت از بیمار گرفته نمیشود، مشکل این روش با پتانسیل انتقال بیماری و به این ترتیب مشکلات ایمنی زایی پدیدار میشود. روشهای حذف سلولهای ایمونوژنیک، به این ترتیب که تنها بخشهای ECM بافت را پشت سر میگذارند، در حال حاضر برای افزایش اثربخشی پیوندهای بافت غیرمتعارف بررسی میشوند.
هدایت[ویرایش]
روشهای هدایت بازسازی PNS از کانالهای راهنمای عصبی برای کمک به دوباره رشد کردن آکسونها در مسیر صحیح استفاده میکنند و ممکن است عوامل رشدی که توسط هر دو انتهای عصب ترشح شدهاند، جهت رشد و تکامل مجدد ارتباط برقرار کنند. روشهای هدایت، عارضه اعصاب را کاهش میدهند و باعث افزایش قابلیت اعصاب برای انتقال پتانسیل عمل پس از اتصال مجدد میشوند. دو نوع مواد در روشهای هدایت بازسازی PNS استفاده میشود: مواد طبیعی و مواد مصنوعی.
مواد طبیعی بر اساس چهارچوبهای اصلاح شده از اجزای ECM و glycosaminoglycans است. لامینین، کلاژن و فیبرونکتین، که همه اجزای ECM هستند، راهنمای توسعه آکسون هستند و باعث تحریک و فعالیت عصبی میشوند. مولکولهای دیگری که توانایی اصلاح عصب را دارند عبارتند از: اسید هیالورونیک، فیبرینوژن، ژل فیبرین، چهارچوب پپتیدهای خودآموز، آلژینات، آگاروز و کیتوزان. مواد مصنوعی همچنین روش دیگری برای بازسازی بافت ارائه میدهند که در آن خواص شیمیایی و فیزیکی پیوندها میتواند کنترل شود. از آنجایی که خواص یک ماده ممکن است برای وضعیتی که در آن استفاده میشود مشخص شود، مواد مصنوعی یک گزینه جذاب برای بازسازی PNS هستند. استفاده از مواد مصنوعی با نگرانیهای خاصی مواجه است، از قبیل: تشکیل آسان مواد پیوند درابعاد لازم، زیست تخریب، استریل پذیری، مقاومت در برابر پارگی، آسان برای کار، خطر کم عفونت، و التهاب کم در اثر مواد. مواد باید کانال را در طول بازسازی عصب حفظ کنند. در حال حاضر موادی اغلب مورد مطالعه قرار میگیرند که عمدتاً روی پلی استر تمرکز میکنند، اما پلی یورتان زیست تخریبپذیر، پلیمرهای دیگر و شیشهٔ زیست تخریب نیز مورد بررسی قرار میگیرند. سایر مواد مصنوعی پلیمرهای در حال استفاده و پلیمرهایی هستند که به لحاظ زیستی اصلاح شدهاند تا رشد آکسون سلولی را افزایش دهند و کانال آکسون را حفظ کنند.
دشواری تحقیق[ویرایش]
از آنجا که عوامل بسیاری درموفقیت یا شکست مهندسی بافت عصبی دخیل است، مشکلات زیادی در استفاده از مهندسی بافت عصبی برای درمان آسیبهای ناشی از CNS و PNS به وجود میآید. اول، درمان باید به محل صدمه وارد شود. این به این معنی است که محل صدمه باید با جراحی یا تحویل دارو به آن در دسترس قرار گیرد. هر دو روش خطرات و مشکلات ذاتی خود را دارند و با مشکلات مربوط به درمان ترکیب میشوند. نگرانی دوم حفظ درمان در محل صدمه است. سلولهای بنیادی تمایل به مهاجرت از محل آسیب به بخشهای دیگر مغز دارند، بنابراین درمان به اندازه زمانی که سلولها در محل آسیب بمانند مؤثر نیست. علاوه بر این، تحویل سلولهای بنیادی و سایر مورفوژنها به محل صدمه میتواند موجب آسیب شود، در صورتی که باعث ایجاد تومور، التهاب یا سایر اثرات غیرقابل پیشبینی شود. در نهایت، یافتههای موجود در آزمایشگاهها ممکن است به درمان بالینی عملی تبدیل نشود. درمان در آزمایشگاه موفقیتآمیز است یا حتی یک مدل حیوانی از آسیب ممکن است در یک بیمار انسانی مؤثرنباشد.
تحقیقات مرتبط[ویرایش]
مدلسازی توسعه بافت مغزی در شرایط آزمایشگاهی[ویرایش]
دو مدل برای توسعه بافت مغزی، organoids مغزی و corticopoiseis هستند. این مدلها یک مدل «در شرایط آزمایشگاهی» برای رشد طبیعی مغز را فراهم میکند اما میتوان آنها را برای نشان دادن نقایص عصبی دستکاری کرد؛ بنابراین، محققان با استفاده از این مدلها میتوانند مکانیزمهایی را برای توسعه سالم و ناکارآمد مورد مطالعه قرار دهند. این بافتها میتوانند با سلولهای بنیادی جنینی موش (ESC) یا ESC انسانی ساخته شوند. موش ESCs در یک پروتئین به نام مهارکننده Hedgehog Sonic کشت شدهاست تا از رشد پیشانی پشتی و مطالعه سرنوشت قورباغه را بهبود دهند. این روش نشان دادهاست که لایههای آکسون تولید شده از طیف وسیعی از لایههای قشر تقلید میکنند. بافتهای انسانی ESC انسان از سلولهای بنیادی پلورپوفنت استفاده میکنند تا بافتها را روی چهارچوب تشکیل دهند و EB انسانها را تشکیل دهند. این بافتهای حاصل ازESC انسانی به وسیلهٔ کشت سلولهای بنیادی انسانی در یک بیوراکتور چرخشی تشکیل میشوند.
reinnervation هدفمند[ویرایش]
reinnervation هدفمند یک روش برای تجدید ارتباطات عصبی در CNS و PNS به ویژه در بیماران فلج شده و amputees با استفاده از اندام مصنوعی است. در حال حاضر، دستگاههایی مورد بررسی قرار میگیرند که سیگنالهای الکتریکی را که از طریق نورونها در واکنش به قصد حرکت انسان ایجاد میشوند، وارد و ثبت میکنند. این تحقیق میتواند چگونگی تجدید ارتباطات عصبی بین اعصاب PNS قطع شده و ارتباط بین چهارجوبهای سه بعدی پیوند شده با CNS را روشنتر کند.[۱]
منابع[ویرایش]
- ↑ Tenore, Francesco; Vogelstein, Jacob (2011). "Revolutionizing Prothetics: Devices for Neural Integration". Johns Hopkins APL Technical Digest. 30 (3): 230–39.
- مشارکتکنندگان ویکیپدیا. «Neural tissue engineering». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۹ ژانویه ۲۰۱۸.
