اولفینیشدن جولیا: تفاوت میان نسخهها
محتوای حذفشده محتوای افزودهشده
قلی زادگان (بحث | مشارکتها) ایجاد شده توسط ترجمهٔ صفحهٔ «Julia olefination» برچسبها: عدم استفاده از یادکرد و پانویس ترجمهٔ محتوا ترجمه محتوا ۲ |
(بدون تفاوت)
|
نسخهٔ ۱ آوریل ۲۰۲۰، ساعت ۱۰:۱۳
| Julia olefination | |
|---|---|
| نامگذاری شده پس از | Marc Julia |
| نوع واکنش | Coupling reaction |
| شناسهها | |
| در درگاه شیمی آلی | julia-olefination |
| RSC ontology ID | RXNO:0000117 |
اولفینیشدن جولیا (همچنین به عنوان اولفینیشدن جولیا-لیتگو شناخته می شود) یک واکنش شیمیایی مورد استفاده در شیمی آلی است که طی آن یک فنیل سولفون (1) با یک آلدئید (یا کتون) واکنش داده و یک آلکن (الفین)(3) ایجاد می شود. در طی این فرآیند یک حد واسط (2) ایجاد می شود که پس از حذف کاهشی با استفاده از آمالگام سدیم یا ساماریم (II) یدید، محصول نهایی تولید می شود. این واکنش به نام شیمیدان فرانسوی مارک جولیا نامگذاری شده است.
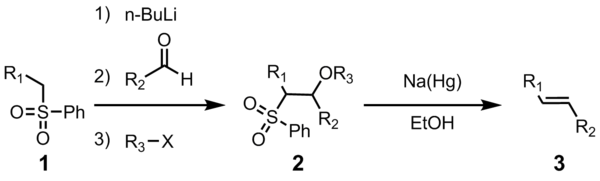
همچنین ببینید
منابع
- ^ Julia, M.; Paris, J.-M. Tetrahedron Lett. 1973, 14, 4833–4836. (doi:10.1016/S0040-4039(01)87348-2)
- ^ Kocienski, P. J.; Lythgoe, B.; Ruston, S. J. Chem. Soc., Perkin Trans. 1 1978, 829.
- ^ Keck, G. E.; Savin, K. A.; Weglarz, M. A. J. Org. Chem. 1995, 60, 3194–3204. (doi:10.1021/jo00115a041)
- ^ Kocienski, P. J. Phosphorus and Sulfur 1985, 24, 97–127. (Review)
- ^ Kelly, S. E. Comprehensive Organic Synthesis 1991, 1, 792–806. (Review) (doi:10.1016/B978-0-08-052349-1.00020-2)
- ^ Blakemore, P. R. J. Chem. Soc., Perkin Trans. 1 2002, 2563–2585. (doi:10.1039/b208078h)
- ^ Baudin, J. B.; Hareau, G.; Julia, S. A.; Ruel, O. Tetrahedron Lett. 1991, 32, 1175. (doi:10.1016/S0040-4039(00)92037-9)
- ^ Truce, W. E.; Kreider, E. M.; Brand, W. W. Org. React. 1970, 18, 99. (Review)
- ^ Paul R. Blakemore, William J. Cole, Philip J. Kocieński, Andrew Morley Synlett 1998, 26–28. (doi:10.1055/s-1998-1570)
- ^ Christophe Aïssa J. Org. Chem. 2006, 71, 360–63. (doi:10.1021/jo051693a)
- ^ Zajc, B., & Kumar, R. (2010). Synthesis of Fluoroolefins via Julia-Kocienski Olefination. Synthesis, 2010(11), 1822–1836.(doi:10.1055/s-0029-1218789)
- ^ Langcake, P.; Pryce, R. J. (1977). "A new class of phytoalexins from grapevines". Experientia 33 (2): 151–2. (doi:10.1007/BF02124034) PMID 844529.
- ^ Moro, A. V.; Cardoso, F. S. P.; Correia, C. R. D. Heck arylation of styrenes with arenediazonium salts: Short, efficient, and stereoselective synthesis of resveratrol, DMU-212, and analogues. Tetrahedron Lett. 2008, 49(39), 5668–5671.
- ^ Prabhakar Peddikotla, Amar G. Chittiboyina, Ikhlas A. Khan, (2014) ChemInform Abstract: Synthesis of Pterostilbene by Julia Olefination. ChemInform 45, doi:10.1002/chin.201408101.
- ^ Alonso DA, Fuensanta M, Nájera C, Varea M. J. Org. Chem. 2005; 70:6404–6416. PMID 16050703.
- ^ A. B. Smith, III and B. M. Brandt. Total Synthesis of (–)-Callystatin A. Org. Lett. 2001, 3, 1685-1688.
- ^ Robiette, R.; Pospíšil, J. On the Origin of E/Z Selectivity in the Modified Julia Olefination: Importance of the Elimination Step; Eur. J. Org. Chem. 2013, 836-840.
