هیدروکسید: تفاوت میان نسخهها
محتوای حذفشده محتوای افزودهشده
جز تمیزکاری یادکردها (وظیفه ۱۹) |
والسلام |
||
| خط ۱: | خط ۱: | ||
[[پرونده:Hydroxide lone pairs-2D.svg|100px|بندانگشتی|[[ساختار لوویس]] یون هیدروکسید]] |
[[پرونده:Hydroxide lone pairs-2D.svg|100px|بندانگشتی|[[ساختار لوویس]] یون هیدروکسید]] |
||
'''هیدروکسید'''{{انگلیسی|Hydroxide}} یک [[آنیون]] دو اتمی با یک بار منفی است که از یک [[اتم]] [[اکسیژن]] و یک اتم [[هیدروژن]] که با [[پیوند کووالانسی]] به هم متصل شدهاند، تشکیل شده است. |
'''هیدروکسید'''{{انگلیسی|Hydroxide}} یک [[آنیون]] دو اتمی با یک بار منفی است که از یک [[اتم]] [[اکسیژن]] و یک اتم [[هیدروژن]] که با [[پیوند کووالانسی]] به هم متصل شدهاند، تشکیل شده است.والسلام |
||
== منابع == |
== منابع == |
||
نسخهٔ ۱ ژوئیهٔ ۲۰۱۹، ساعت ۰۹:۲۸
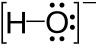
هیدروکسید(به انگلیسی: Hydroxide) یک آنیون دو اتمی با یک بار منفی است که از یک اتم اکسیژن و یک اتم هیدروژن که با پیوند کووالانسی به هم متصل شدهاند، تشکیل شده است.والسلام
منابع
- Holleman, A.F.; Wiberg, E.; Wiberg, N. (2001). Inorganic Chemistry. Academic press. ISBN 0123526515.
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3rd ed.). Prentice Hall. ISBN 978-0131755536.
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Oxford: Butterworth-Heinemann. ISBN 0080379419.
{{cite book}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - Shriver, D.F; Atkins, P.W (1999). Inorganic Chemistry (3rd ed.). Oxford: Oxford University Press. ISBN 019850330X.
- Wells, A.F (1962). Structural Inorganic Chemistry (3rd. ed.). Oxford: Clarendon Press. ISBN 0198551258.
