پیوند هیدروژنی: تفاوت میان نسخهها
بدون خلاصۀ ویرایش برچسبها: ویرایش همراه ویرایش از برنامهٔ همراه |
|||
| خط ۱: | خط ۱: | ||
[[پرونده:Acac.png|بندانگشتی|چپ|300px|Intramolecular hydrogen bonding in [[اکاک]] helps stabilize the [[enol]] tautomer]] |
[[پرونده:Acac.png|بندانگشتی|چپ|300px|Intramolecular hydrogen bonding in [[اکاک]] helps stabilize the [[enol]] tautomer]] |
||
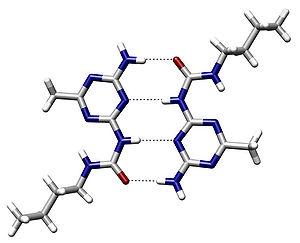
[[پرونده:Hydrogen_Bond_Quadruple_AngewChemIntEd_1998_v37_p75.jpg|thumbnail|300px|مثالی از پیوند هیدروژنی بین ملکولی، گزارش از |
[[پرونده:Hydrogen_Bond_Quadruple_AngewChemIntEd_1998_v37_p75.jpg|thumbnail|300px|مثالی از پیوند هیدروژنی بین ملکولی، گزارش از Beijer و همکاران (۱۹۹۸).<ref>{{cite journal|author=Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer| journal=[[Angew. Chem. Int. Ed.]] |title= Self-Complementarity Achieved through Quadruple Hydrogen Bonding| year= ۱۹۹۸ | volume=37 |pages= ۷۵–۷۸| doi=10.۱۰۰۲/(SICI)۱۵۲۱-۳۷۷۳(۱۹۹۸۰۲۰۲)۳۷:۱/۲<75::AID-ANIE75>۳.۰.CO;۲-R}}</ref>]] |
||
'''پیوند هیدروژنی''' بین اتمهای [[هیدروژن]] و اتمهایی که [[الکترونگاتیوی]] بالایی دارند شکل میگیرد. این پیوندها می توانند بین ملکولهای مختلف یا بین اتمهای مختلف یک مولکول (درون مولکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوندهای یونی و کووالانس ضعیفتر است. این نوع پیوند شیمیایی در هر دو نوع مولکولهای غیر آلی (مانند آب) و آلی (مانند DNA) دیده می شود./ |
'''پیوند هیدروژنی''' بین اتمهای [[هیدروژن]] و اتمهایی که [[الکترونگاتیوی]] بالایی دارند شکل میگیرد. این پیوندها می توانند بین ملکولهای مختلف یا بین اتمهای مختلف یک مولکول (درون مولکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوندهای یونی و کووالانس ضعیفتر است. این نوع پیوند شیمیایی در هر دو نوع مولکولهای غیر آلی (مانند آب) و آلی (مانند DNA) دیده می شود./ |
||
نسخهٔ ۱ اکتبر ۲۰۱۷، ساعت ۰۶:۲۶

پیوند هیدروژنی بین اتمهای هیدروژن و اتمهایی که الکترونگاتیوی بالایی دارند شکل میگیرد. این پیوندها می توانند بین ملکولهای مختلف یا بین اتمهای مختلف یک مولکول (درون مولکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوندهای یونی و کووالانس ضعیفتر است. این نوع پیوند شیمیایی در هر دو نوع مولکولهای غیر آلی (مانند آب) و آلی (مانند DNA) دیده می شود./
پیوند
این پیوند درون ترکیباتی دیده میشود که هم هیدروژن و هم عناصر با الکترونگاتیوی بالا (مانند:اکسیژن، نیتروژن، فلوئور) وجود داشته باشد.
مقایسهی انرژی پیوند هیدروژنی با دیگر پیوندها
انرژی پیوند هیدروژنی تقریبا 20 کیلوژول بر مول است . بنابراین ، پیوند هیدروژنی، ضعیفتر از پیوندهای کووالانسی یا یونی که حدود چند صد کیلوژول بر مول انرژی دارند ، می باشد اما از جاذبه های موقت با دامنه ی کوتاه که به نیروهای واندروالس معروفند - با انرژی تقریبی 4 کیلو ژول بر مول- قوی تر می باشد . بنابراین ، پیوند هیدروژنی مسئول بسیاری از خواص منحصر به فرد آب در مقایسه با مولکول هایی با اندازه ی مولکولی یکسان است .[۲]
پیوند هیدروژنی در آب

هنگامی که مولکولهای آب در کنار هم جا میگیرند، میان اتم اکسیژن از یک مولکول (که جزئی بار منفی دارد) و اتم هیدروژن از مولکول دیگر (که جزئی بار مثبت دارد) نوعی کشش یا پیوند «الکترواستاتیکی» شکل میگیرد که همان پیوند هیدروژنی است.
به دلیل نظم تقریبا ۴ وجهی الکترونها پیرامون مولکول آب، هر مولکول آب به طور بالقوه میتواند با ۴ مولکول آب دیگر پیوند هیدروژنی برقرار کند. همین پیوند هیدروژنی میان مولکولهای آب، موجب پيوستگي سطحی شدید روی آب مایع شده است.
پیوند هیدروژنی موجب ویژگیهای شگفتی در آب شده است. برای نمونه:
- بالا بودن ظرفیت گرمایی
- بالا بودن گرمای نهان تبخیر
- افزایش حجم غیرعادی در مقابل کاهش دما( از 0 تا 4-درجه سانتی گراد )[۳]
آب پیوندی
پیوند هیدروژنی علاوه بر ایجاد واکنش بین مولکول های آب ، مسئول جاذبه ی بین مولکول های آب با سایر مولکول ها یا سطوح است . به عنوان مثال ، پیوند هیدروژنی اساس تشکیل لایه آبی است که در اطراف ماکرومولکول های مهم بیولوژیکی نظیر پروتئین ها ، اسیدهای نوکلئیک و کربوهیدرات ها وجود دارد . این لایه ها به طور محکم پیوند برقرار کرده و به شدت آرایش یافته اند ، اغلب به آب پیوندی Bound water معروفند . برآورد شده است که آب پیوندی 30 درصد وزن خشک مولکول های پروتئین هیدراته را تشکیل می دهد . آب پیوندی برای پایداری مولکول های پروتئین مهم است . آب پیوندی لایه ای ضربه گیر در اطراف پروتئین ایجاد می کند که مانع از نزدیکی زیاد مولکول ها و در نتیجه (مانع از ) توده ای شدن و رسوب آن ها می شود.[۴] در آب شناسی آب پیوندی لایه بسیار نازکی است که مواد معدنی را احاطه می کند .
پانویس
- ↑ Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer (1998). "Self-Complementarity Achieved through Quadruple Hydrogen Bonding". Angew. Chem. Int. Ed. 37: ۷۵–۷۸. doi:10.۱۰۰۲/(SICI)۱۵۲۱-۳۷۷۳(۱۹۹۸۰۲۰۲)۳۷:۱/۲<75::AID-ANIE75>۳.۰.CO;۲-R.
{{cite journal}}: Check|doi=value (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ مقدمه ای بر فیزیولوژی گیاهی ، ویلیام ج هاپکینز ترجمه علی احمدی ، پرویز احسان زاده ، فرهاد جباری، انتشارات دانشگاه تهران صفحه ی 51
- ↑ کتاب شیمی اول دبیرستان2 فصل اول
- ↑ مقدمه ای بر فیزیولوژی گیاهی ، ویلیام ج هاپکینز ترجمه علی احمدی ، پرویز احسان زاده ، فرهاد جباری، انتشارات دانشگاه تهران صفحه ی 52 و 53
منابع
- مشارکتکنندگان ویکیپدیا. «Hydrogen bond». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۹ ژانویه ۲۰۰۸.
پیوند به بیرون
- The Bubble Wall (Audio slideshow from the National High Magnetic Field Laboratory explaining cohesion, surface tension and hydrogen bonds)
- isotopic effect on bond dynamics
| در ویکیانبار پروندههایی دربارهٔ پیوند هیدروژنی موجود است. |
