پیوند هیدروژنی: تفاوت میان نسخهها
محتوای حذفشده محتوای افزودهشده
قرار دادن {{دادههای کتابخانهای}} با اطلاعات ویکیداده |
تصحیح کووالانت به کووالانس |
||
| خط ۱: | خط ۱: | ||
[[پرونده:Acac.png|بندانگشتی|چپ|300px|Intramolecular hydrogen bonding in [[اکاک]] helps stabilize the [[enol]] tautomer]] |
[[پرونده:Acac.png|بندانگشتی|چپ|300px|Intramolecular hydrogen bonding in [[اکاک]] helps stabilize the [[enol]] tautomer]] |
||
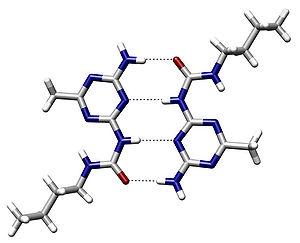
[[پرونده:Hydrogen_Bond_Quadruple_AngewChemIntEd_1998_v37_p75.jpg|thumbnail|300px|مثالی از پیوند هیدروژنی بین ملکولی، گزارش از Meijer و همکاران .<ref>{{cite journal|author=Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer| journal=[[Angew. Chem. Int. Ed.]] |title= Self-Complementarity Achieved through Quadruple Hydrogen Bonding| year= ۱۹۹۸ | volume=37 |pages= ۷۵–۷۸| doi=10.۱۰۰۲/(SICI)۱۵۲۱-۳۷۷۳(۱۹۹۸۰۲۰۲)۳۷:۱/۲<75::AID-ANIE75>۳.۰.CO;۲-R}}</ref>]] |
[[پرونده:Hydrogen_Bond_Quadruple_AngewChemIntEd_1998_v37_p75.jpg|thumbnail|300px|مثالی از پیوند هیدروژنی بین ملکولی، گزارش از Meijer و همکاران .<ref>{{cite journal|author=Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer| journal=[[Angew. Chem. Int. Ed.]] |title= Self-Complementarity Achieved through Quadruple Hydrogen Bonding| year= ۱۹۹۸ | volume=37 |pages= ۷۵–۷۸| doi=10.۱۰۰۲/(SICI)۱۵۲۱-۳۷۷۳(۱۹۹۸۰۲۰۲)۳۷:۱/۲<75::AID-ANIE75>۳.۰.CO;۲-R}}</ref>]] |
||
'''پیوند هیدروژنی''' بین اتمهای [[هیدروژن]] و اتمهایی که [[الکترونگاتیوی]] بالایی دارند برقرار میشود. این پیوندها می توانند بین ملکولهای مختلف و یا بین اتمهای مختلف یک ملکول (درون ملکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوند واندروالس مستحکمتر است اما از پیوندهای یونی و |
'''پیوند هیدروژنی''' بین اتمهای [[هیدروژن]] و اتمهایی که [[الکترونگاتیوی]] بالایی دارند برقرار میشود. این پیوندها می توانند بین ملکولهای مختلف و یا بین اتمهای مختلف یک ملکول (درون ملکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوند واندروالس مستحکمتر است اما از پیوندهای یونی و کووالانس ضعیفتر است. این نوع پیوند شیمیایی در هر دو نوع ملکولهای غیر آلی (مانند آب) و آلی (مانند DNA) دیده می شود. |
||
== پیوند == |
== پیوند == |
||
نسخهٔ ۱۰ اکتبر ۲۰۱۵، ساعت ۱۳:۰۷

پیوند هیدروژنی بین اتمهای هیدروژن و اتمهایی که الکترونگاتیوی بالایی دارند برقرار میشود. این پیوندها می توانند بین ملکولهای مختلف و یا بین اتمهای مختلف یک ملکول (درون ملکولی) ایجاد شوند. پیوند هیدروژنی (۵-۳۰ kj/mol) از پیوند واندروالس مستحکمتر است اما از پیوندهای یونی و کووالانس ضعیفتر است. این نوع پیوند شیمیایی در هر دو نوع ملکولهای غیر آلی (مانند آب) و آلی (مانند DNA) دیده می شود.
پیوند
این پیوند درون ترکیباتی دیده میشود که هم هیدروژن و هم عناصر با الکترونگاتیوی بالا (مانند:اکسیژن، نیتروژن، فلوئور) وجود داشته باشد.
پیوند هیدروژنی در آب

پیوند هیدروژنی موجب خواص عجیبی در آب شده است. مثلا:
- بالا بودن ظرفیت گرمایی
- بالا بودن گرمای نهان تبخیر
- افزایش حجم غیرعادی در مقابل کاهش دما( از -۴ درجه سانتیگراد تا ۰ درجه سانتی گراد )[۲]
پانویس
- ↑ Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer (1998). "Self-Complementarity Achieved through Quadruple Hydrogen Bonding". Angew. Chem. Int. Ed. 37: ۷۵–۷۸. doi:10.۱۰۰۲/(SICI)۱۵۲۱-۳۷۷۳(۱۹۹۸۰۲۰۲)۳۷:۱/۲<75::AID-ANIE75>۳.۰.CO;۲-R.
{{cite journal}}: Check|doi=value (help)نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link) - ↑ کتاب شیمی اول دبیرستان2 فصل اول
منابع
- مشارکتکنندگان ویکیپدیا. «Hydrogen bond». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۹ ژانویه ۲۰۰۸.
پیوند به بیرون
- The Bubble Wall (Audio slideshow from the National High Magnetic Field Laboratory explaining cohesion, surface tension and hydrogen bonds)
- isotopic effect on bond dynamics
| در ویکیانبار پروندههایی دربارهٔ پیوند هیدروژنی موجود است. |
