پلیمرهای واکنش دهنده به دما
پلیمرهای واکنش دهنده به دما یا پلیمرهای حرارتی پلیمرهایی هستند که تغییر چشمگیر و ناپیوسته از خصوصیات فیزیکی آنها با دما که با تغییر آن تغییر میکند را نشان میدهند[۱] این اصطلاح معمولاً زمانی مورد استفاده قرار میگیرد که خاصیت مورد نظر حلالیت در یک حلال معین باشد، اما در صورت آسیب دیدن سایر خواص نیز ممکن است مورد استفاده قرار گیرد. پلیمرهای گرماسنجی مربوط به طبقه مواد محرک پاسخگو هستند که بر خلاف مواد حساس به دما (برای کوتاه مدت و گرمازا) که به طور مداوم با شرایط محیطی تغییر میکنند، میباشند. به معنای دقیق تر، پلیمرهای گرماسنج، میزان شکاف مورد قبول بودن را در نمودار ترکیب دما خود نشان میدهند. بسته به اینکه امتزاج شکاف در دماهای بالا یا پایین پیدا شدهاست، به ترتیب دمای محلول انتقادی بالایی یا پایینی وجود دارد. (به صورت مختصر UCST یا LCST).
تحقیقات عمدتاً روی پلیمرهایی تمرکز دارند که گرماگرایی را در محلول آبی نشان میدهد. سطوح امیدوارکننده در زمینه کاربرد عبارتند از: مهندسی بافت،[۲] کروماتوگرافی مایع،[۳][۴] دارورسانی[۵][۶] و جدایی زیستی.[۷] فقط چند کاربرد انگشت شمار تجاری وجود دارد، به عنوان مثال، صفحات کشت سلولی که با یک پلیمر LCST پوشیده شدهاند.
تاریخچه[ویرایش]
نظریه پلیمر گرماسوز (یا همان، میکروژلها) در دهه ۱۹۴۰ با تلاشهای لوری و هاگنز که هر کدام به طور مستقل انتظارات نظری مشابهی برای پلیمر در محلول با درجه حرارت متفاوت ایجاد کردند شروع شد.
اثرات محرکهای خارجی در پلیمرهای مشخص در دهه ۱۹۶۰ میلادی توسط Heskins و Guillet مورد بررسی قرار گرفت.[۸] آنها دمای ۳۲ درجه سانتیگراد را به عنوان دمای محلول بحرانی پایین (LCST) برای پلی (N-isopropyl arrylamide) در نظر گرفتند.
انتقال سیم پیچ به گلوبول[ویرایش]
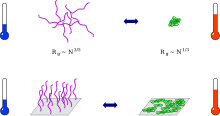
زنجیرههای پلیمری گرماسنجی در حالت محلول یک ترکیب سیم پیچ گسترده را تشکیل میدهند. در دمای جدایی فاز آنها به هم میخورند تا گلوبولهای جمع و جور تشکیل شوند. این فرایند را میتوان مستقیماً با روش پراکندگی نور استاتیک و پویا مشاهده کرد.[۹][۱۰] ولی افت ویسکوزیته را میتوان غیر مستقیم مشاهده کرد. هنگامی که مکانیسمهایی که تنش سطحی را کاهش میدهند وجود نداشته باشد، گلوبولها جمع میشوند و در نتیجه باعث کدورت و تشکیل ذرات قابل مشاهده میشوند.
نمودارهای فاز پلیمرهای گرماسنجی[ویرایش]
دمای جدایی فاز (و از این رو، نقطه ابر) به غلظت پلیمر وابسته است. از این رو، نمودارهای ترکیب دما برای نشان دادن رفتار گرمازا در طیف گستردهای از غلظتها استفاده میشوند.[۱۱] فازها به دو دستهٔ فاز فقیر پلیمر و فاز غنی تقسیم میشوند. مخلوطهای به شدت باینری که به صورت ترکیبی از مراحل همزیستی هستند را میتوان با ترسیم خطوط کراوات تعیین کرد. اگر چه، پلیمرها توزیع جرم مولی را نشان میدهند، این رویکرد ساده ممکن است کافی نباشد.
در طی فرایند جداسازی فاز، فاز پلیمر غنی میتواند قبل از رسیدن به تعادل، به حالت شیشه ای تبدیل شود. این برای هر ترکیب مستقل، وابسته به دمای گذار شیشه میباشد. اگرچه میتوانیم که منحنی انتقال شیشه را به نمودار فاز اضافه کنیم، اما تعادل واقعی نیست. تقاطع منحنی گذار شیشه ای با منحنی نقطه ابر، نقطه برغمانس نامیده میشود.[۱۲] در رابطه با پلیمرهای UCST، در بالای نقطه برغمن فازها به دو حالت مایع تقسیم میشوند، در زیر نقطهٔ برغمن به یک فاز ضعیف از پلیمر مایع و یک فاز غنی از پلیمر منجمد شده تقسیم میشود. برای پلیمرهای LCST رفتار معکوس مشاهده میشود.
ترمودینامیک[ویرایش]
هنگامی پلیمرها در حلال حل میشوند انرژی گیبس سیستم کم میشود، یعنی تغییر انرژی گیبس (ΔG) منفی است. از تحول شناخته شده لژاندر معادله گیبس - هلمولتز استنباط میشود که ΔG توسط آنتالپی اختلاط (ΔH) و آنتروپی اختلاط (ΔS) تعیین میشود.
بدون تداخل بین ترکیبات ، آنتالپی اختلاط وجود نخواهد داشت و آنتروپی اختلاط ایدهآل خواهد بود. آنتروپی ایدهآل از چندین ترکیب خالص چندگانه همیشه مثبت است (اصطلاح T∙ΔS- منفی است) و ΔG برای همه ترکیبات منفی خواهد بود و باعث اختلال در عملکرد میشود؛ بنابراین شکافهای اختلالی که مشاهده میشوند، فقط با تعامل قابل توضیح هستند. در مورد محلولهای پلیمری، اثرات متقابل پلیمر-پلیمر، حلال-حلال و پلیمر-حلال باید در نظر گرفته شوند. یک مدل برای توصیف پدیدارشناختی نمودارهای فاز پلیمری توسط فلوری و هاگنز تهیه شدهاست (به تئوری راه حل Flory-Huggins مراجعه کنید). معادله حاصله برای تغییر انرژی گیبس شامل یک اصطلاح برای آنتروپی اختلاط برای پلیمرها و یک پارامتر تعامل است که مجموع همه تعاملها را توصیف میکند.[۱۱]

که در اینجا:
- R = ثابت گاز جهانی
- m = تعداد سایتهای شبکه ای در هر مولکول (برای محلولهای پلیمری m 1 تقریباً برابر با درجه پلیمریزاسیون و m 2 = ۱ است)
- φ =به ترتیب کسر حجمی پلیمر و حلال
- پارامتر χ = پارامتر اثر متقابل
به عنوان مثال، نتیجه نظریه Flory-Huggins این است که UCST (در صورت وجود) افزایش مییابد و با افزایش جرم مولی پلیمر، به منطقه غنی از حلال تبدیل میشود. این که آیا یک پلیمر عملکرد LCST و / یا UCST را نشان میدهد، میتواند ناشی از وابستگی به دمای پارامتر تعامل باشد (شکل را ببینید). لازم به ذکر است که پارامتر تعامل نه تنها شامل سهم آنتالپیک بلکه شامل آنتروپی غیر ایدهآل مخلوط کردن، که باز هم شامل بسیاری از مشارکتهای فردی است (به عنوان مثال، اثر آبگریز قوی در محلولهای آبی) نیز هست. به همین دلایل، نظریه کلاسیک Flory-Huggins نمیتواند به بینش مولکولی شکافهای قابل قبول تعمیم دهد.
برنامههای کاربردی[ویرایش]
جدایی زیستی[ویرایش]

پلیمرهای گرماسنجی را میتوان با قسمتهایی که به زیست مولکولهای خاص متصل میشوند، عملیاتی و فعال کرد. ترکیب جفت پلیمر بیومولکول با تغییر جزئی دما میتواند از محلول رسوب شود.[۷][۱۳] جداسازی ممکن است با تصفیه یا سانتریفیوژ انجام شود.
سطوح حرارتی[ویرایش]
مهندسی بافت[ویرایش]
کروماتوگرافی[ویرایش]
ژلهای گرمازا[ویرایش]
ژلهای مرتبط با کووالانسی[ویرایش]
ژلهای فیزیکی[ویرایش]
منابع[ویرایش]
- ↑ Allan S. Hoffman, "Intelligent" Polymers in Medicine and Biotechnology, Artificial Organs, 1995, Volume 19, pp 458–467.
- ↑ Mark A. Ward; Theoni K. Georgiou (2011). "Thermoresponsive Polymers for Biomedical Applications" (PDF). Polymers. 3 (3): 1215–1242. doi:10.3390/polym3031215.
- ↑ Irene Tan; Farnoosh Roohi; Maria-Magdalena Titirici (2012). "Thermoresponsive polymers in liquid chromatography". Analytical Methods. 4 (1): 34–43. doi:10.1039/C1AY05356F.
- ↑ Pankaj Maharjan; Brad W. Woonton; Louise E. Bennett; Geoffrey W. Smithers; Kirthi DeSilva; Milton T.W. Hearn (2008). "Novel chromatographic separation — the potential of smart polymers". Innovative Food Science and Emerging Technologies. 9 (2): 232–242. doi:10.1016/j.ifset.2007.03.028.
- ↑ Mark A. Ward, Theoni K. Georgiou, Thermoresponsive Polymers for Biomedical Applications, Polymers, 2011, Volume 3, pp 1215-1242.
- ↑ A. K. Bajpai, Sandeep K. Shukla, Smitha Bhanu, Sanjana Kankane, Responsive polymers in controlled drug delivery, Progress in Polymer Science, 2008, Volume 33, pp 1088-1118.
- ↑ ۷٫۰ ۷٫۱ Igor Galaev, Bo Mattiasson, Smart Polymers for Bioseparation and Bioprocessing, CRC Press, 2001, شابک ۹۷۸۰۴۱۵۲۶۷۹۸۴.
- ↑ Michael Heskins; James E. Guillet (1968). "Solution Properties of Poly(N-isopropylacrylamide)". J. Macromol. Sci. Chem. 2 (8): 1441–1455. doi:10.1080/10601326808051910.
- ↑ C. Wu, X. Wang, Globule-to-Coil Transition of a Single Homopolymer Chain in Solution, Physical Review Letters, 1998, Volume 80, pp 4092–4094.
- ↑ S. Vshivkov, A. P. Safronov, The conformational coil-globule transition of polystyrene in cyclohexane solution, Macromolecular Chemistry and Physics, 1997, Volume 198, 3015.
- ↑ ۱۱٫۰ ۱۱٫۱ Ronald Koningsveld, Walter H. Stockmayer, Erik Nies, Polymer Phase Diagrams, Oxford University Press, Oxford, 2001, شابک ۹۷۸−۰۱۹۸۵۵۶۳۵۰.
- ↑ V. Aseyev, H. Tenhu, F. M. Winnik, Non-ionic Thermoresponsive Polymers in Water, Advances Polymer Science, 2010, Volume 242,pp 29-89.
- ↑ Jing Ping Chen, Allan S. Hoffman, Polymer-Protein Conjugates II.


