لومینول
| Luminol[۱] | |
|---|---|
| |
| |
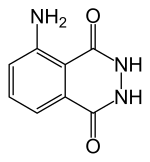
5-Amino-23-dihydro- | |
دیگر نامها o-Aminophthaloyl hydrazide | |
| شناساگرها | |
| شماره ثبت سیایاس | 521-31-3 |
| پابکم | 10638 |
| کماسپایدر | 10192 |
| شمارهٔ ئیسی | 208-309-4 |
| ChEMBL | CHEMBL442329 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | C8H7N3O2 |
| جرم مولی | 177.16 g/mol |
| دمای ذوب | ۳۱۹ درجه سلسیوس (۶۰۶ درجه فارنهایت؛ ۵۹۲ کلوین) |
| خطرات | |
| MSDS | MSDS for luminol |
| لوزی آتش | |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
لومینال (به انگلیسی: Luminol) با فرمول شیمیایی C8H7N3O2 یک ترکیب شیمیایی با شناسه پابکم 10638 است. که جرم مولی آن ۱۷۷٫۱۶ گرم بر مول میباشد. این ماده به صورت پودر زرد رنگ یا بلور های ریز یافت می شود. این ماده با اکسایش خود خاصیت نورتابی شیمیایی از خود نشان می دهد. از این ماده در آشکار سازی صحنه های جرم استفاده می شود.
تولید[ویرایش]

از واکنش ۳- نیتروفتالیک اسید با هیدرازین و تولید ۳-نیتروفتالهیدرازید و کاهش آن با استفاده از عوامل کاهنده ای چون سدیم دی تیونیت ۳- آمینوفتالهیدرازید (لومینول) تولید می شود.
خواص جالب[ویرایش]
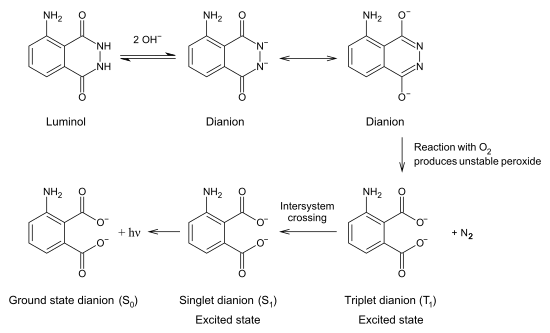
هنگامی که محلول رقیق این ماده در آب با اکسنده ای همچون واتکس (نیاز به کاتالیزور ندارد) یا هیدروژن پرکسید (نیاز به کاتالیزور دارد) مخلوط شود نور زیبای آبی تولید می گردد. همچنین می توان این ماده را در یک حلال کاملاً ناقطبی مانند کربن دی سولفید (که اکسیژن را به خوبی در خود حل می کنند) حل کرد و با هم زدن و اضافه کردن سدیم هیدروکسید (که در آن حل نمی شود) نور سبزرنگ زیبایی تولید می گردد. به این خاصیت جالب که طی واکنشی شیمیایی نور تولید میشود نورتابی شیمیایی می گویند.
جستارهای وابسته[ویرایش]
منابع[ویرایش]
- ↑ Merck Index, 11th Edition, 5470.
- "IUPAC GOLD BOOK" (به انگلیسی). International Union of Pure and Applied Chemistry. Retrieved 17 July 2013.

